Ekspert medyczny artykułu
Nowe publikacje
Siatkówka została wyhodowana z ludzkich embrionalnych komórek macierzystych
Ostatnia recenzja: 01.07.2025

Cała zawartość iLive jest sprawdzana medycznie lub sprawdzana pod względem faktycznym, aby zapewnić jak największą dokładność faktyczną.
Mamy ścisłe wytyczne dotyczące pozyskiwania i tylko linki do renomowanych serwisów medialnych, akademickich instytucji badawczych i, o ile to możliwe, recenzowanych badań medycznych. Zauważ, że liczby w nawiasach ([1], [2] itd.) Są linkami do tych badań, które można kliknąć.
Jeśli uważasz, że któraś z naszych treści jest niedokładna, nieaktualna lub w inny sposób wątpliwa, wybierz ją i naciśnij Ctrl + Enter.
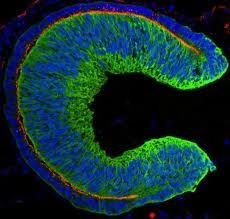
Ludzkie komórki macierzyste spontanicznie tworzą tkankę, która rozwija się w siatkówkę, tkankę w oku, która pozwala nam widzieć, zgodnie z artykułem opublikowanym w czasopiśmie Cell Stem Cell. W przyszłości przeszczep tej trójwymiarowej tkanki może pomóc pacjentom z problemami ze wzrokiem.
„To ważny kamień milowy w kolejnym etapie medycyny regeneracyjnej” – powiedział kierownik badania, profesor Yoshiki Sasai, MD, PhD, dyrektor Organogenesis and Neuroogenesis Group, RIKEN Center for Developmental Biology, Japonia. „Nasze podejście otwiera nowe perspektywy na wykorzystanie złożonych tkanek pochodzących z ludzkich komórek macierzystych w leczeniu, a także w badaniach medycznych związanych z patogenezą i rozwojem leków”.
Podczas rozwoju siatkówka – światłoczuła tkanka wyściełająca wnętrze oka – powstaje ze struktury znanej jako kielich optyczny. W nowej pracy japońskich badaczy struktura ta powstała spontanicznie z ludzkich komórek macierzystych zarodka (hESC) – komórek pochodzących z ludzkich zarodków, które mają potencjał różnicowania się w różne tkanki. Stało się to możliwe dzięki technikom hodowli komórkowej zoptymalizowanym przez profesora Sasai i jego zespół.
Komórki pochodzące z HESC organizują się w regularną trójwymiarową strukturę z dwiema warstwami kielicha optycznego, z których jedna zawiera dużą liczbę wrażliwych na światło komórek zwanych fotoreceptorami. Ponieważ zwyrodnienie siatkówki wynika przede wszystkim z uszkodzenia fotoreceptorów, tkanka pochodząca z hESC może być idealnym materiałem do przeszczepu.
Badania japońskich naukowców nie tylko otwierają dalsze perspektywy wykorzystania komórek macierzystych w medycynie regeneracyjnej, ale z pewnością przyspieszą rozwój takiej dziedziny nauk przyrodniczych, jak biologia rozwoju. Podczas eksperymentów naukowcy przekonali się, że kielich optyczny utworzony z ludzkich komórek macierzystych zarodka jest znacznie grubszy niż ten wyhodowany z mysich komórek macierzystych zarodka. Ponadto zawiera zarówno pręciki, jak i czopki, podczas gdy różnicowanie w czopki jest rzadko obserwowane w hodowli mysich ESC. Oznacza to, że komórki zarodkowe niosą specyficzne dla gatunku instrukcje dotyczące tworzenia tej struktury oka.
„Nasze badania otwierają drogę do zrozumienia cech rozwojowych oka, które są specyficzne dla człowieka i których dotychczas nie dało się zbadać” – mówi profesor Sasai.

To nie pierwszy duży sukces grupy profesora Sasai. Pod koniec zeszłego roku naukowcy wyhodowali funkcjonalny przedni płat przysadki mózgowej (adenohypophysis) z komórek macierzystych zarodka myszy, składających się z kilku różnych typów komórek produkujących hormony. Artykuł o wynikach tej pracy, Self-formation of functional adenhypophysis in three-dimensional culture, został opublikowany w czasopiśmie Nature.
Przysadka mózgowa to mały gruczoł dokrewny u podstawy mózgu, który produkuje kilka ważnych hormonów. Jest szczególnie ważny podczas wczesnego rozwoju, a możliwość naśladowania jego powstawania w laboratorium pomoże naukowcom lepiej zrozumieć embriogenezę. Nieprawidłowości w przysadce mózgowej są powiązane z zaburzeniami wzrostu, takimi jak gigantyzm i problemy ze wzrokiem, w tym ślepotą.
Ten eksperyment nie byłby możliwy bez hodowli komórkowej 3D. Przysadka mózgowa jest oddzielnym organem, ale jej rozwój wymaga sygnałów chemicznych z obszaru mózgu bezpośrednio nad nią, podwzgórza. W hodowli 3D naukowcy byli w stanie wyhodować dwa rodzaje tkanek obok siebie w tym samym czasie, co zaowocowało komórkami macierzystymi, które samorzutnie zorganizowały się w przysadkę mózgową po dwóch tygodniach.
Barwienie fluorescencyjne wykazało, że hodowana tkanka przysadki mózgowej wyrażała odpowiednie biomarkery i wydzielała hormony typowe dla przedniego płata przysadki mózgowej. Naukowcy posunęli się o krok dalej i przetestowali funkcjonalność zsyntetyzowanych organów, przeszczepiając je myszom pozbawionym przysadki mózgowej. Eksperymenty zakończyły się sukcesem: bioinżynieryjne przysadki przywróciły poziom hormonów glukokortykoidowych we krwi zwierząt i wyeliminowały objawy behawioralne, takie jak letarg. Stan myszy z wszczepionymi strukturami wykonanymi z komórek macierzystych, które nie były wystawione na niezbędne czynniki sygnałowe i dlatego nie stały się funkcjonalnym gruczołem przysadki mózgowej, nie poprawił się.
Profesor Sasai i jego koledzy planują powtórzyć eksperyment na ludzkich komórkach macierzystych i uważają, że praca ta zajmie co najmniej trzy lata.


 [
[