Nowe publikacje
Hodowla komórek macierzystych w laboratorium pozwoli przezwyciężyć odrzucenie narządów przez układ odpornościowy
Ostatnia recenzja: 30.06.2025

Cała zawartość iLive jest sprawdzana medycznie lub sprawdzana pod względem faktycznym, aby zapewnić jak największą dokładność faktyczną.
Mamy ścisłe wytyczne dotyczące pozyskiwania i tylko linki do renomowanych serwisów medialnych, akademickich instytucji badawczych i, o ile to możliwe, recenzowanych badań medycznych. Zauważ, że liczby w nawiasach ([1], [2] itd.) Są linkami do tych badań, które można kliknąć.
Jeśli uważasz, że któraś z naszych treści jest niedokładna, nieaktualna lub w inny sposób wątpliwa, wybierz ją i naciśnij Ctrl + Enter.
Badanie przeprowadzone przez naukowców z University of Texas Southwestern Medical Center, opublikowane niedawno przez Cell Press w czasopiśmie Cell Stem Cell, może pomóc w opracowaniu bardziej obiecujących strategii terapeutycznych dla przeszczepu komórek macierzystych układu krwiotwórczego. Wstępna hodowla tych komórek w laboratorium przez około tydzień może pomóc w pokonaniu jednej z najtrudniejszych przeszkód w udanej transplantacji: odrzucenia immunologicznego.
Komórki macierzyste układu krwiotwórczego (HSC) to komórki, które dają początek wszystkim rodzajom komórek krwi. Przeszczepy komórek układu krwiotwórczego są stosowane w leczeniu białaczki, chłoniaka i innych nowotworów, a także chorób autoimmunologicznych.
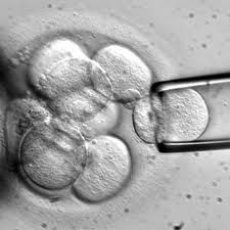
Szpik kostny. Mikrofotografia świetlna komórek macierzystych, które dają początek komórkom krwi. Białe krwinki są duże i fioletowe, czerwone krwinki są blade, a płytki krwi to małe fioletowe granulki. Komórki krwi są stale produkowane w szpiku kostnym, ponieważ ich żywotność jest tak krótka. Czerwone krwinki, płytki krwi i wszystkie trzy rodzaje białych krwinek (granulocyty, limfocyty i monocyty) pochodzą z pojedynczej komórki przodków, wielopotencjalnej komórki macierzystej. (Zdjęcie: Astrid & Hanns-Frieder Michler/Science Photo Library, P234/0030)
Jednak brak zrozumienia interakcji między hematopoetycznymi komórkami macierzystymi a układem odpornościowym biorcy znacznie komplikuje zarówno badania nad komórkami macierzystymi, jak i rozwój praktycznej transplantologii. Istnieje znaczne ryzyko, że przeszczepione komórki nie zostaną zaakceptowane przez organizm gospodarza, tj. nowe komórki zostaną odrzucone przez jego układ odpornościowy. Do głównych problemów przeszczepów allogenicznych należą niski poziom przyjęcia przeszczepów dawcy i wysokie ryzyko rozwoju zagrażającej życiu choroby przeszczep przeciwko gospodarzowi. Przeszczep oczyszczonych allogenicznych komórek macierzystych HSC zmniejsza ryzyko tego ostatniego, ale prowadzi do zmniejszenia przyjęcia przeszczepu.
Chociaż naukowcy znają niektóre z przyczyn takich niepowodzeń, wiele pytań pozostaje bez odpowiedzi. „Rozwiązanie tych problemów przyczyni się do zrozumienia immunologii komórek macierzystych układu krwiotwórczego i innych komórek macierzystych oraz znacząco przyspieszy praktyczne przeszczepy” — powiedział kierownik badań dr Cheng Cheng Zhang.
Dr Zhang i jego współpracownicy wykazali już, że ludzkie i mysie komórki macierzyste układu krwiotwórczego (HSC) można z powodzeniem hodować w laboratorium, a następnie wykorzystywać do przeszczepów. Jednocześnie obserwuje się pewne zmiany w wielu białkach wyrażanych na powierzchni takich komórek. Naukowcy byli zainteresowani tym, czy takie „doświadczenie poza ciałem” może również zmienić właściwości funkcjonalne HSC i uczynić je bardziej odpowiednimi do przeszczepów.
Transplantolodzy są szczególnie zainteresowani klinicznie istotnymi przeszczepami allogenicznymi, czyli przeszczepami między genetycznie różnymi osobami, w tym rodzeństwem i niespokrewnionymi parami dawca/biorca. Grupa dr Zhanga przeszczepiła zarówno świeżo wyizolowane, jak i laboratoryjnie wyhodowane komórki HSC myszom i odkryła, że komórki, które znajdowały się w laboratorium przez około tydzień, były znacznie mniej skłonne do zakłócania układu odpornościowego biorcy. Komórki macierzyste hematopoezy myszy hodowane ex vivo pomyślnie przekroczyły barierę głównego kompleksu zgodności tkankowej i zasiedliły szpik kostny myszy allogenicznych biorców. Przy użyciu ośmiodniowej hodowli, alloprzeszczepy były w stanie przyjąć się 40-krotnie.
Naukowcy postanowili dokładniej zbadać mechanizm leżący u podstaw tego efektu i odkryli, że do tego wzrostu przyczynił się zarówno wzrost liczby komórek macierzystych krwi (HSC), jak i wywołany hodowlą wzrost ekspresji specyficznego inhibitora układu odpornościowego CD274 (B7-H1 lub PD-L1) na powierzchni komórki.
„Ta praca powinna rzucić nowe światło na immunologię komórek macierzystych układu krwiotwórczego i innych komórek macierzystych i może doprowadzić do opracowania nowych strategii udanego przeszczepu allogenicznego” – podsumował dr Zhang. „Możliwość ekspansji ludzkich komórek macierzystych HSC dawcy w hodowli i przeszczepiania ich osobom genetycznie odległym od dawców, przy jednoczesnym uniknięciu rozwoju choroby przeszczep przeciwko gospodarzowi, rozwiąże poważny problem w tej dziedzinie”.

 [
[