Nowe publikacje
Zidentyfikowano kluczowe białko zapobiegające utracie masy kostnej w osteoporozie
Ostatnia recenzja: 02.07.2025

Cała zawartość iLive jest sprawdzana medycznie lub sprawdzana pod względem faktycznym, aby zapewnić jak największą dokładność faktyczną.
Mamy ścisłe wytyczne dotyczące pozyskiwania i tylko linki do renomowanych serwisów medialnych, akademickich instytucji badawczych i, o ile to możliwe, recenzowanych badań medycznych. Zauważ, że liczby w nawiasach ([1], [2] itd.) Są linkami do tych badań, które można kliknąć.
Jeśli uważasz, że któraś z naszych treści jest niedokładna, nieaktualna lub w inny sposób wątpliwa, wybierz ją i naciśnij Ctrl + Enter.
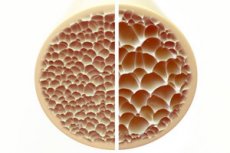
Osteoporoza, stan charakteryzujący się porowatymi i kruchymi kośćmi, stanowi poważne zagrożenie dla zdrowia szkieletu. Kości, jako podstawowe podparcie strukturalne ludzkiego ciała, zapewniają niezbędne wsparcie. Kiedy masa kostna maleje, nie tylko upośledza to wsparcie, ale także upośledza ogólną funkcję, co prowadzi do obniżenia jakości życia.
Wraz ze wzrostem częstości występowania osteoporozy w starzejącej się populacji, wzrasta obciążenie zasobów opieki zdrowotnej w zakresie opieki długoterminowej. Dlatego konieczne jest zrozumienie mechanizmów przyczyniających się do rozwoju osteoporozy i opracowanie skutecznych ukierunkowanych metod leczenia w celu zminimalizowania jej długoterminowego wpływu.
Osteoblasty i osteoklasty to dwa rodzaje komórek, które odgrywają kluczową rolę w utrzymaniu i przebudowie tkanki kostnej. Podczas gdy osteoblasty to komórki kościotwórcze odpowiedzialne za syntezę i odkładanie nowej tkanki kostnej, osteoklasty to komórki degradujące kość, które uczestniczą w rozpadzie i usuwaniu starej lub uszkodzonej tkanki kostnej.
Wzrost udziału osteoklastów prowadzi do utraty tkanki kostnej w takich schorzeniach jak osteoporoza, reumatoidalne zapalenie stawów (zapalenie stawów) i przerzuty do kości (rak, który rozprzestrzenił się do kości). Osteoklasty powstają w wyniku różnicowania makrofagów lub monocytów, które są rodzajami komórek odpornościowych.
Zatem hamowanie różnicowania osteoklastów może służyć jako strategia terapeutyczna zapobiegająca utracie kości. Jednak dokładne mechanizmy molekularne regulujące złożony proces przebudowy kości pozostają niejasne.
W nowym badaniu profesor Tadayoshi Hayata, pan Takuto Konno i pani Hitomi Murachi z Tokyo University of Science wraz ze współpracownikami zagłębili się w molekularną regulację różnicowania osteoklastów. Stymulacja ligandem receptora aktywatora czynnika jądrowego kappa B (RANKL) indukuje różnicowanie makrofagów w osteoklasty.
Ponadto szlaki sygnałowe białka morfogenetycznego kości (BMP) i transformującego czynnika wzrostu (TGF)-β zostały uwikłane w regulację różnicowania osteoklastów za pośrednictwem RANKL. W bieżącym badaniu naukowcy chcieli zbadać rolę Ctdnep1, fosfatazy (enzymu, który usuwa grupy fosforanowe), o której donoszono, że tłumi szlaki sygnałowe BMP i TGF-β.
Wyniki badania opublikowano w czasopiśmie Biochemical and Biophysical Research Communications.
Profesor Hayata stwierdza: „RANKL działa jak „przyspieszacz” różnicowania osteoklastów. Jazda samochodem wymaga nie tylko przyspieszacza, ale także hamulców. Tutaj odkryliśmy, że Ctdnep1 działa jak „hamulec” różnicowania osteoklastów”.
Naukowcy najpierw zbadali ekspresję Ctdnep1 w makrofagach myszy leczonych RANKL i nieleczonych komórkach kontrolnych. Zaobserwowali, że ekspresja Ctdnep1 nie zmieniła się w odpowiedzi na stymulację RANKL. Jednakże była zlokalizowana w cytoplazmie w postaci ziarnistej w makrofagach i różnicowała się w osteoklasty, różniąc się od swojej normalnej lokalizacji okołojądrowej w innych typach komórek, co wskazuje na jej funkcję cytoplazmatyczną w różnicowaniu osteoklastów.
Co więcej, obniżenie ekspresji genu Ctdnep1 (zmniejszenie ekspresji genów) spowodowało wzrost liczby osteoklastów wykazujących aktywność kwaśnej fosfatazy opornej na winian (TRAP), gdzie TRAP jest markerem zróżnicowanych osteoklastów.
Wybicie Ctdnep1 spowodowało zwiększoną ekspresję kluczowych markerów różnicowania, w tym „Nfatc1”, głównego czynnika transkrypcyjnego indukowanego przez RANKL w celu różnicowania osteoklastów. Wyniki te potwierdzają „funkcję hamulca” Ctdnep1, w wyniku której negatywnie reguluje różnicowanie osteoklastów. Ponadto wybicie Ctdnep1 spowodowało również zwiększoną absorpcję fosforanu wapnia, co sugeruje supresyjną rolę Ctdnep1 w resorpcji kości.
Wreszcie, chociaż wybicie Ctdnep1 nie zmieniło sygnalizacji BMP i TGF-β, komórki z niedoborem Ctdnep1 wykazały zwiększone poziomy fosforylowanych (aktywowanych) białek, które są produktami szlaku sygnałowego RANKL. Wyniki te sugerują, że hamujący wpływ Ctdnep1 na różnicowanie osteoklastów może nie być pośredniczony przez sygnalizację BMP i TGF-β, ale przez obniżenie poziomu szlaku sygnałowego RANKL i białka Nfatc1.
Ogólnie rzecz biorąc, wyniki te dostarczają nowych spostrzeżeń na temat procesu różnicowania osteoklastów i identyfikują potencjalne cele terapeutyczne, które można by wykorzystać do opracowania metod leczenia w celu zmniejszenia utraty tkanki kostnej z powodu nadmiernej aktywności osteoklastów. Oprócz chorób charakteryzujących się utratą tkanki kostnej, Ctdnep1 został również zidentyfikowany jako czynnik sprawczy w medulloblastoma, guzie mózgu u dzieci. Autorzy są optymistycznie nastawieni do tego, że ich badania można rozszerzyć na inne choroby ludzkie poza metabolizmem kości.
Profesor Hayata podsumowuje: „Nasze wyniki sugerują, że Ctdnep1 jest niezbędny do zapobiegania nadmiernej osteoklastogenezie. Wyniki te mogą poszerzyć naszą wiedzę na temat tego, w jaki sposób sieć fosforylacji-defosforylacji kontroluje różnicowanie osteoklastów i mogą dostarczyć nowych strategii terapeutycznych w leczeniu chorób kości związanych z nadmierną aktywnością osteoklastów”.
