Nowe publikacje
Zatwierdzony przez FDA TIVDAK®: celowanie w czynnik tkankowy w raku szyjki macicy
Ostatnia recenzja: 02.07.2025

Cała zawartość iLive jest sprawdzana medycznie lub sprawdzana pod względem faktycznym, aby zapewnić jak największą dokładność faktyczną.
Mamy ścisłe wytyczne dotyczące pozyskiwania i tylko linki do renomowanych serwisów medialnych, akademickich instytucji badawczych i, o ile to możliwe, recenzowanych badań medycznych. Zauważ, że liczby w nawiasach ([1], [2] itd.) Są linkami do tych badań, które można kliknąć.
Jeśli uważasz, że któraś z naszych treści jest niedokładna, nieaktualna lub w inny sposób wątpliwa, wybierz ją i naciśnij Ctrl + Enter.
29 kwietnia 2024 r. amerykańska Agencja ds. Żywności i Leków (FDA) udzieliła pełnej zgody na TIVDAK® (tisotumab vedotin) firmy Seagen Inc., lek ukierunkowany na czynnik tkankowy (TF), w leczeniu pacjentek z nawracającym lub przerzutowym rakiem szyjki macicy, który rozwinął się w trakcie lub po chemioterapii. Stanowi to znaczący przełom w terapii raka szyjki macicy, podkreślając potencjał koniugatów przeciwciał i leków (ADC) w onkologii.
Mechanizm działania leku TIVDAK
Tivdak to ADC, który atakuje czynnik transkrypcyjny (TF) poprzez połączenie monoklonalnego przeciwciała anty-TF firmy Genmab, tisotumabu, z technologią ADC firmy Seagen, mającą na celu atakowanie antygenów czynnika transkrypcyjnego (TF) na komórkach nowotworowych i dostarczanie cytotoksycznego składnika MMAE bezpośrednio do komórek nowotworowych.
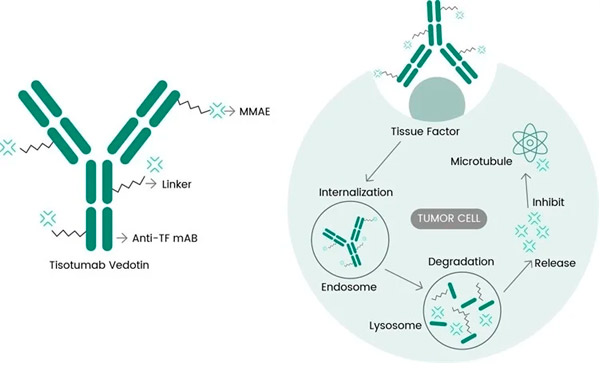
Molekularny mechanizm działania tisotumabu vedotin ( https://doi.org/10.3390/ijms23073559 )
TF: Idealny cel dla rozwoju ADC
Wiadomo, że TF bierze udział w sygnalizacji guza i angiogenezie i jest nadmiernie ekspresjonowany u zdecydowanej większości pacjentów z rakiem szyjki macicy i wieloma innymi guzami litymi. Jego zdolność do szybkiej internalizacji po związaniu przeciwciała i jego minimalny wpływ na normalne krzepnięcie krwi dodatkowo zwiększają jego przydatność do ukierunkowanej terapii nowotworowej.
