Nowe publikacje
Nowa perspektywa w neurodegeneracji: rola neurochemicznego T14 w chorobie Alzheimera
Ostatnia recenzja: 02.07.2025

Cała zawartość iLive jest sprawdzana medycznie lub sprawdzana pod względem faktycznym, aby zapewnić jak największą dokładność faktyczną.
Mamy ścisłe wytyczne dotyczące pozyskiwania i tylko linki do renomowanych serwisów medialnych, akademickich instytucji badawczych i, o ile to możliwe, recenzowanych badań medycznych. Zauważ, że liczby w nawiasach ([1], [2] itd.) Są linkami do tych badań, które można kliknąć.
Jeśli uważasz, że któraś z naszych treści jest niedokładna, nieaktualna lub w inny sposób wątpliwa, wybierz ją i naciśnij Ctrl + Enter.
Międzynarodowy zespół klinicystów i neurobiologów opublikował nowy artykuł przeglądowy na temat procesu neurodegeneracji. Ich odkrycia badają mechanizm poprzedzający powstawanie amyloidu, w tym kluczowy neurochemik, który ułatwia ten proces.
Artykuł opublikowany w czasopiśmie Alzheimer's & Dementia skupia się na jądrach izodendrytycznych, grupie neuronów, które różnią się od innych komórek mózgowych i które wcześniej uznano za szczególnie podatne na chorobę Alzheimera (AD).
Autorzy przyznają, że amyloid jest istotnym czynnikiem w późnym stadium AD, ale zauważają, że jest on nieobecny w tych neuronach na wczesnym etapie. Jeśli te wrażliwe neurony zostaną uszkodzone w wieku dorosłym, reagują, mobilizując mechanizm odpowiedzi. Mechanizm ten zazwyczaj promuje wzrost neuronów w okresie płodowym i wczesnym, ale jest szkodliwy w wieku dorosłym.
W przeglądzie opisano, w jaki sposób kluczową cząsteczką napędzającą ten proces jest bioaktywny 14-merowy peptyd T14, który selektywnie aktywuje jeden docelowy receptor. W dojrzałym mózgu zamiast przywracać normalne funkcje, T14 powoduje śmierć neuronów i inicjuje negatywną kulę śnieżną, która z czasem nabiera siły.
Jądra izodendrytyczne, zlokalizowane głęboko w mózgu, odpowiadają za pobudzenie i cykle snu/czuwania i nie są bezpośrednio powiązane z wyższymi funkcjami, takimi jak pamięć. W związku z tym proces degeneracji może trwać bez widocznych objawów, aż do momentu, gdy uszkodzenie rozprzestrzeni się na obszary odpowiedzialne za poznanie.
Wyjaśnienie zaproponowane w artykule może tłumaczyć długi, 10–20-letni okres między początkiem zaniku neuronów a wystąpieniem upośledzenia funkcji poznawczych.
W przeglądzie wykazano, że T14 można wykryć na bardzo wczesnym etapie choroby Alzheimera, co może służyć jako przedobjawowy wskaźnik początku neurodegeneracji i w związku z tym mogłoby zostać opracowane jako biomarker.
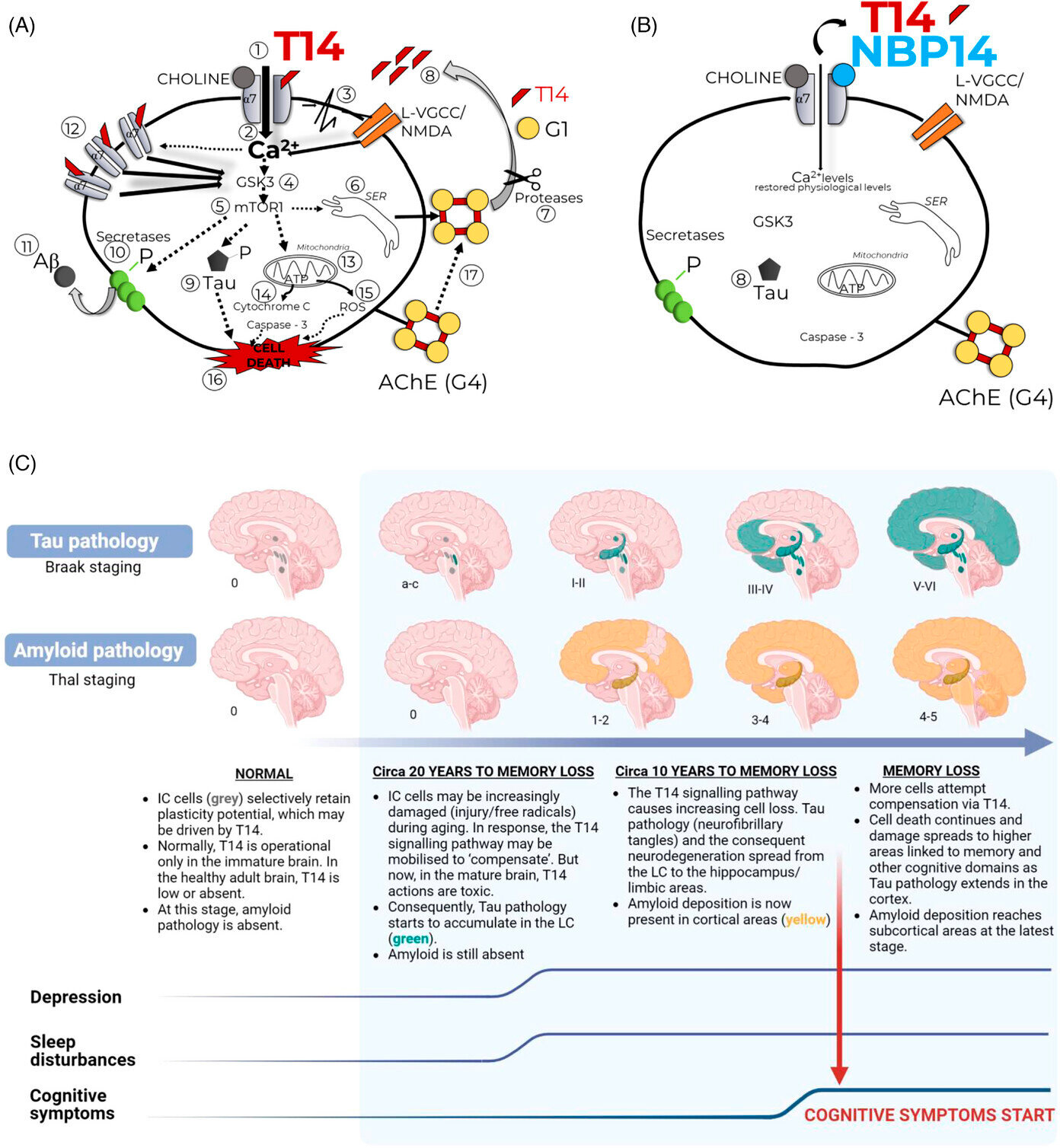
Ponadto autorzy opisują, w jaki sposób cyklizowana wersja T14, NBP14, może blokować działanie T14. Wykazano, że NBP14 zapobiega upośledzeniu pamięci w mysim modelu AD, a jego mechanizm działania został wykazany w różnych badaniach, w tym badaniach postmortem ludzkiej tkanki mózgowej. Zatem NBP14 może stanowić podstawę nowej strategii terapeutycznej.
To nowe podejście oferuje ważne odkrycia, które mogą mieć znaczący wpływ na wczesną diagnostykę i leczenie choroby Alzheimera, podkreślając wagę dalszych badań w tej dziedzinie.
