Nowe publikacje
Naukowcy śledzą najwcześniejsze zmiany fizyczne w komórkach, które powodują raka
Ostatnia recenzja: 02.07.2025

Cała zawartość iLive jest sprawdzana medycznie lub sprawdzana pod względem faktycznym, aby zapewnić jak największą dokładność faktyczną.
Mamy ścisłe wytyczne dotyczące pozyskiwania i tylko linki do renomowanych serwisów medialnych, akademickich instytucji badawczych i, o ile to możliwe, recenzowanych badań medycznych. Zauważ, że liczby w nawiasach ([1], [2] itd.) Są linkami do tych badań, które można kliknąć.
Jeśli uważasz, że któraś z naszych treści jest niedokładna, nieaktualna lub w inny sposób wątpliwa, wybierz ją i naciśnij Ctrl + Enter.
Gdy diagnozuje się raka, wiele zdarzeń na poziomie komórkowym i molekularnym zachodziło już niezauważalnie. Chociaż rak jest klasyfikowany na wczesne i późne stadia w celach klinicznych, nawet guz we wczesnym stadium jest wynikiem wielu wcześniejszych zmian w organizmie, które były niewykrywalne.
Teraz naukowcy z Yale University School of Medicine (YSM) i ich współpracownicy uzyskali szczegółowy wgląd w niektóre z tych wczesnych zmian, wykorzystując potężną mikroskopię o wysokiej rozdzielczości do śledzenia pierwszych fizycznych zmian wywołujących raka w komórkach skóry myszy.
Badając myszy z mutacją, która promuje raka w ich mieszkach włosowych, naukowcy odkryli, że pierwsze oznaki powstawania raka występują w określonym czasie i miejscu wzrostu mieszków włosowych myszy. Co więcej, odkryli, że te przedrakowe zmiany można zablokować lekami znanymi jako inhibitory MEK.
Zespołem kierował dr Tianchi Xin, adiunkt w Katedrze Genetyki YSM. W jego skład wchodziła także dr Valentina Greco, profesor genetyki w YSM i członek Yale Cancer Center oraz Yale Stem Cell Center, a także dr Sergi Regot, adiunkt biologii molekularnej i genetyki w Johns Hopkins School of Medicine.
Wyniki ich badań opublikowano w czasopiśmie Nature Cell Biology.
Naukowcy badali myszy, u których rozwinął się rak płaskonabłonkowy skóry, drugi najczęściej występujący typ raka skóry u ludzi. Myszy te zostały zmodyfikowane genetycznie, wprowadzając mutację promującą raka w genie KRAS, który jest jednym z najczęściej zmutowanych onkogenów w ludzkich nowotworach. Mutacje KRAS stwierdzono również w raku płuc, trzustki i jelita grubego.
Wczesne zmiany, które badali naukowcy, obejmowały wzrost małego, nieprawidłowego guzka w mieszku włosowym, który jest klasyfikowany jako nieprawidłowość przedrakowa. „Zrozumienie tych wczesnych zdarzeń może pomóc nam opracować podejścia zapobiegające ostatecznemu powstaniu raka” — powiedział Xin, pierwszy autor badania.
Chociaż ich badania skupiają się na raku skóry, naukowcy sądzą, że odkryte przez nich zasady można zastosować do wielu innych nowotworów wywołanych mutacjami KRAS, ponieważ kluczowe geny i białka biorące udział w tych procesach są takie same we wszystkich guzach.
Więcej niż tylko proliferacja komórek Zarówno u ludzi, jak i u myszy mieszki włosowe stale rosną, pozbywając się starych włosów i tworząc nowe. Komórki macierzyste, które mają zdolność do przekształcania się w różne typy komórek, odgrywają dużą rolę w tym procesie odnowy. Poprzednie badania wykazały, że mutacje KRAS prowadzą do zwiększonej proliferacji komórek macierzystych w mieszkach włosowych, a ten duży wzrost liczby komórek macierzystych był uważany za odpowiedzialny za przedrakowe zaburzenie tkanki.
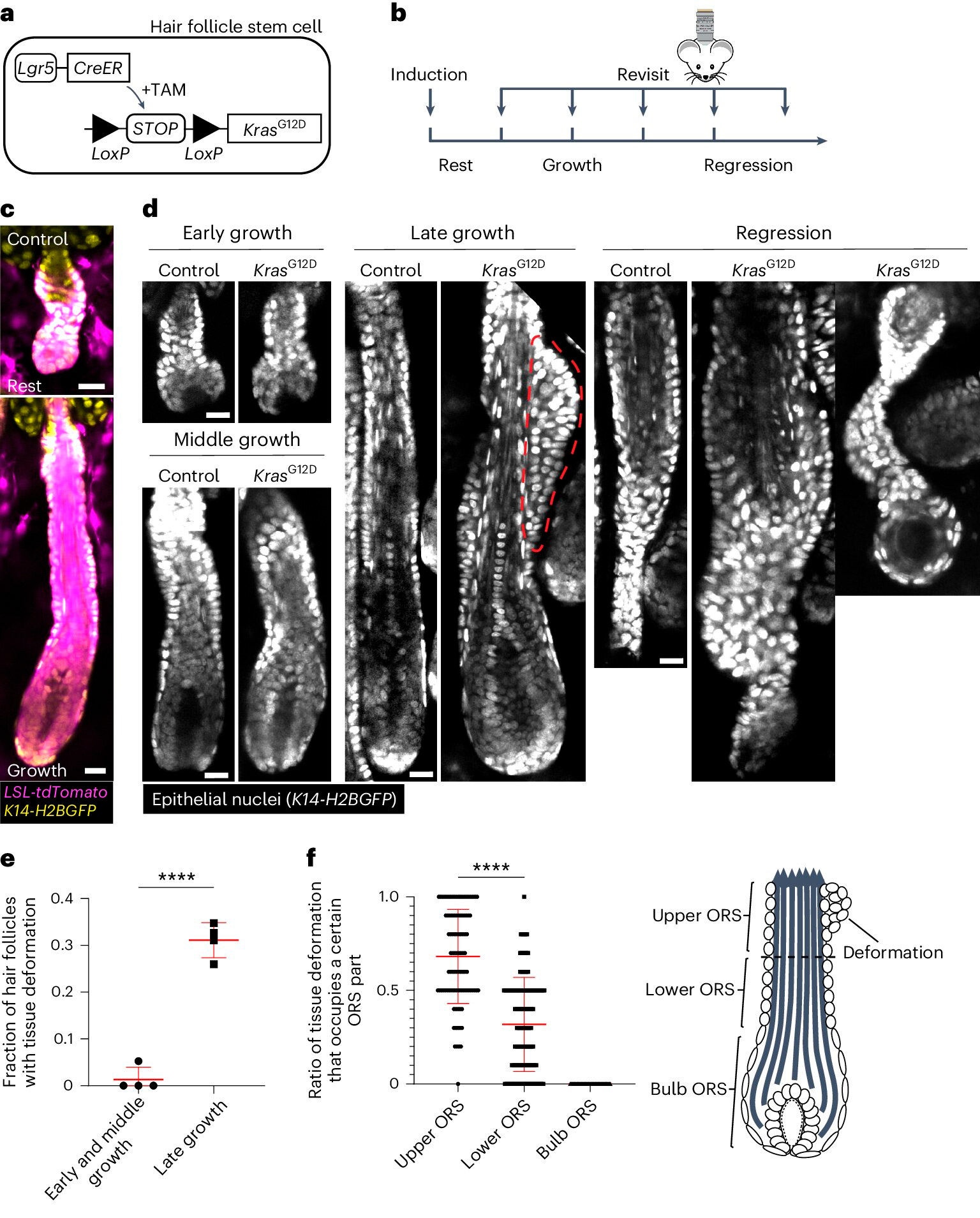
KrasG12D wywołuje przestrzenno-czasowe specyficzne deformacje tkanek podczas regeneracji mieszków włosowych.
A. Schemat podejścia genetycznego do indukcji KrasG12D w komórkach macierzystych mieszków włosowych przy użyciu indukowanego tamoksifenem układu Cre–LoxP (TAM).
B. Schemat pokazujący czas indukcji KrasG12D i ponownego obrazowania w odniesieniu do stadiów cyklu włosowego.
C. Typowe obrazy uśpionych i rosnących mieszków włosowych dzikiego typu zawierających reporter tdTomato (Magenta) indukowany Cre po indukcji.
D. Typowe obrazy mieszków włosowych kontrolnych i KrasG12D w różnych stadiach cyklu włosowego. Deformacja tkanki w postaci guzków w zewnętrznej osłonce korzenia (ORS) jest oznaczona czerwoną linią przerywaną.
E. Proporcja mieszków włosowych KrasG12D z deformacją tkanki na różnych etapach wzrostu mieszków włosowych.
F. Proporcja deformacji tkanek zajmujących górne, dolne i cebulkowe części ORS dla poszczególnych mieszków włosowych KrasG12D.
Źródło: Nature Cell Biology (2024). DOI: 10.1038/s41556-024-01413-y
Aby przetestować tę ideę, zespół wykorzystał specjalnie skonstruowaną formę zmutowanego KRAS, którą mogli aktywować w określonych momentach w komórkach skóry mieszków włosowych zwierząt. Xin i jego współpracownicy wykorzystali technikę mikroskopową znaną jako obrazowanie przyżyciowe, która umożliwia wykonywanie obrazów komórek o wysokiej rozdzielczości in vivo oraz oznaczanie i śledzenie pojedynczych komórek macierzystych u zwierząt.
Po aktywacji mutacji KRAS wszystkie komórki macierzyste zaczęły proliferować szybciej, ale przedrakowy guzek utworzył się tylko w jednym określonym miejscu w mieszku włosowym i na pewnym etapie wzrostu, co oznacza, że ogólny wzrost liczby komórek prawdopodobnie nie był całym problemem.
Aktywacja mutacji KRAS w mieszkach włosowych spowodowała szybszą proliferację komórek macierzystych, zmianę ich wzorców migracji i podział w innych kierunkach w porównaniu do komórek bez mutacji promującej raka.
Mutacja dotyczy białka znanego jako ERK. Xin był w stanie monitorować aktywność ERK w czasie rzeczywistym w poszczególnych komórkach macierzystych u żywych zwierząt i odkrył specyficzną zmianę w aktywności tego białka spowodowaną mutacją KRAS. Naukowcy byli również w stanie zatrzymać tworzenie się przedrakowego guza za pomocą inhibitora MEK, który blokuje aktywność ERK.
Lek zahamował wpływ mutacji na migrację i orientację komórek, ale nie na ogólną proliferację komórek macierzystych, co oznacza, że przyczyną powstania stanu przedrakowego są te dwie pierwsze zmiany, a nie zwiększona proliferacja komórek.
Zmiany przedrakowe w kontekście Śledzenie skutków mutacji onkogennej w czasie rzeczywistym w żywym organizmie to jedyny sposób, w jaki naukowcy byli w stanie odkryć te zasady. Jest to ważne, ponieważ nowotwory nie powstają w próżni — w dużym stopniu polegają na swoim mikrośrodowisku, aby rosnąć i utrzymywać się. Naukowcy musieli również śledzić nie tylko zachowanie poszczególnych komórek, ale także cząsteczki wewnątrz tych komórek.
„Podejście, które przyjęliśmy, aby zrozumieć te onkogenne zdarzenia, polega tak naprawdę na łączeniu się w różnych skalach” — powiedział Greco. „Struktura i podejścia, których użyli dr Xin i dr Regot, pozwoliły nam zejść do elementów molekularnych, łącząc je ze skalą komórkową i tkankową, co dało nam rozwiązanie tych zdarzeń, które jest tak trudne do osiągnięcia poza żywym organizmem”.
Naukowcy chcą teraz śledzić proces przez dłuższy okres czasu, aby zobaczyć, co się dzieje po utworzeniu się początkowego wybrzuszenia. Chcą również zbadać inne zdarzenia onkogenne, takie jak stan zapalny, aby sprawdzić, czy odkryte przez nich zasady mają zastosowanie w innych kontekstach.
