Ekspert medyczny artykułu
Nowe publikacje
Malformacja tętniczo-żylna
Ostatnia recenzja: 04.07.2025

Cała zawartość iLive jest sprawdzana medycznie lub sprawdzana pod względem faktycznym, aby zapewnić jak największą dokładność faktyczną.
Mamy ścisłe wytyczne dotyczące pozyskiwania i tylko linki do renomowanych serwisów medialnych, akademickich instytucji badawczych i, o ile to możliwe, recenzowanych badań medycznych. Zauważ, że liczby w nawiasach ([1], [2] itd.) Są linkami do tych badań, które można kliknąć.
Jeśli uważasz, że któraś z naszych treści jest niedokładna, nieaktualna lub w inny sposób wątpliwa, wybierz ją i naciśnij Ctrl + Enter.
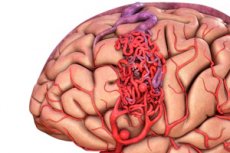
Malformacja tętniczo-żylna to wrodzona wada w rozwoju naczyń krwionośnych, która charakteryzuje się obecnością nieprawidłowej sieci zespoleń tętniczo-żylnych. Najczęściej malformacje tętniczo-żylne są zlokalizowane w tylnym dole czaszki i mają dość typową strukturę - jedną lub dwie prawdziwe tętnice, splątanie AVM i jedną żyłę odpływową.
 [ 1 ]
[ 1 ]
Przyczyny malformacja tętniczo-żylna
Przyczyny, które mogą leżeć u podstaw rozwoju AVM nie są w pełni zrozumiałe, ale uważa się, że mogą być związane z czynnikami genetycznymi i środowiskowymi. Oto niektóre z możliwych przyczyn, które mogą być związane z rozwojem AVM:
- Czynniki genetyczne: Badania wykazały, że niektórzy pacjenci z AVM mają rodzinną historię tej choroby. Mutacje genetyczne mogą odgrywać rolę w powstawaniu nieprawidłowości naczyniowych.
- Wrodzone wady: Wrodzone anomalie naczyniowe mogą rozwinąć się w trakcie rozwoju embrionalnego. Mogą być spowodowane błędami w rozwoju tkanek naczyniowych mózgu.
- Czynniki środowiskowe: Niektóre badania wykazały związek między AVM a pewnymi czynnikami środowiskowymi, takimi jak promieniowanie lub ekspozycja na substancje toksyczne w czasie ciąży. Jednak te powiązania nie zawsze są potwierdzane i nie wyjaśniają wszystkich przypadków AVM.
- Czynniki regionalne: W niektórych przypadkach AVM może być związane z określonymi obszarami geograficznymi lub grupami etnicznymi, ale powiązania te wymagają dalszych badań.
Oprócz tych czynników, które mogą wpływać na rozwój AVM, ważne jest, aby zauważyć, że jest to stan wrodzony i zwykle jest wykrywany przy urodzeniu lub we wczesnym dzieciństwie, chociaż objawy mogą pojawić się później w życiu. Potrzebne są dalsze badania, aby dokładnie zrozumieć przyczyny i mechanizmy rozwoju AVM.
Patogeneza
Najbardziej niebezpieczne jest pęknięcie ścian malformacji, któremu towarzyszy samoistny krwotok wewnątrzczaszkowy. Dzieje się tak, ponieważ mieszana krew krąży w naczyniach malformacji pod ciśnieniem zbliżonym do tętniczego. I naturalnie wysokie ciśnienie prowadzi do rozciągnięcia zdegenerowanie zmienionych naczyń, zwiększenia ich objętości i ścieńczenia ściany. Ostatecznie pęknięcie następuje w najcieńszym miejscu. Według danych statystycznych występuje to u 42-60% pacjentów z AVM. Śmiertelność przy pierwszym pęknięciu AVM sięga 12-15%. U pozostałych krwawienie może się powtarzać, bez żadnej okresowości. Obserwowaliśmy pacjenta, który miał jedenaście samoistnych krwotoków wewnątrzczaszkowych w ciągu 8 lat. Taki stosunkowo „łagodny” przebieg pęknięcia AVM w porównaniu z pęknięciem tętniaków tętniczych tłumaczy się osobliwościami zaburzeń hemodynamicznych, które występują po pęknięciu. Wiadomo, że pęknięcie tętniaka tętnicy najczęściej prowadzi do krwotoku podpajęczynówkowego (SAH) i rozwoju skurczu naczyń, który w pierwszych minutach ma charakter ochronny, pomagając szybko zatamować krwawienie, lecz później stanowi poważne zagrożenie dla życia pacjenta.
To właśnie skurcz naczyń prowadzący do niedokrwienia mózgu i obrzęku decyduje o ciężkości stanu pacjenta i rokowaniu. Natomiast skurcz naczyń tętnic doprowadzających AVM poprawia ukrwienie mózgu ze względu na zmniejszenie wypływu tętniczo-żylnego. Gdy pęka AVM, częściej tworzą się krwiaki śródmózgowe i podtwardówkowe. Przebicie się krwi do zbiorników podpajęczynówkowych jest wtórne. Krwawienie z pękniętej ściany AVM zatrzymuje się szybciej, ponieważ ciśnienie krwi w niej jest niższe niż w tętnicach głównych, a ściana jest bardziej podatna na ucisk przez rozlaną krew. Naturalnie nie zawsze kończy się to dobrze dla pacjenta. Najniebezpieczniejsze pęknięcia AVM występują w pobliżu komór mózgu, w zwojach podkorowych i w pniu mózgu. Skurcz naczyń tętnic doprowadzających w tej sytuacji pomaga zatrzymać krwawienie.
Czynnikiem decydującym w patogenezie pęknięcia AVM jest objętość rozlanej krwi i lokalizacja krwiaka. Półkuliste krwiaki śródmózgowe, nawet o objętości do 60 cm3 , przebiegają stosunkowo korzystnie. Mogą powodować ciężkie ogniskowe zaburzenia neurologiczne, ale rzadko prowadzą do ciężkich zaburzeń życiowych. Pęknięcie krwiaka do komór mózgu znacznie pogarsza rokowanie. Z jednej strony krew, drażniąc wyściółkę komór, zwiększa produkcję płynu mózgowo-rdzeniowego, z drugiej strony, wpływając na dno komory, prowadzi do ciężkich zaburzeń funkcji ośrodków życiowych zlokalizowanych w podwzgórzu. Rozprzestrzenianie się krwi w całym układzie komorowym prowadzi do tamponady tego ostatniego, co samo w sobie jest niezgodne z życiem.
Krew, która przedostała się do zbiorników podpajęczynówkowych, zaburza również krążenie płynu mózgowo-rdzeniowego, utrudniając płynowi mózgowo-rdzeniowemu dotarcie do zablokowanych krwią granulek pakchionów. W rezultacie resorpcja płynu mózgowo-rdzeniowego ulega spowolnieniu i może rozwinąć się ostre nadciśnienie płynu mózgowo-rdzeniowego, a następnie wodogłowie wewnętrzne i zewnętrzne. W wyniku rozpadu uformowanych elementów rozlanej krwi powstaje duża liczba substancji toksycznych, z których większość ma działanie wazoaktywne. Z jednej strony prowadzi to do zwężenia naczyń małych tętnic oponowych, a z drugiej strony zwiększa przepuszczalność naczyń włosowatych. Produkty rozpadu krwi wpływają również na komórki nerwowe, zmieniając ich procesy biochemiczne i zaburzając przepuszczalność błon komórkowych. Przede wszystkim zmienia się funkcja pompy potasowo-sodowej i potas zaczyna opuszczać komórkę, a kation sodowy, który jest czterokrotnie bardziej hydrofilowy niż potas, spieszy, aby zająć jego miejsce.
Prowadzi to najpierw do obrzęku wewnątrzkomórkowego w okolicy krwotoku, a następnie do obrzęku komórek. Niedotlenienie również przyczynia się do rozwoju obrzęku, który nieuchronnie dołącza się z powodu ucisku naczyń mózgowych przez krwiak i zwiększonego ciśnienia płynu mózgowo-rdzeniowego, o czym już wspomniano. Dysfunkcja części międzymózgowiowych mózgu, a przede wszystkim regulacja równowagi wodno-elektrolitowej prowadzi do zatrzymania płynów w organizmie, utraty potasu, co również nasila obrzękową reakcję mózgu. Patogeneza pęknięcia AVM nie ogranicza się do zaburzeń mózgowych. Nie mniej niebezpieczne są powikłania pozamózgowe. Przede wszystkim jest to zespół mózgowo-sercowy, który na elektrokardiogramie może symulować ostrą niewydolność wieńcową.
Dość szybko u pacjentów z krwotokami śródmózgowymi rozwija się zapalenie płuc i niewydolność oddechowa. Ponadto flora bakteryjna odgrywa drugorzędną rolę. Podstawowym efektem jest ośrodkowy wpływ na płuca, składający się z rozległego skurczu oskrzeli, zwiększonej produkcji plwociny i śluzu, niedokrwienia miąższu płucnego z powodu rozległego skurczu małych tętnic płucnych, co szybko prowadzi do zaburzeń dystroficznych, złuszczania nabłonka pęcherzykowego i zmniejszenia funkcji wymiany gazowej płuc.
Jeśli towarzyszy temu zahamowanie odruchu kaszlu, niewydolność oddechowa typu opuszkowego, wówczas powstaje poważne zagrożenie dla życia pacjenta. W większości przypadków następujące po tym ropne zapalenie trachyobronchitu jest słabo podatne na terapię antybakteryjną i zaostrza niewydolność oddechową, co bezpośrednio wpływa na wzrost niedotlenienia mózgu. Tak więc zaburzenie oddychania zewnętrznego, nawet przy względnej kompensacji zaburzeń mózgowych, może prowadzić do zgonu. Często pacjenci po śpiączce odzyskują przytomność, ale potem umierają z powodu narastającej niewydolności oddechowej i niedotlenionego obrzęku mózgu.
Zmiany dystroficzne rozwijają się szybko nie tylko w płucach, ale także w wątrobie, przewodzie pokarmowym, nadnerczach i nerkach. Zakażenia układu moczowego i odleżyny, które rozwijają się szybko przy braku dobrej opieki nad pacjentem, stanowią zagrożenie dla jego życia. Ale tych powikłań można uniknąć, jeśli lekarze o nich pamiętają i wiedzą, jak z nimi walczyć.
Podsumowując badanie patogenezy pęknięcia AVM, należy podkreślić, że śmiertelność w takich krwotokach wewnątrzczaszkowych jest niższa niż w przypadku pęknięcia tętniaków tętniczych i nadciśnieniowych udarów krwotocznych, chociaż sięga 12-15%. AVM charakteryzują się powtarzającymi się, niekiedy wielokrotnymi krwotokami o zmiennej okresowości, której nie da się przewidzieć. W przypadku niekorzystnego przebiegu okresu pokrwotocznego wymienione mechanizmy patogenetyczne mogą doprowadzić do zgonu.
Objawy malformacja tętniczo-żylna
Krwotoczny typ choroby (50-70% przypadków). Ten typ charakteryzuje się obecnością nadciśnienia tętniczego u pacjenta, niewielkim rozmiarem węzła chłonnego, jego odpływem do żył głębokich, dość powszechna jest malformacja tętniczo-żylna tylnego dołu czaszki.
Typ krwotoczny w 50% przypadków jest pierwszym objawem manifestacji malformacji tętniczo-żylnej, powoduje szczegółowy wynik i 10-15% oraz niepełnosprawność 20-30% pacjentów (N. Martin i wsp.). Roczne ryzyko krwotoku u pacjentów z malformacją tętniczo-żylną wynosi 1,5-3%. Ryzyko ponownego krwotoku w ciągu pierwszego roku sięga 8% i wzrasta wraz z wiekiem. Krwawienie z malformacji tętniczo-żylnej jest przyczyną 5-12% wszystkich zgonów matek i 23% wszystkich krwotoków wewnątrzczaszkowych u kobiet w ciąży. Obraz krwotoku podpajęczynówkowego obserwuje się u 52% pacjentów. U 17% pacjentów występują powikłane postacie krwotoku: powstawanie krwiaków śródmózgowych (38%), podtwardówkowych (2%) i mieszanych (13%), hemotamponada komór rozwija się u 47%.
Typ torpidowy przebiegu jest typowy dla pacjentów z dużymi malformacjami tętniczo-żylnymi zlokalizowanymi w korze mózgowej. Dopływ krwi do malformacji tętniczo-żylnej zapewniają gałęzie tętnicy mózgowej środkowej.
Najbardziej charakterystycznymi objawami przebiegu typu ospałego są zespół drgawkowy (u 26-27% chorych z malformacją tętniczo-żylną), klasterowe bóle głowy i postępujący deficyt neurologiczny, jak w przypadku guzów mózgu.
Warianty objawów klinicznych malformacji tętniczo-żylnych
Jak już wspomniano, najczęstszym pierwszym objawem klinicznym AVM jest samoistny krwotok wewnątrzczaszkowy (40-60% pacjentów). Często występuje bez żadnych prekursorów, w trakcie pełnego zdrowia. Momentami prowokującymi mogą być wysiłek fizyczny, sytuacja stresowa, napięcie neuropsychiczne, przyjmowanie dużych dawek alkoholu itp. W momencie pęknięcia AVM pacjenci odczuwają nagły ostry ból głowy, podobny do uderzenia lub pęknięcia. Ból szybko się nasila, powodując zawroty głowy, nudności i wymioty.

Utrata przytomności może nastąpić w ciągu kilku minut. W rzadkich przypadkach ból głowy może być łagodny, pacjenci nie tracą przytomności, ale czują, że ich kończyny słabną i stają się drętwiałe (zwykle po przeciwnej stronie krwotoku), a mowa jest upośledzona. W 15% przypadków krwotok objawia się jako pełnoobjawowy napad padaczkowy, po którym pacjenci mogą pozostać w stanie śpiączki.
Aby określić ciężkość krwotoku z AVM, można użyć podanej powyżej skali Hunta-Hessa jako podstawy z pewnymi dostosowaniami. Ze względu na fakt, że krwotoki z AVM mogą mieć bardzo różne objawy, ogniskowe objawy neurologiczne mogą przeważać nad ogólnymi objawami mózgowymi. Dlatego pacjenci z poziomem świadomości na poziomie I lub II skali mogą mieć ciężkie ogniskowe zaburzenia neurologiczne (niedowład połowiczy, niedoczulica połowicza, afazja, niedowidzenie połowicze). W przeciwieństwie do krwotoków tętniakowych, pęknięcie AVM jest określane nie przez ciężkość i częstość występowania skurczu naczyń, ale przez objętość i lokalizację krwiaka śródmózgowego.
Zespół oponowy rozwija się po kilku godzinach, a jego nasilenie może być różne. Ciśnienie krwi zwykle wzrasta, ale nie tak gwałtownie i nie tak długo, jak w przypadku pękniętych tętniaków tętniczych. Zwykle wzrost ten nie przekracza 30-40 mm Hg. Drugiego lub trzeciego dnia pojawia się hipertermia ośrodkowego pochodzenia. Stan chorych naturalnie pogarsza się, ponieważ obrzęk mózgu wzrasta, a rozpad rozlanej krwi nasila się. Trwa to do 4-5 dni. Przy korzystnym przebiegu, po ustabilizowaniu się w 6-8 dniu, stan chorych zaczyna się poprawiać. Dynamika objawów ogniskowych zależy od lokalizacji i wielkości krwiaka.
W przypadku krwotoku w funkcjonalnie ważnych rejonach mózgu lub zniszczenia przewodów ruchowych objawy utraty pojawiają się natychmiast i utrzymują się przez długi czas bez żadnej dynamiki. Jeśli objawy utraty nie pojawiają się natychmiast, ale nasilają się równolegle z obrzękiem mózgu, można spodziewać się przywrócenia deficytu w ciągu 2-3 tygodni, gdy obrzęk całkowicie ustąpi.
Obraz kliniczny pęknięcia AVM jest bardzo zróżnicowany i zależy od wielu czynników, z których najważniejsze to: objętość i lokalizacja krwotoku, nasilenie reakcji obrzęku mózgu oraz stopień zaangażowania struktur pnia mózgu w proces.
Malformacje tętniczo-żylne mogą objawiać się jako napady padaczkowe (30-40%). Przyczyną ich rozwoju mogą być zaburzenia hemokrążenia w sąsiednich obszarach mózgu z powodu zjawiska podkradania. Ponadto sama malformacja może drażnić korę mózgową, generując wyładowania padaczkowe. A już mówiliśmy o niektórych typach AVM, wokół których rozwija się glioza tkanki mózgowej, która również często objawia się napadami padaczkowymi.
Zespół padaczkowy wywołany obecnością AVM charakteryzuje się bezprzyczynowym występowaniem w wieku dorosłym, często przy całkowitym braku czynnika prowokującego. Napady padaczkowe mogą być uogólnione lub ogniskowe. Obecność wyraźnego komponentu ogniskowego w napadzie padaczkowym przy braku ogólnych objawów mózgowych powinna nasuwać myśl o możliwym AVM. Nawet napady uogólnione, jeśli zaczynają się od drgawek głównie w tych samych kończynach z wymuszonym obrotem głowy i oczu w jedną lub drugą stronę, są często manifestacją AVM. Rzadziej pacjenci doświadczają drobnych napadów, takich jak nieobecność lub świadomość zmierzchowa. Częstotliwość i okresowość napadów padaczkowych mogą być różne: od izolowanych do nawracających.
Formularze
VV Lebedev i współautorzy na podstawie danych EKG zidentyfikowali trzy warianty zespołu mózgowo-sercowego:
- Typ I – zaburzenie funkcji automatyzmu i pobudliwości (tachykardia zatokowa lub bradykardia, arytmia, migotanie przedsionków);
- Typ II – zmiany procesów repolaryzacji, przejściowe zmiany w końcowej fazie zespołu komorowego w zależności od rodzaju niedokrwienia, uszkodzenie mięśnia sercowego ze zmianami załamka T i położenia odcinka ST;
- Typ III - zaburzenie funkcji przewodzenia (blok, objawy zwiększonego obciążenia prawego serca). Te zmiany EKG mogą być łączone, a ich nasilenie koreluje z ciężkością ogólnego stanu pacjentów.
Komplikacje i konsekwencje
Malformacja tętniczo-żylna (AVM) to wrodzona anomalia naczyniowa, w której tętnice i żyły są połączone bez pośredniej warstwy naczyń włosowatych. Powikłania i konsekwencje AVM mogą być poważne i zależą od rozmiaru, lokalizacji i cech konkretnej malformacji. Niektóre z nich obejmują:
- Udar: Jednym z najpoważniejszych powikłań AVM jest ryzyko udaru. Wady rozwojowe mogą tworzyć nieprawidłowe ścieżki przepływu krwi, co może prowadzić do krwawienia w mózgu, powodując udar. Udar może mieć różny stopień nasilenia i pozostawiać resztkowe deficyty neurologiczne.
- Padaczka: AVM mogą powodować napady padaczkowe u niektórych pacjentów, szczególnie jeśli wada jest zlokalizowana w określonych obszarach mózgu.
- Krwotok: Wady rozwojowe mogą być nieprzewidywalne i powodować krwawienie w mózgu. Może to być powikłanie zagrażające życiu i prowadzić do poważnych konsekwencji.
- Wodogłowie: Jeśli AVM znajduje się w pobliżu komór mózgu, może to powodować wodogłowie, które może prowadzić do gromadzenia się dodatkowej ilości płynu w mózgu i wzrostu ciśnienia śródczaszkowego.
- Deficyty neurologiczne: AVM może uszkodzić otaczającą tkankę mózgową i wywołać różnorodne deficyty neurologiczne, w tym paraliż, zaburzenia czucia oraz deficyty mowy i koordynacji ruchowej.
- Ból i bóle głowy: Pacjenci z AVM mogą odczuwać przewlekły ból i bóle głowy związane z wadą rozwojową.
- Skutki psychologiczne: Powikłania spowodowane przez malformacje tętniczo-żylne mogą mieć istotny wpływ na samopoczucie psychiczne pacjentów, wywołując lęk, depresję i stres.
- Ograniczenia stylu życia: Po wykryciu AVM u pacjentów może być konieczna zmiana stylu życia i zalecenia dotyczące zarządzania ryzykiem, obejmujące ograniczenie aktywności fizycznej i niektórych rodzajów aktywności.
Diagnostyka malformacja tętniczo-żylna
Diagnoza malformacji tętniczo-żylnej (AVM) zazwyczaj obejmuje szereg badań obrazowych w celu potwierdzenia obecności i oceny cech malformacji. Główne metody stosowane do diagnozy AVM to:
- Angiografia rezonansu magnetycznego (MRA): MRA jest jedną z głównych metod diagnozowania AVM. Jest to nieinwazyjne badanie, które obrazuje strukturę naczyń krwionośnych i przepływ krwi w mózgu za pomocą pól magnetycznych i fal radiowych. MRA może określić lokalizację, rozmiar i kształt AVM.
- Cyfrowa angiografia subtrakcyjna (DSA): Jest to bardziej inwazyjna procedura, która polega na wstrzykiwaniu środka kontrastowego bezpośrednio do naczyń przez cewnik i wykorzystaniu promieni rentgenowskich do uzyskania wysokiej jakości obrazów naczyń mózgowych. DSA umożliwia bardziej szczegółowe badanie struktury AVM i wzorców przepływu krwi.
- Tomografia komputerowa (TK): TK może być stosowana do wykrywania AVM i oceny możliwych powikłań, takich jak krwawienie. W razie potrzeby środek kontrastowy może być stosowany w celu poprawy wizualizacji.
- Badanie tętniczo-żylne metodą duplex (ultrasonografia dupleksowa): Technika ta może być przydatna przy badaniu naczyń szyi i głowy oraz identyfikowaniu zaburzeń przepływu krwi związanych z tętniczo-żylnymi naczyniakami krwionośnymi.
- Spektroskopia rezonansu magnetycznego (MRS): MRS może dostarczyć informacji o składzie chemicznym tkanek w obszarze AVM i ujawnić oznaki zmian metabolicznych.
- Echoencefalografia: Badanie ultrasonograficzne, które można stosować w celu oceny przepływu krwi i struktury mózgu.
- Angiografia tomografii komputerowej (CTA): CTA łączy tomografię komputerową i angiografię w celu uzyskania trójwymiarowych obrazów naczyń krwionośnych w mózgu.
Po zdiagnozowaniu AVM ważne jest przeprowadzenie szczegółowej oceny cech wady, takich jak jej rozmiar, kształt i ciężkość. Pomoże to ustalić, czy leczenie jest konieczne i jaka jest najlepsza opcja leczenia, w tym usunięcie chirurgiczne, embolizacja, radioterapia lub obserwacja. Decyzja o leczeniu AVM powinna zostać podjęta wspólnie przez pacjenta i zespół opieki zdrowotnej, biorąc pod uwagę indywidualne okoliczności każdego przypadku.
Diagnostyka różnicowa
Diagnostyka różnicowa malformacji tętniczo-żylnych (AVM) może być ważnym krokiem w ocenie pacjenta ze zmianami naczyniowymi w mózgu. AVM to nieprawidłowości naczyniowe, w których tętnice i żyły są połączone bez pośredniej warstwy naczyń włosowatych. Mogą powodować różnorodne objawy i stany, a ich odróżnienie od innych zaburzeń naczyniowych jest ważne dla właściwego leczenia. Niektóre stany, które mogą wymagać diagnostyki różnicowej z AVM, obejmują:
- Udar: Udar może imitować objawy AVM, zwłaszcza jeśli udar jest spowodowany zmianami naczyniowymi. Rozróżnienie może wymagać tomografii komputerowej (TK) lub obrazowania metodą rezonansu magnetycznego (MRI) mózgu w celu uwidocznienia zmian naczyniowych.
- Krwiak: Krwiaki, takie jak krwiak podtwardówkowy lub nadtwardówkowy, mogą imitować objawy AVM, zwłaszcza jeśli towarzyszą im bóle głowy i objawy neurologiczne. Tomografia komputerowa lub rezonans magnetyczny mogą pomóc ustalić przyczynę objawów.
- Guzy mózgu: Guzy mózgu mogą powodować różne objawy, które mogą być podobne do objawów AVM. Diagnoza może obejmować MRI z kontrastem i inne badania obrazowe.
- Migrena: Migreny z aurą mogą imitować objawy AVM, takie jak zaburzenia widzenia i zawroty głowy. Historia i dodatkowe badania mogą pomóc odróżnić te dwa schorzenia.
- Zapalenie naczyń mózgowych: Zapalenie naczyń może powodować stany zapalne naczyń krwionośnych i nieprawidłowości naczyniowe, które mogą przypominać objawy AVM. Biopsja lub angiografia mogą być użyte do diagnozy zapalenia naczyń.
- Zakrzepica żylna: Zakrzepica żylna może imitować objawy AVM, zwłaszcza jeśli występuje zaburzenie odpływu żylnego z mózgu. Dodatkowe badania mogą pomóc w identyfikacji zakrzepicy.
W celu dokładnej diagnostyki różnicowej malformacji tętniczo-żylnych (AVM) badania obejmują szczegółowe badanie kliniczne, metody neuroedukacyjne (TK, MRI, angiografia), czasami biopsję i inne specjalistyczne procedury w zależności od konkretnych objawów i okoliczności.
Z kim się skontaktować?
Leczenie malformacja tętniczo-żylna
Leczenie malformacji tętniczo-żylnej (AVM) zależy od jej rozmiaru, lokalizacji, objawów i potencjalnych powikłań. W niektórych przypadkach AVM może być mała i bezobjawowa, i może nie wymagać aktywnego leczenia. Jednak jeśli występują objawy lub ryzyko krwawienia, leczenie może być konieczne. Niektóre z metod leczenia AVM obejmują:
- Chirurgia: Chirurgiczne usunięcie AVM może być rozważane w przypadkach, gdy malformacja znajduje się w dostępnym miejscu i jest mało skomplikowana. Chirurgiczne usunięcie może pomóc zapobiec ryzyku krwawienia i zmniejszyć objawy. Jest to złożona procedura i może wiązać się z ryzykiem, takim jak uszkodzenie otaczających tkanek i nerwów.
Interwencje otwarte (przezczaszkowe):
- Etap I - koagulacja naczyń aferentnych;
- Etap II - izolacja rdzenia malformacji tętniczo-żylnej;
- Etap III - podwiązanie i koagulacja odpływu oraz usunięcie malformacji tętniczo-żylnej,
Interwencje wewnątrznaczyniowe:
- nieruchoma okluzja balonowa tętnic doprowadzających - embolizacja dopływu (niekontrolowana);
- połączenie czasowej lub stałej okluzji balonowej z embolizacją przepływu;
- embolizacja superselektywna.
Malformację tętniczo-żylną leczy się również za pomocą radiochirurgii (nóż gamma, nóż cybernetyczny, nac Li itp.).
- Embolizacja: Embolizacja to zabieg polegający na wprowadzeniu materiałów medycznych lub kleju do naczyń krwionośnych w celu zablokowania przepływu krwi do AVM. Embolizacja może być stosowana jako etap przygotowawczy przed operacją lub jako samodzielne leczenie. Może pomóc zmniejszyć krwawienie i rozmiar AVM.
- Radioterapia: Radioterapia może być stosowana w leczeniu AVM, szczególnie w przypadkach, gdy inne metody leczenia mogą być zbyt ryzykowne. Radioterapia ma na celu zmniejszenie krwawienia AVM i może wymagać wielu sesji.
- Leki: W niektórych przypadkach leki mogą być stosowane w celu zmniejszenia objawów, takich jak ból lub skurcze. Leki mogą być również stosowane w celu kontrolowania ciśnienia krwi, aby zmniejszyć ryzyko krwawienia.
- Obserwacja i leczenie objawowe: W niektórych sytuacjach, zwłaszcza gdy AVM jest niewielki i nie powoduje objawów, może zostać podjęta decyzja o prostej obserwacji schorzenia i leczeniu objawowym w razie potrzeby.
Leczenie AVM musi być dostosowane indywidualnie do każdego pacjenta, a decyzja o wyborze metody zależy od konkretnych okoliczności. Ważne jest, aby omówić wszystkie opcje leczenia z pracownikiem służby zdrowia i przeprowadzić dokładną ocenę pacjenta w celu ustalenia najlepszego planu leczenia. Wyniki leczenia mogą być skuteczne, a pacjenci mogą osiągnąć poprawę lub całkowite wyzdrowienie, ale każdy przypadek jest wyjątkowy.
Prognoza
Rokowanie w przypadku malformacji tętniczo-żylnej (AVM) zależy od kilku czynników, w tym od jej rozmiaru, lokalizacji, objawów, wieku pacjenta i powodzenia leczenia. Ważne jest, aby pamiętać, że AVM to stan chorobowy, który może objawiać się inaczej u różnych pacjentów, a rokowanie może być różne u różnych osób. Oto kilka ogólnych aspektów rokowania w przypadku AVM:
- Ryzyko krwawienia: Głównym ryzykiem AVM jest ryzyko krwawienia (krwotoku) w mózgu. Małe AVM z niskim ryzykiem krwawienia mogą mieć dobre rokowanie i nie powodować poważnych problemów. Jednak duże i średnie AVM mogą stanowić znaczne ryzyko.
- Objawy: Objawy związane z AVM, takie jak bóle głowy, drgawki, paraliż lub zaburzenia sensoryczne, mogą wpływać na rokowanie. W niektórych przypadkach skuteczne leczenie może poprawić lub wyeliminować objawy.
- Rozmiar i lokalizacja: AVM zlokalizowane w bardziej niebezpiecznych miejscach, takich jak głęboko w mózgu lub w pobliżu struktur krytycznych, mogą mieć gorsze rokowanie. Jednak nawet wiele dużych AVM można skutecznie leczyć.
- Leczenie: Leczenie AVM może obejmować chirurgiczne usunięcie, embolizację, radioterapię lub leki. Skuteczne leczenie może zmniejszyć ryzyko krwawienia i poprawić rokowanie.
- Wiek: Wiek pacjenta może również wpływać na rokowanie. Dzieci i młodzi dorośli często mają lepsze rokowanie niż starsi pacjenci.
- Choroby współistniejące: Obecność innych schorzeń lub czynników ryzyka, takich jak wysokie ciśnienie krwi lub zaburzenia krzepnięcia, może mieć wpływ na rokowanie i leczenie AVM.
Ważne jest, aby pamiętać, że AVM wymaga starannego monitorowania medycznego i leczenia. Decyzję o metodzie leczenia i prognozie powinni podejmować wykwalifikowani neurochirurdzy i neuroradiolodzy na podstawie szczegółowej oceny każdego indywidualnego przypadku.

