Ekspert medyczny artykułu
Nowe publikacje
Prątki niegruźlicze
Last reviewed: 04.07.2025

Cała zawartość iLive jest sprawdzana medycznie lub sprawdzana pod względem faktycznym, aby zapewnić jak największą dokładność faktyczną.
Mamy ścisłe wytyczne dotyczące pozyskiwania i tylko linki do renomowanych serwisów medialnych, akademickich instytucji badawczych i, o ile to możliwe, recenzowanych badań medycznych. Zauważ, że liczby w nawiasach ([1], [2] itd.) Są linkami do tych badań, które można kliknąć.
Jeśli uważasz, że któraś z naszych treści jest niedokładna, nieaktualna lub w inny sposób wątpliwa, wybierz ją i naciśnij Ctrl + Enter.
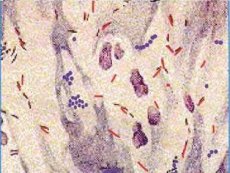
Mykobakterie niegruźlicze to niezależne gatunki, szeroko rozpowszechnione w środowisku jako saprofity, które w niektórych przypadkach mogą powodować ciężkie choroby - mykobakteriozę. Nazywane są również mykobakteriami środowiskowymi, czynnikami wywołującymi mykobakteriozę, mykobakteriami oportunistycznymi i atypowymi. Istotną różnicą między mykobakteriami niegruźliczymi a kompleksem Mycobacterium tuberculosis jest to, że praktycznie nie są przenoszone z człowieka na człowieka.
Mykobakterie niegruźlicze dzieli się na 4 grupy na podstawie ograniczonej liczby cech: szybkości wzrostu, tworzenia pigmentu, morfologii kolonii i właściwości biochemicznych.
1. grupa - wolno rosnące fotochromogeniczne (M. kansasii itp.). Główną cechą przedstawicieli tej grupy jest pojawienie się pigmentu w świetle. Tworzą kolonie od form S do RS, zawierają kryształy karotenu, barwiąc je na żółto. Tempo wzrostu wynosi od 7 do 20 dni w temperaturze 25, 37 i 40 °C, katadazo-dodatnie.
M. kansasii to żółte pałeczki, które żyją w wodzie i glebie i najczęściej atakują płuca. Bakterie te można rozpoznać po ich dużych rozmiarach i krzyżowym układzie. Ważnym objawem zakażeń wywołanych przez M. kansasii jest rozwój rozsianej choroby. Możliwe są również zmiany skórne i tkanki miękkie, rozwój zapalenia pochewki ścięgna, zapalenia kości i szpiku, zapalenia węzłów chłonnych, zapalenia osierdzia i zakażeń układu moczowo-płciowego.
2. grupa - wolno rosnące scotochromogeniczne (M. scrofulaceum, M. matmoense, M. gordonae itp.). Mikroorganizmy tworzą żółte kolonie w ciemności i pomarańczowe lub czerwonawe kolonie w świetle, zwykle kolonie w kształcie litery S, rosną w temperaturze 37 °C. Jest to najliczniejsza grupa niegruźliczych prątków. Są izolowane z zanieczyszczonych zbiorników wodnych i gleby i mają niską patogeniczność dla ludzi i zwierząt.
M. scrofulaceum (od angielskiego scrofula - scrofula) jest jedną z głównych przyczyn zapalenia węzłów chłonnych szyjnych u dzieci poniżej 5 roku życia. W obecności poważnych chorób współistniejących mogą powodować uszkodzenia płuc, kości i tkanek miękkich. Oprócz wody i gleby, mikroby zostały wyizolowane z surowego mleka i innych produktów mlecznych.
M. maimoense to mikroaerofil tworzący szarobiałe, gładkie, błyszczące, nieprzezroczyste, kopulaste, okrągłe kolonie.
Pierwotne izolaty rosną bardzo powoli w temperaturze 22-37°C. Ekspozycja na światło nie powoduje produkcji pigmentu. W razie potrzeby ekspozycja może być kontynuowana do 12 tygodni. U ludzi powodują przewlekłą chorobę płuc.
M. gordonae to najczęściej rozpoznawane saprofity, scotochromogeny wody kranowej, które niezwykle rzadko powodują mykobakteriozę. Oprócz wody (znanej jako M. aquae) są one często izolowane z gleby, płukania żołądka, wydzielin oskrzelowych lub innych materiałów od pacjentów, ale w większości przypadków są niepatogenne dla ludzi. Jednocześnie istnieją doniesienia o przypadkach zapalenia opon mózgowych, zapalenia otrzewnej i zmian skórnych wywołanych przez ten typ mykobakterii.
Grupa 3 - wolno rosnące niechromogenne prątki (M. avium complex, M. gaslri, M. terrae complex itp.). Tworzą bezbarwne formy kolonii S lub SR i R, które mogą mieć jasnożółte i kremowe odcienie. Są izolowane od chorych zwierząt, wody i gleby.
M. avium - M. inlracellulare są połączone w jeden kompleks M. avium, ponieważ ich różnicowanie międzygatunkowe stwarza pewne trudności. Mikroorganizmy rosną w temperaturze 25-45 °C, są patogenne dla ptaków, mniej patogenne dla bydła, świń, owiec, psów i nie są patogenne dla świnek morskich. Najczęściej te mikroorganizmy powodują zmiany w płucach u ludzi. Opisano zmiany na skórze, tkance mięśniowej i układzie kostnym, a także rozsiane formy chorób. Należą do czynników sprawczych zakażeń oportunistycznych, które komplikują zespół nabytego niedoboru odporności (AIDS). Podgatunek paratuberculosis M. avium jest czynnikiem sprawczym choroby Jonesa u bydła i prawdopodobnie choroby Leśniowskiego-Crohna (przewlekłej choroby zapalnej przewodu pokarmowego) u ludzi. Mikroorganizm jest obecny w mięsie, mleku i kale zakażonych krów, a także występuje w wodzie i glebie. Standardowe metody oczyszczania wody nie dezaktywują tego drobnoustroju.
M. xenopi powoduje zmiany w płucach u ludzi i rozsiane formy choroby związane z AIDS. Są izolowane od żab z rodzaju Xenopus. Bakterie tworzą małe, gładkie, błyszczące, niepigmentowane kolonie, które następnie stają się jasnożółte. Termofile nie rosną w temperaturze 22 °C i dobrze rosną w temperaturze 37 i 45 °C. Po zbadaniu bakterioskopem wyglądają jak bardzo cienkie pręty, zwężające się na jednym końcu i ułożone równolegle do siebie (jak płot sztachetowy). Często są izolowane z zimnej i gorącej wody z kranu, w tym wody pitnej przechowywanej w zbiornikach szpitalnych (epidemie szpitalne). W przeciwieństwie do innych oportunistycznych mykobakterii są wrażliwe na większość leków przeciwgruźliczych.
M. ukerans jest czynnikiem etiologicznym mykobakteryjnej skórnej N (wrzód Buruli), rośnie tylko w temperaturze 30-33 °C, wzrost kolonii jest zauważalny dopiero po 7 tygodniach. Patogen jest również uwalniany, gdy myszy są zarażane w miazdze podeszwy łapy. Ta choroba jest powszechna w Australii i Afryce. Źródłem zakażenia jest środowisko tropikalne i szczepienie BCG przeciwko tej mykobakteriozie.
Grupa 4 - szybko rosnące mykobakterie (M. fortuitum complex, M. phlei, M. xmegmatis itp.). Ich wzrost obserwuje się w postaci kolonii w formie R lub S przez 1-2 do 7 dni. Występują w wodzie, glebie, ściekach i są przedstawicielami normalnej mikroflory organizmu człowieka. Bakterie z tej grupy rzadko są izolowane z materiału patologicznego od pacjentów, ale niektóre z nich mają znaczenie kliniczne.
Kompleks M. fortuitum obejmuje M. fortuitum i M. chcionae, które składają się z podgatunków. Powodują one procesy rozsiane, zakażenia skóry i pooperacyjne, choroby płuc. Drobnoustroje tego kompleksu są wysoce odporne na leki przeciwgruźlicze.
M. smegmatis jest przedstawicielem normalnej mikroflory, wyizolowanej ze smegmy u mężczyzn. Dobrze rośnie w temperaturze 45 °C. Jako czynnik wywołujący choroby u ludzi zajmuje drugie miejsce wśród szybko rosnących prątków po kompleksie M. fortuitum. Atakuje skórę i tkanki miękkie. Patogeny gruźlicy należy odróżnić od M. smegmatis podczas badania moczu.
Najczęściej mykobakteriozę wywołują przedstawiciele grup 3 i 1.
Epidemiologia mykobakteriozy
Czynniki wywołujące mykobakteriozę są szeroko rozpowszechnione w przyrodzie. Można je znaleźć w glebie, kurzu, torfie, błocie, wodzie rzecznej, stawach i basenach. Występują u kleszczy i ryb, wywołują choroby u ptaków, zwierząt dzikich i domowych, a także są przedstawicielami normalnej mikroflory błon śluzowych górnych dróg oddechowych i układu moczowo-płciowego u ludzi. Zakażenie prątkami niegruźliczymi następuje ze środowiska poprzez transmisję drogą powietrzną, kontakt z uszkodzeniem skóry, a także poprzez żywność i wodę. Przenoszenie mikroorganizmów z człowieka na człowieka jest rzadkie. Są to bakterie oportunistyczne, więc spadek odporności makroorganizmu i jego predyspozycje genetyczne mają duże znaczenie w rozwoju choroby. W dotkniętych obszarach tworzą się ziarniniaki. W cięższych przypadkach fagocytoza jest niekompletna, bakteriemia jest wyraźna, a w narządach wykrywa się makrofagi wypełnione niegruźliczymi prątkami i komórkami przypominającymi komórki trądu.
Objawy mykobakteriozy
Objawy mykobakteriozy są zróżnicowane. Najczęściej dotknięty jest układ oddechowy. Objawy patologii płuc są podobne do objawów gruźlicy. Jednak często zdarzają się przypadki pozapłucnej lokalizacji procesu obejmującej skórę i tkankę podskórną, powierzchnie ran, węzły chłonne, narządy moczowo-płciowe, kości i stawy, a także opony mózgowe. Zmiany narządowe mogą rozpocząć się zarówno ostro, jak i utajone, ale prawie zawsze postępują poważnie,
Możliwe jest również wystąpienie zakażenia mieszanego; w niektórych przypadkach może ono być przyczyną rozwoju wtórnego zakażenia endogennego.
Diagnostyka mikrobiologiczna mykobakteriozy
Główną metodą diagnozowania mykobakteriozy jest bakteriologia. Materiał do badania pobiera się na podstawie patogenezy i objawów klinicznych choroby. Początkowo ustala się, czy wyizolowana czysta kultura należy do czynników wywołujących gruźlicę, czy do prątków niegruźliczych. Następnie stosuje się zestaw badań w celu ustalenia rodzaju prątków, stopnia wirulencji i grupy Runyona. Pierwotna identyfikacja opiera się na takich cechach, jak szybkość wzrostu, zdolność do tworzenia pigmentu, morfologia kolonii i zdolność do wzrostu w różnych temperaturach. Aby zidentyfikować te cechy, nie jest wymagany żaden dodatkowy sprzęt ani odczynniki, więc można je stosować w podstawowych laboratoriach przychodni przeciwgruźliczych. Ostateczna identyfikacja (identyfikacja referencyjna) z wykorzystaniem złożonych badań biochemicznych przeprowadzana jest w specjalistycznych moratoriach instytucji naukowych. W większości przypadków preferuje się ich identyfikację za pomocą faktów biochemicznych, takich jak nowoczesne metody genetyki molekularnej, które są pracochłonne, mają wiele etapów przygotowawczych, wymagają specjalistycznego sprzętu i są drogie. Określenie wrażliwości na antybiotyki ma duże znaczenie dla leczenia. Kryterium równoczesnego pojawienia się danych klinicznych, radiologicznych, laboratoryjnych i wyizolowania czystej hodowli prątków niegruźliczych, przeprowadzenie wielu badań dynamiki ma decydujące znaczenie dla rozpoznania mykobakteriozy.
Pomocnicze znaczenie w diagnostyce ma oznaczanie antytez metodą RNGA, RP, immunoelektroforezy, RNIF i ELISA, a także wykonywanie skórnych testów alergicznych z sensytynami.
Leczenie i swoista profilaktyka mykobakteriozy
Wszystkie rodzaje prątków niegruźliczych, z wyjątkiem M. xenopi, są oporne na izoniazyd, streptomycynę i tiosemikarbazony. Leczenie mykobakteriozy lekami przeciwgruźliczymi i przeciwbakteryjnymi powinno być długotrwałe (12-13 miesięcy) i łączone. Zazwyczaj jest nieskuteczne w przypadku zakażeń MAC i chorób wywołanych przez szybko rosnące prątki. W niektórych przypadkach stosuje się leczenie chirurgiczne. Nie opracowano leków do swoistej profilaktyki mykobakteriozy.


 [
[