Ekspert medyczny artykułu
Nowe publikacje
Oskrzela oddechowe
Ostatnia recenzja: 04.07.2025

Cała zawartość iLive jest sprawdzana medycznie lub sprawdzana pod względem faktycznym, aby zapewnić jak największą dokładność faktyczną.
Mamy ścisłe wytyczne dotyczące pozyskiwania i tylko linki do renomowanych serwisów medialnych, akademickich instytucji badawczych i, o ile to możliwe, recenzowanych badań medycznych. Zauważ, że liczby w nawiasach ([1], [2] itd.) Są linkami do tych badań, które można kliknąć.
Jeśli uważasz, że któraś z naszych treści jest niedokładna, nieaktualna lub w inny sposób wątpliwa, wybierz ją i naciśnij Ctrl + Enter.
W miarę zmniejszania się średnicy oskrzeli ich ściany stają się cieńsze, wysokość i liczba rzędów komórek nabłonkowych maleją. Oskrzeliki niechrzęstne (lub błoniaste) mają średnicę 1-3 mm, w nabłonku nie ma komórek kubkowych, ich rolę pełnią komórki Clara, a warstwa podśluzówkowa bez wyraźnej granicy przechodzi w przydankę. Oskrzeliki błoniaste przechodzą w oskrzeliki końcowe o średnicy około 0,7 mm, ich nabłonek jest jednorzędowy. Od oskrzelików końcowych odchodzą oskrzeliki oddechowe o średnicy 0,6 mm. Oskrzeliki oddechowe są połączone z pęcherzykami płucnymi przez pory. Oskrzeliki końcowe przewodzą powietrze, oddechowe uczestniczą w przewodzeniu powietrza i wymianie gazowej.
Całkowita powierzchnia przekroju poprzecznego końcowych dróg oddechowych jest wielokrotnie większa niż powierzchnia przekroju poprzecznego tchawicy i dużych oskrzeli (53-186 cm2 w porównaniu z 7-14 cm2 ), ale oskrzeliki odpowiadają tylko za 20% oporu przepływu powietrza. Ze względu na niski opór końcowych dróg oddechowych wczesne uszkodzenie oskrzelików może być bezobjawowe, nie towarzyszyć mu mogą zmiany w testach czynnościowych i być przypadkowym znaleziskiem w tomografii komputerowej o wysokiej rozdzielczości.
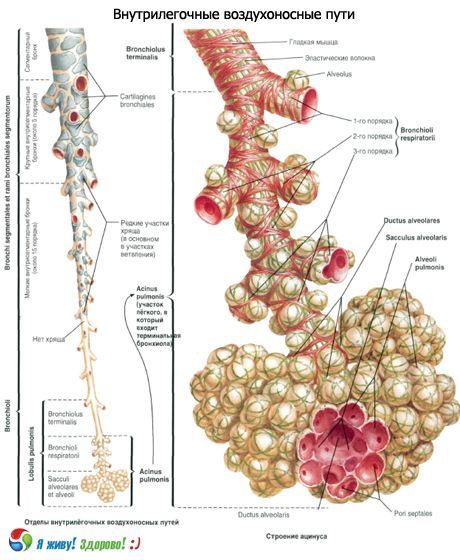
Według Międzynarodowej Klasyfikacji Histologicznej, zespół odgałęzień oskrzelika końcowego nazywany jest pierwotnym zrazikiem płucnym lub acinusem. Jest to najliczniejsza struktura płuc, w której zachodzi wymiana gazowa. Każde płuco ma 150 000 zrazików. Zrazik u osoby dorosłej ma średnicę 7-8 mm i ma jeden lub więcej oskrzelików oddechowych. Wtórny zrazik płucny jest najmniejszą jednostką płuca, ograniczoną przegrodami tkanki łącznej. Wtórne zraziki płucne składają się z 3 do 24 zrazików. Część centralna zawiera oskrzelik płucny i tętnicę. Nazywane są jądrem zrazikowym lub „strukturą środkowozrazikową”. Wtórne zraziki płucne są oddzielone przegrodami międzyzrazikowymi zawierającymi żyły i naczynia limfatyczne, gałęzie tętnicze i oskrzelikowe w jądrze zrazikowym. Wtórny zrazik płucny ma zwykle kształt wielokąta, a długość każdego ze składowych boków wynosi 1–2,5 cm.
Szkielet zrazika zbudowany jest z tkanki łącznej, która składa się z przegród międzyzrazikowych, śródmiąższu wewnątrzzrazikowego, środkowozrazikowego, okołooskrzelowo-naczyniowego i śródmiąższu podopłucnowego.
Oskrzelik końcowy jest podzielony na 14-16 oskrzelików oddechowych pierwszego rzędu, z których każdy jest z kolei dzielony dychotomicznie na oskrzeliki oddechowe drugiego rzędu, które z kolei są dzielony dychotomicznie na oskrzeliki oddechowe trzeciego rzędu. Każdy oskrzelik oddechowy trzeciego rzędu jest podzielony na przewody pęcherzykowe (o średnicy 100 μm). Każdy przewód pęcherzykowy kończy się dwoma woreczkami pęcherzykowymi.
Przejścia i woreczki pęcherzykowe mają w swoich ścianach wypukłości (pęcherzyki) - pęcherzyki. Na jeden kanał pęcherzykowy przypada około 20 pęcherzyków. Całkowita liczba pęcherzyków osiąga 600-700 milionów, a ich łączna powierzchnia wynosi około 40 m2 podczas wydechu i 120 m2 podczas wdechu.
W nabłonku oskrzelików oddechowych liczba komórek rzęskowych stopniowo maleje, a liczba nierzęskowych komórek sześciennych i komórek Clara wzrasta. Przewody pęcherzykowe są wyścielone nabłonkiem płaskim.
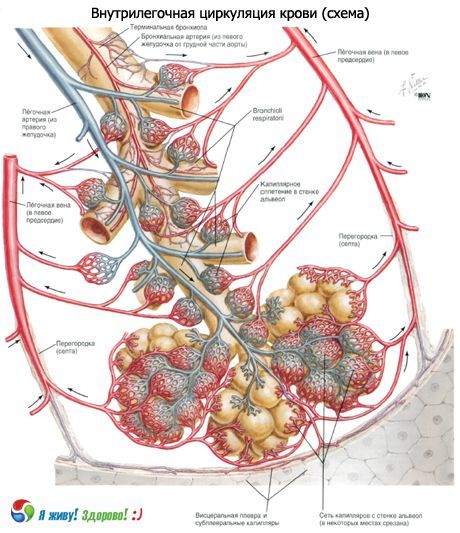
Badania mikroskopowe elektronowe wniosły znaczący wkład do współczesnego zrozumienia struktury pęcherzyków płucnych. Ściany są wspólne dla dwóch sąsiadujących pęcherzyków płucnych na dużym obszarze. Nabłonek pęcherzykowy pokrywa ścianę z obu stron. Pomiędzy dwiema warstwami wyściółki nabłonkowej znajduje się śródmiąższ, w którym wyróżnia się przestrzeń przegrodową i sieć naczyń włosowatych. Przestrzeń przegrodowa zawiera wiązki cienkich włókien kolagenowych, włókien siateczkowych i elastycznych, kilka fibroblastów i wolnych komórek (histocytów, limfocytów, leukocytów neutrofilowych). Zarówno nabłonek, jak i śródbłonek naczyń włosowatych leżą na błonie podstawnej o grubości 0,05-0,1 μm. W niektórych miejscach błony podnabłonkowa i podśródbłonkowa są rozdzielone przestrzenią przegrodową, w innych miejscach stykają się, tworząc pojedynczą błonę pęcherzykowo-włośniczkową. W ten sposób nabłonek pęcherzykowy, błona pęcherzykowo-włośniczkowa oraz warstwa komórek śródbłonka są składnikami bariery powietrze-krew, przez którą zachodzi wymiana gazowa.
Nabłonek pęcherzykowy jest heterogeniczny; wyróżnia się w nim trzy rodzaje komórek. Alweolocyty (pneumocyty) typu I pokrywają większość powierzchni pęcherzyków płucnych. Wymiana gazowa zachodzi przez nie.
Alweolocyty (pneumocyty) typu II, czyli duże alweolocyty, są okrągłe i wystają do światła pęcherzyków płucnych. Na ich powierzchni znajdują się mikrokosmki. Cytoplazma zawiera liczne mitochondria, dobrze rozwinięte ziarniste retikulum endoplazmatyczne i inne organelle, z których najbardziej charakterystyczne są otoczone błoną osmofilowe ciałka blaszkowate. Składają się one z gęstej elektronowo substancji warstwowej zawierającej fosfolipidy, a także składniki białkowe i węglowodanowe. Podobnie jak granulki wydzielnicze, ciałka blaszkowate są uwalniane z komórki, tworząc cienką (około 0,05 μm) warstwę surfaktantu, która zmniejsza napięcie powierzchniowe, zapobiegając zapadaniu się pęcherzyków płucnych.
Alweolocyty typu III, opisane pod nazwą komórek szczoteczkowych, wyróżniają się obecnością krótkich mikrokosmków na powierzchni wierzchołkowej, licznych pęcherzyków w cytoplazmie i wiązek mikrofibryli. Uważa się, że wykonują one absorpcję płynów i koncentrację surfaktantu lub chemorecepcję. Romanova LK (1984) zasugerowała ich funkcję neurosekrecyjną.
W świetle pęcherzyków płucnych zwykle znajduje się kilka makrofagów, które pochłaniają kurz i inne cząstki. Obecnie pochodzenie makrofagów pęcherzykowych z monocytów krwi i histiocytów tkankowych można uznać za ustalone.
Skurcz mięśni gładkich prowadzi do zmniejszenia podstawy pęcherzyków płucnych, zmiany konfiguracji pęcherzyków – wydłużają się. To właśnie te zmiany, a nie pęknięcia przegród, leżą u podłoża obrzęku i rozedmy płuc.
Konfiguracja pęcherzyków płucnych jest determinowana przez elastyczność ich ścian, rozciąganych przez wzrost objętości klatki piersiowej i przez aktywne skurcze mięśni gładkich oskrzelików. Dlatego przy tej samej objętości oddechowej możliwe jest różne rozciąganie pęcherzyków płucnych w różnych segmentach. Trzecim czynnikiem determinującym konfigurację i stabilność pęcherzyków płucnych jest siła napięcia powierzchniowego powstająca na granicy dwóch środowisk: powietrza wypełniającego pęcherzyk płucny i filmu ciekłego wyściełającego jego wewnętrzną powierzchnię i chroniącego nabłonek przed wysychaniem.
Aby przeciwdziałać sile napięcia powierzchniowego (T), która ma tendencję do ściskania pęcherzyków płucnych, konieczne jest pewne ciśnienie (P). Wartość P jest odwrotnie proporcjonalna do promienia krzywizny powierzchni, co wynika z równania Laplace'a: P = T / R. Wynika z tego, że im mniejszy promień krzywizny powierzchni, tym wyższe ciśnienie jest niezbędne do utrzymania danej objętości pęcherzyków płucnych (przy stałym T). Jednak obliczenia wykazały, że powinno ono być wielokrotnie większe od ciśnienia wewnątrzpęcherzykowego występującego w rzeczywistości. Podczas wydechu na przykład pęcherzyki płucne powinny się zapadać, co się nie dzieje, ponieważ stabilność pęcherzyków płucnych przy małych objętościach zapewnia substancja powierzchniowo czynna - surfaktant, który zmniejsza napięcie powierzchniowe filmu, gdy powierzchnia pęcherzyków płucnych się zmniejsza. Jest to tzw. czynnik przeciwatelektatyczny, odkryty w 1955 roku przez Pattle'a i składający się z kompleksu substancji o charakterze białkowo-węglowodanowo-lipidowym, w skład którego wchodzi dużo lecytyny i innych fosfolipidów. Surfaktant wytwarzany jest w odcinku oddechowym przez komórki pęcherzykowe, które wraz z komórkami nabłonka powierzchniowego wyściełają pęcherzyki od wewnątrz. Komórki pęcherzykowe są bogate w organelle, ich protoplazma zawiera duże mitochondria, dlatego wyróżniają się wysoką aktywnością enzymów oksydacyjnych, zawierają również niespecyficzną esterazę, fosfatazę alkaliczną, lipazę. Największe zainteresowanie budzą stale znajdowane w tych komórkach inkluzje, oznaczane mikroskopem elektronowym. Są to osmiofilne ciała o owalnym kształcie, o średnicy 2-10 μm, o warstwowej strukturze, ograniczone pojedynczą błoną.
Układ powierzchniowo czynny płuc
Układ surfaktantowy płuc pełni kilka ważnych funkcji. Substancje powierzchniowo czynne płuc zmniejszają napięcie powierzchniowe i pracę wymaganą do wentylacji płuc, stabilizują pęcherzyki płucne i zapobiegają ich atelaktyzie. W tym przypadku napięcie powierzchniowe wzrasta podczas wdechu i maleje podczas wydechu, osiągając wartość bliską zeru pod koniec wydechu. Surfaktant stabilizuje pęcherzyki płucne poprzez natychmiastowe zmniejszenie napięcia powierzchniowego, gdy objętość pęcherzyków zmniejsza się, i zwiększenie napięcia powierzchniowego, gdy objętość pęcherzyków zwiększa się podczas wdechu.
Surfaktant stwarza również warunki do istnienia pęcherzyków płucnych o różnych rozmiarach. Gdyby nie było surfaktantu, małe pęcherzyki zapadałyby się i przepuszczały powietrze do większych. Powierzchnia najmniejszych dróg oddechowych jest również pokryta surfaktantem, co zapewnia ich drożność.
Dla funkcjonowania dystalnej części płuca najważniejsza jest drożność połączenia oskrzelowo-pęcherzykowego, gdzie znajdują się naczynia limfatyczne i skupiska limfoidalne oraz gdzie rozpoczynają się oskrzeliki oddechowe. Surfaktant pokrywający powierzchnię oskrzelików oddechowych pochodzi tutaj z pęcherzyków płucnych lub powstaje lokalnie. Zastąpienie surfaktantu w oskrzelikach wydzieliną komórek kubkowych prowadzi do zwężenia małych dróg oddechowych, zwiększenia ich oporu, a nawet całkowitego zamknięcia.
Oczyszczanie zawartości najmniejszych dróg oddechowych, gdzie transport zawartości nie jest związany z aparatem rzęskowym, jest w dużej mierze zapewnione przez surfaktant. W strefie funkcjonowania nabłonka rzęskowego występują gęste (żelowe) i płynne (solowe) warstwy wydzieliny oskrzelowej dzięki obecności surfaktantu.
Układ surfaktantowy płuc bierze udział w absorpcji tlenu i regulacji jego transportu przez barierę powietrze-krew, a także w utrzymaniu optymalnego poziomu ciśnienia filtracji w układzie mikrokrążenia płucnego.
Zniszczenie filmu surfaktantowego przez Tween powoduje atelektazę. Wdychanie aerozoli związków lecytyny daje natomiast dobry efekt terapeutyczny, np. w przypadku niewydolności oddechowej u noworodków, u których film może zostać zniszczony przez kwasy żółciowe podczas aspiracji płynu owodniowego.
Hipowentylacja płuc prowadzi do zaniku filmu surfaktantowego, a przywrócenie wentylacji w zapadniętym płucu nie wiąże się z całkowitym przywróceniem filmu surfaktantowego we wszystkich pęcherzykach płucnych.
Właściwości powierzchniowo czynne surfaktantu zmieniają się również w przewlekłej hipoksji. W nadciśnieniu płucnym obserwuje się zmniejszenie ilości surfaktantu. Jak wykazały badania eksperymentalne, upośledzona drożność oskrzeli, zastój żylny w krążeniu płucnym i zmniejszenie powierzchni oddechowej płuc przyczyniają się do zmniejszenia aktywności układu surfaktantu w płucach.
Wzrost stężenia tlenu we wdychanym powietrzu prowadzi do pojawienia się w świetle pęcherzyków płucnych dużej liczby formacji błonowych dojrzałego surfaktantu i ciał osmofilowych, co wskazuje na zniszczenie surfaktantu na powierzchni pęcherzyków płucnych. Dym tytoniowy ma negatywny wpływ na układ surfaktantu płuc. Spadek aktywności powierzchniowej surfaktantu jest spowodowany przez kwarc, pył azbestowy i inne szkodliwe zanieczyszczenia w wdychanym powietrzu.
Według wielu autorów surfaktant zapobiega również przesiękom i obrzękom oraz działa bakteriobójczo.
Proces zapalny w płucach prowadzi do zmian właściwości powierzchniowo czynnych surfaktantu, a stopień tych zmian zależy od aktywności stanu zapalnego. Jeszcze silniejszy negatywny wpływ na układ surfaktantu płuc mają nowotwory złośliwe. U nich właściwości powierzchniowo czynne surfaktantu znacznie częściej się zmniejszają, zwłaszcza w strefie atelektazy.
Istnieją wiarygodne dane na temat zaburzeń aktywności powierzchniowej surfaktantu podczas długotrwałego (4-6 godzin) znieczulenia fluorotanem. Operacje z użyciem aparatów do sztucznego krążenia krwi często wiążą się ze znacznymi zaburzeniami w układzie surfaktantu płuc. Znane są również wrodzone wady układu surfaktantu płuc.
Surfaktant można wykryć morfologicznie za pomocą mikroskopii fluorescencyjnej ze względu na pierwotną fluorescencję w postaci bardzo cienkiej warstwy (0,1 do 1 µm) wyściełającej pęcherzyki płucne. Nie jest on widoczny w mikroskopie optycznym i ulega zniszczeniu, gdy preparaty są traktowane alkoholem.
Istnieje pogląd, że wszystkie przewlekłe choroby układu oddechowego wiążą się z jakościowym lub ilościowym niedoborem układu powierzchniowo czynnego narządów oddechowych.


 [
[