Ekspert medyczny artykułu
Nowe publikacje
Amyloidoza wątroby
Ostatnia recenzja: 29.06.2025

Cała zawartość iLive jest sprawdzana medycznie lub sprawdzana pod względem faktycznym, aby zapewnić jak największą dokładność faktyczną.
Mamy ścisłe wytyczne dotyczące pozyskiwania i tylko linki do renomowanych serwisów medialnych, akademickich instytucji badawczych i, o ile to możliwe, recenzowanych badań medycznych. Zauważ, że liczby w nawiasach ([1], [2] itd.) Są linkami do tych badań, które można kliknąć.
Jeśli uważasz, że któraś z naszych treści jest niedokładna, nieaktualna lub w inny sposób wątpliwa, wybierz ją i naciśnij Ctrl + Enter.
Amyloidoza jest zazwyczaj układową, ogólną patologią charakteryzującą się gromadzeniem się amyloidu (specyficznego glikoproteiny) w tkankach i późniejszym zaburzeniem prawidłowej funkcji narządów. Amyloidoza wątroby jest znacznie rzadsza niż nerek i śledziony [ 1 ], ale prawie zawsze towarzyszy układowemu uszkodzeniu organizmu. Żadna z istniejących technik obrazowania nie jest w stanie konkretnie wykazać obecności amyloidu. Nawet w przypadku podejrzenia klinicznego i radiologicznego, rozpoznanie amyloidozy zależy od biopsji tkanki w celu potwierdzenia obecności złogów amyloidu. [ 3 ] Leczenie jest złożone, kompleksowe i obejmuje środki immunosupresyjne i objawowe. W ciężkich przypadkach może być wymagany przeszczep wątroby.
Epidemiologia
Sukces leczenia zależy bezpośrednio od terminowego rozpoznania choroby, która powoduje powstawanie kompleksu białkowo-polisacharydowego (amyloidu) w różnych narządach i wątrobie. Jak pokazuje praktyka, amyloidozę trudno założyć lub podejrzewać, chociaż można ją zidentyfikować i potwierdzić. Faktem jest, że w ponad 80% nierozpoznanych przypadków choroba jest klinicznie maskowana przez patologię wątroby. Najskuteczniejszą metodą diagnostyczną jest biopsja.
Amyloidoza wątroby jest rzadszym problemem w porównaniu do amyloidozy nerek. Jednocześnie wszystkim przypadkom zmian wątrobowych towarzyszą zmiany innych narządów. Najczęściej patologia dotyczy głównie strukturalnych części triady wątrobowej, co determinuje minimalną i niespecyficzną symptomatologię. Obraz kliniczny i morfologiczny niedoboru hepatocytów i nadciśnienia wrotnego objawia się rozlanym i wewnątrzzrazikowym typem patologii.
Biopsja wątroby jest uzasadniona w przypadku hepatomegalii bez wcześniejszych objawów ze strony wątroby i przy braku zespołu nerczycowego.
Rozlane zajęcie wątroby obserwuje się u około 25% pacjentów, przy czym u 75% pacjentów zajęte są jedynie drogi wrotne.
Pierwotna amyloidoza atakuje wątrobę w 90% przypadków, podczas gdy wtórna amyloidoza atakuje wątrobę jedynie w 47% przypadków.
Wyizolowane zajęcie wątroby jest niezwykle rzadkie. Nerki (około 93% przypadków), śledziona (72%), serce (57%), trzustka (36%), nadnercza (29%), jelita i płuca (po 21%) są zwykle dotknięte synchronicznie.
Kobiety zapadają na tę chorobę prawie dwa razy częściej niż mężczyźni. Średnia długość życia pacjentów z amyloidozą wynosi 52-64 lata.
Przyczyny amyloidoza wątrobowa
Amyloidoza przebiega wraz z powstawaniem i gromadzeniem się w tkance wątroby kompleksu polisacharydowo-białkowego – amyloidu. Problem występowania pierwotnej zmiany chorobowej jest do tej pory niedostatecznie zbadany. Jeśli chodzi o patologię wtórną, jej pojawienie się jest zwykle związane z takimi chorobami:
- Przewlekłe procesy zakaźne (gruźlica, kiła, promienica);
- Procesy zapalne o charakterze ropnym (bakteryjne zapalenie wsierdzia, zapalenie kości i szpiku, rozstrzenie oskrzeli itp.);
- Choroby złośliwe (białaczka, rak narządów wewnętrznych, limfogranulomatoza).
Reaktywna forma amyloidozy występuje u pacjentów z towarzyszącą miażdżycą, chorobami reumatologicznymi (choroba Bechterewa, reumatoidalne zapalenie stawów), łuszczycą, przewlekłymi procesami zapalnymi i wielonarządowymi (w tym sarkoidozą). Główne czynniki ryzyka: predyspozycje dziedziczne, zaburzenia odporności komórkowej, hiperglobulinemia.
Patogeneza
Istnieje szereg założeń dotyczących pochodzenia amyloidozy wątroby. Większość specjalistów opowiada się za wersją dysproteinozy, immunologiczną i mutacyjną naturą choroby, a także lokalną genezą komórkową. Wersja genezy komórkowej obejmuje zmiany w reakcjach działających na poziomie komórkowym (tworzenie fibrylarnych prekursorów amyloidu przez kompleks makrofagów), chociaż amyloid powstaje i gromadzi się poza strukturami komórkowymi.
Wersja dysproteinozy opiera się na fakcie, że amyloid jest produktem nieprawidłowego metabolizmu białek. Podstawowym ogniwem patogenetycznym problemu jest dysproteinemia i hiperfibrynogenemia, które prowadzą do gromadzenia się grubych rozproszonych frakcji białkowych i paraproteinowych w osoczu.
Według wersji immunologicznej, powstawanie amyloidu jest spowodowane reakcją antygen-przeciwciało, w której produkty rozpadu tkanek lub obce białka działają jako antygeny. Gromadzenie się amyloidu występuje głównie w obszarze powstawania przeciwciał i nadmiernej obecności antygenów.
Za najbardziej prawdopodobną wersję naukowcy uważają teorię mutacji, która bierze pod uwagę różnorodne czynniki mutagenne mogące prowadzić do nieprawidłowości w syntezie białek.
Amyloid jest złożonym hipoproteinem, który składa się z białek globularnych i fibrylarnych połączonych z polisacharydami. Nagromadzenia amyloidu wpływają na błonę wewnętrzną i przydankę sieci naczyniowej, podścielisko narządów miąższowych, strukturę gruczołów itp. Nagromadzenia amyloidu nie powodują uszkodzeń czynnościowych. Małe nagromadzenia nie powodują zaburzeń czynnościowych, ale przy intensywnej obecności amyloidu wątroba zwiększa objętość, zmienia wygląd narządu, rozwija się brak funkcji.
Amyloidoza wątroby charakteryzuje się odkładaniem się włókienek amyloidu w przestrzeni Dyssego, która zwykle zaczyna się w okolicy okołowrotnej, chociaż czasami jest środkowo-zrazikowa i może również odkładać się w naczyniach krwionośnych wątroby. [ 4 ], [ 5 ] W ciężkich przypadkach odkładanie się amyloidu prowadzi do zaniku ciśnieniowego hepatocytów, co uniemożliwia przepływ żółci, powodując cholestazę lub może blokować zatoki, powodując nadciśnienie wrotne. [ 6 ], [ 7 ], [ 8 ]
Objawy amyloidoza wątrobowa
Obraz kliniczny amyloidozy wątroby jest różnorodny i zależy od intensywności gromadzenia się amyloidu, jego cech biochemicznych, czasu trwania procesu chorobowego, stopnia uszkodzenia narządów i zaburzenia ich stanu czynnościowego.
W stadium utajonym amyloidozy, gdy nagromadzenia amyloidu w wątrobie można wykryć jedynie badaniem mikroskopowym, pierwszych objawów choroby nie ma. Wraz z dalszym rozwojem i narastającym deficytem czynnościowym narządu symptomatologia postępuje.
Wątroba stopniowo się pogrubia, powiększa. Metodą palpacji można wyczuć zmienione, ale gładkie i bezbolesne granice narządu. Rzadko patologii towarzyszy ból w okolicy podżebrowej po prawej stronie, niestrawność, powiększenie śledziony, zażółcenie skóry, błon śluzowych i twardówek, zespół krwotoczny.
Najbardziej charakterystyczne objawy amyloidozy wątroby: [ 9 ], [ 10 ]
- Gromadzenie się amyloidu w wątrobie powoduje hepatomegalię u 33–92% pacjentów;
- Łagodna żółtaczka
- nadciśnienie wrotne;
- Cholestaza umiarkowana do ciężkiej.
Ponieważ amyloidoza bardzo rzadko atakuje tylko jeden narząd, zwykle występują dodatkowe objawy:
- W przypadku uszkodzenia nerek rozwija się zespół nerczycowy i nadciśnienie tętnicze z dalszą niewydolnością nerek, obrzękiem, czasami zakrzepicą żył nerkowych, leukocyturią, krwiomoczem, hipoproteinemią, azotemią itd.;
- W przypadku zaatakowania serca rozwija się stan podobny do kardiomiopatii restrykcyjnej (zaburzenia rytmu serca, kardiomegalia, narastająca niewydolność serca, osłabienie i duszność, obrzęki, rzadziej - gromadzenie się płynu w jamie brzusznej i opłucnej, zapalenie osierdzia);
- Jeśli przewód pokarmowy jest dotknięty chorobą, mogą wystąpić: powiększenie języka, osłabienie i zaburzenia perystaltyki przełyku, nudności i zgaga, zaparcia lub biegunka itp.;
- W przypadku zajęcia trzustki występują objawy przewlekłego zapalenia trzustki;
- Jeśli zaangażowany jest mechanizm mięśniowo-szkieletowy, rozwija się symetryczne zapalenie wielostawowe, zespół cieśni nadgarstka, miopatie, a jeśli zajęty jest układ nerwowy – polineuropatie, paraliż, ortostatyczne niedociśnienie tętnicze, wzmożone pocenie, demencja.
Jeśli reakcja patologiczna rozprzestrzeni się na skórę, na twarzy, szyi, fałdach skórnych pojawiają się liczne woskowe blaszki. Możliwy jest obraz neurodermitu, czerwonej gorączki płaskonabłonkowej, twardziny.
Współwystępowanie wielu zmian amyloidowych i różnorodność objawów sprawiają, że rozpoznanie amyloidozy wątrobowej jest znacznie trudniejsze i wymaga kompleksowej i pełnej diagnozy.
Formularze
Według klasyfikacji WHO wyróżnia się pięć typów amyloidozy:
- AL (podstawowy);
- AA (średnie);
- ATTR (dziedziczna i starcza układowa);
- Aβ2M (u pacjentów dializowanych);
- AIAPP (u pacjentów z cukrzycą insulinoniezależną);
- AB (na chorobę Alzheimera);
- AANF (amyloidoza przedsionkowa starcza).
Występuje miejscowa amyloidoza wątroby, jednak częściej jest to zmiana ogólnoustrojowa, w której proces patologiczny obejmuje także nerki, serce, śledzionę, układ nerwowy, a także inne narządy i tkanki.
Komplikacje i konsekwencje
Amyloidoza układowa stopniowo prowadzi do rozwoju ostrych procesów patologicznych, które z kolei mogą prowadzić do śmierci. Do najczęstszych i zagrażających życiu powikłań należą:
- Częste patologie zakaźne (bakteryjne, wirusowe), w tym zapalenie płuc, odmiedniczkowe zapalenie nerek, kłębuszkowe zapalenie nerek;
- Przewlekła niewydolność wątroby i nerek;
- Przewlekła niewydolność serca (może poprzedzać zawał mięśnia sercowego);
- Udar krwotoczny.
Zakrzepica żylna powstaje w wyniku gromadzenia się i odkładania białek na ścianach żył. Światło dotkniętych naczyń zwęża się, rozwija się niewydolność narządów. Z czasem, na tle długotrwałej hiperproteinemii, naczynie może całkowicie się zamknąć. Każde z powikłań może prowadzić do niekorzystnego wyniku - zgonu.
Diagnostyka amyloidoza wątrobowa
W przypadku podejrzenia amyloidozy wątroby, po obowiązkowych konsultacjach, zarówno gastroenterologa i terapeuty, jak i reumatologa, kardiologa, dermatologa, neurologa, urologa, przeprowadza się działania diagnostyczne. Ważne jest, aby kompleksowo ocenić dane wywiadu i objawy kliniczne, przeprowadzić kompleksową diagnostykę laboratoryjną i instrumentalną.
Badania koniecznie obejmują badanie moczu i krwi. W amyloidozie wątrobowej często stwierdza się połączenie leukocyturii z białkomoczem i cylindrurią, a także hipoproteinemię - z hiperlipidemią, anemią, hiponatremią i hipokalcemią, zmniejszoną liczbą płytek krwi. Paraproteiny wykrywa się w elektroforezie moczu i surowicy.
Diagnostyka instrumentalna obejmuje:
- EKG, echokardiografia;
- USG jamy brzusznej;
- Zdjęcia rentgenowskie żołądka, przełyku;
- Irygografia, prześwietlenie barem;
- Endoskopia.
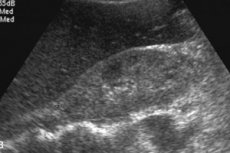
Radiologiczne wyniki amyloidozy wątroby obejmują niespecyficzną hepatomegalię, zwiększoną echogeniczność w badaniu ultrasonograficznym lub gęstość w tomografii komputerowej (TK) i zwiększoną intensywność sygnału T1 w obrazowaniu metodą rezonansu magnetycznego (MRI). [ 12 ] Scyntygrafia ze wskaźnikami związanymi z Tc-99m wykazuje niejednorodny wychwyt, ale jest on niespecyficzny. [ 13 ], [ 14 ] Wykazano, że GC zwiększa sztywność wątroby mierzoną elastografią; [ 15 ], [ 16 ], [ 17 ], ale istnieje niewiele opisów przypadków. Elastografia rezonansu magnetycznego (MRE) jest obecnie najdokładniejszą nieinwazyjną metodą wykrywania i określania stadium włóknienia wątroby, [ 18 ], [ 19 ] MRE jest przydatna do wykrywania progresji, odpowiedzi na leczenie i przewidywania dekompensacji wątroby u pacjentów z włóknieniem wątroby. [ 20 ]
Amyloidoza wątroby jest trudna do określenia na USG: stwierdza się powiększenie narządu, przy czym najbardziej charakterystyczna jest hepatomegalia przekraczająca 15 cm. Pod kontrolą USG wykonuje się biopsję, która staje się decydującym wskaźnikiem diagnostycznym. Za pomocą specjalnej igły pobiera się niewielką ilość tkanki wątroby, a następnie barwi się ją specjalnym barwnikiem i bada pod mikroskopem, co pozwala na bezpośrednie dostrzeżenie złogów amyloidu.
Ostateczną diagnozę stawia się dopiero po wykryciu włókienek amyloidowych w tkance wątroby i innych narządów. Genetycznie uwarunkowany typ amyloidozy ustala się poprzez dokładne badanie genetyczno-medyczne rodowodu.
Diagnostyka różnicowa
Amyloidozę należy podejrzewać u wszystkich pacjentów z połączeniem białkomoczu nerkowego, kardiomiopatii restrykcyjnej, neuropatii autonomicznej lub obwodowej i hepatomielii, nawet w przypadku braku monoklonalnego paraproteiny. Weryfikacja rodzaju amyloidozy jest bardzo ważna, ponieważ leczenie zmian o różnej etiologii jest bardzo różne.
Diagnostyka histologiczna obejmuje barwienie czerwienią Kongo, a następnie badanie mikroskopowe w świetle spolaryzowanym. Zaleca się biopsję kilku próbek tkanek na raz. Jeśli wynik barwienia okaże się pozytywny, przeprowadza się analizę immunohistochemiczną przy użyciu przeciwciał monoklonalnych do białek prekursorowych w celu zidentyfikowania rodzaju amyloidu.
Analiza DNA jest przeprowadzana w celu rozróżnienia między pierwotną amyloidozą a różnymi odmianami genetycznie uwarunkowanej amyloidozy. Włókna amyloidu można wyizolować z próbek biopsji i sekwestrować do pojedynczych aminokwasów.
Dodatkowe badania mające na celu określenie dyskrazji komórek plazmatycznych:
- Elektroforeza białek surowicy krwi i moczu;
- Badanie immunologiczne na obecność wolnych łańcuchów lekkich;
- Immunofiksacja (immunoblotting) białek surowicy;
- Aspiracyjna biopsja szpiku kostnego i trepanobiopsja.
Diagnostyka amyloidozy wątroby to długotrwały i pracochłonny proces, wymagający zwiększonej uwagi specjalistów oraz dobrego wyposażenia klinik i laboratoriów.
Z kim się skontaktować?
Leczenie amyloidoza wątrobowa
Działania lecznicze mają na celu obniżenie stężenia istniejących białek amyloidowych we krwi (eliminacja przyczyny amyloidozy) i wspomaganie prawidłowej funkcji wątroby.
Wtórna amyloidoza wymaga zablokowania procesu zapalnego (w przewlekłych patologiach zakaźnych i autoimmunologicznych). W chorobach autoimmunologicznych zaleca się stosowanie cytostatyków. Aby wyeliminować przewlekłe procesy zakaźne, obszar zapalenia jest często usuwany chirurgicznie. Często takie podejście może zatrzymać dalszy postęp amyloidozy i poprawić funkcję wątroby.
Pierwotna amyloidoza wymaga zastosowania leków chemioprewencyjnych, a czasami przeszczepu szpiku kostnego.
Aktualne wytyczne zalecają skojarzenie cyklofosfamidu, bortezomibu, deksametazonu (CyBorD) i daratumumabu jako terapię pierwszego rzutu u pacjentów ze świeżo rozpoznaną AL.
Bortezomib jest inhibitorem proteasomu. Proteasomy biorą udział w zmniejszaniu proteotoksyczności i regulowaniu białek, które kontrolują progresję komórkową i apoptozę. Komórki plazmatyczne, które generują amyloid, są szczególnie wrażliwe na hamowanie proteasomu, ponieważ polegają na proteasomie w celu zmniejszenia toksycznych efektów łańcuchów lekkich i zapobiegania apoptozie.
Daratumumumab to przeciwciało monoklonalne (mAb), które wiąże się z CD38, glikoproteiną transbłonową ekspresowaną na powierzchni komórek plazmatycznych, indukując apoptozę. Jest to jedyny lek specjalnie zatwierdzony do leczenia amyloidozy AL w przypadku stosowania z CyBorD. Skuteczność CyBorD-daratumumab jest bardzo wysoka, a 78% pacjentów osiągnęło znaczącą odpowiedź hematologiczną (zdefiniowaną jako odpowiedź całkowita lub bardzo dobra odpowiedź częściowa). Mediana przeżycia w małej grupie pacjentów otrzymujących CyBorD (n = 15) wyniosła 655 dni w porównaniu do 178 dni u pacjentów otrzymujących inne leczenie na bazie melfalanu i deksametazonu (n = 10). 4
Terapie te mają jednak liczne skutki uboczne, w tym kardiotoksyczność, która zmusza do zmniejszenia dawki lub przerwania leczenia i zastosowania mniej skutecznych, ale lepiej tolerowanych strategii terapeutycznych.
Isatuximab, monoklonalne przeciwciało skierowane przeciwko CD38, podobne do daratumumabu, jest badane w leczeniu dyskrazji komórek plazmatycznych będącej przyczyną AL.
Obecnie badane są trzy przeciwciała monoklonalne: birtamimab, CAEL-101 i AT-03, które mają na celu usuwanie włókienek amyloidu z chorych narządów. Wyniki tych badań będą mogły dostarczyć bezpośrednich dowodów na hipotezę, że usunięcie włókienek złogów łańcucha lekkiego z narządów powoduje poprawę funkcji narządów. [ 21 ]
W celu wsparcia funkcji wątroby przepisuje się leki na bazie kwasu urso-deoksycholowego (np. Ursosan). Kwas urso-deoksycholowy pomaga stabilizować błony komórkowe, zmniejsza niekorzystny wpływ toksycznych kwasów tłuszczowych w zastoju żółci wywołanym przez złogi amyloidu i pomaga przywrócić prawidłowy odpływ żółci.
Ponadto leczenie objawowe i wspomaganie funkcjonowania innych ważnych struktur, takich jak układ nerwowy, serce, nerki itp. Terapia wspomagająca u pacjentów z amyloidozą wątrobową obejmuje różne aspekty kliniczne, w tym leczenie niewydolności serca, arytmii, zaburzeń przewodzenia, choroby zakrzepowo-zatorowej i współistniejącego zwężenia aorty.
Inne metody leczenia zależą od rodzaju amyloidozy i tego, które części ciała są dotknięte chorobą. Metody leczenia mogą obejmować: [ 22 ]
- Leki łagodzące objawy, takie jak leki przeciwbólowe, leki przeciw nudnościom lub leki zmniejszające obrzęk (diuretyki);
- Leki redukujące amyloid;
- Dializa nerek;
- Przeszczep wątroby.
Wątroba produkuje 95% TTR (transtyretyny, białka zaangażowanego w transport tyroksyny (T4) i białka wiążącego retinol. Transtyretyna jest syntetyzowana głównie w wątrobie i jest bogata w pasma beta, które mają tendencję do agregacji w nierozpuszczalne fibryle amyloidu) mierzone w surowicy. Dlatego przeszczep wątroby był historycznie (od 1990 r.) sugerowany jako terapia pierwszego rzutu w celu wyeliminowania głównego źródła amyloidogennego TTR u pacjentów z postacią rodzinną (ATTRv), podczas gdy nie jest wskazany w postaci ATTR-wt. Przeszczep wątroby u młodych pacjentów we wczesnych stadiach choroby wiąże się z wysokim 20-letnim wskaźnikiem przeżycia. Przeszczep wątroby wydaje się być skuteczniejszy w przypadku niektórych mutacji i mniej skuteczny w przypadku innych, takich jak V122I (związany z kardiomiopatią). U młodych pacjentów z chorobą ATTRv i kardiomiopatią możliwy jest również łączony przeszczep wątroby i serca, a dane z literatury naukowej dotyczące niewielkiej grupy pacjentów wskazują, że takie skojarzenie daje lepsze rokowanie niż przeszczep samego serca.
U pacjentów z amyloidozą wątrobową przeciwwskazane jest przyjmowanie glikozydów nasercowych i antagonistów wapnia, takich jak diltiazem lub werapamil, które mogą gromadzić się w amyloidzie. Inhibitory ACE i beta-adrenoblokery są stosowane ostrożnie.
W przypadku niedociśnienia ortostatycznego przepisuje się mineralokortykosteroidy lub glikokortykosteroidy, biorąc pod uwagę, że mogą one powodować dekompensację niewydolności serca. Ostrożnie stosuje się również alfa-adrenomimetyk midodrynę (Gutron).
W przypadku neuropatii wskazane jest stosowanie leków przeciwdrgawkowych i przeciwdepresyjnych.
W niektórych przypadkach amyloidozy wątroby lekarze muszą rozważyć przeszczep narządu.
Zapobieganie
Z powodu braku informacji o patogenezie amyloidozy wątroby specjaliści nie mogą opracować konkretnej profilaktyki choroby. Dlatego główne wysiłki sprowadzają się do terminowego wykrywania i leczenia wszelkich przewlekłych patologii, które mogą wywołać rozwój zaburzenia. Jeśli w rodzinie występują przypadki amyloidozy o dowolnej lokalizacji, zaleca się systematyczne zgłaszanie się do lekarzy na badania ambulatoryjne.
Ogólnie rzecz biorąc, działania profilaktyczne sprowadzają się do terminowego eliminowania chorób zakaźnych, zwłaszcza tych, które mają tendencję do przekształcania się w proces przewlekły. Chodzi o zapobieganie rozwojowi gruźlicy, infekcji płucnych itp. Ważne jest terminowe wykrywanie i odpowiednie leczenie zakażeń paciorkowcowych, które mogą stać się przyczyną przewlekłych form autoimmunologicznych procesów zapalnych. Mowa tu o szkarlatynie, paciorkowcowym zapaleniu migdałków itp.
Jeśli u pacjenta występuje już choroba autoimmunologiczna, należy systematycznie konsultować się z lekarzem, obserwować aktywność patologii, stosować niezbędne leki zgodnie z zaleceniami lekarza, dostosowywać dawkowanie zgodnie ze wskazaniami.
Prognoza
Rokowanie dla pacjentów z amyloidozą wątrobową jest niekorzystne. Choroba rozwija się powoli, ale stale, co ostatecznie powoduje dysfunkcję dotkniętych narządów i zgon - w szczególności z powodu niewydolności narządów.
Pacjenci z patologią układową umierają głównie w wyniku rozwoju przewlekłej niewydolności nerek, chociaż w niektórych przypadkach hemodializa lub ciągła ambulatoryjna dializa otrzewnowa poprawia rokowanie takich pacjentów. Wskaźnik przeżycia pacjentów poddawanych hemodializie, niezależnie od jej rodzaju, można porównać z osobami z innymi patologiami układowymi i cukrzycą.
Najczęstszą przyczyną zgonów podczas hemodializy są powikłania ze strony układu sercowo-naczyniowego.
Transplantacja wątroby od dawna jest uważana za jedną z głównych metod leczenia tej choroby, a najbardziej optymistyczne wskaźniki przeżywalności obserwuje się u pacjentów, których wiek nie przekracza 50 lat (pod warunkiem, że proces patologiczny jest krótkotrwały, a wskaźnik masy ciała jest prawidłowy). Nieco gorsze rokowanie mają pacjenci z amyloidozą wątroby połączoną z neuropatią obwodową.

