Ekspert medyczny artykułu
Nowe publikacje
Arachnodaktylia
Ostatnia recenzja: 04.07.2025

Cała zawartość iLive jest sprawdzana medycznie lub sprawdzana pod względem faktycznym, aby zapewnić jak największą dokładność faktyczną.
Mamy ścisłe wytyczne dotyczące pozyskiwania i tylko linki do renomowanych serwisów medialnych, akademickich instytucji badawczych i, o ile to możliwe, recenzowanych badań medycznych. Zauważ, że liczby w nawiasach ([1], [2] itd.) Są linkami do tych badań, które można kliknąć.
Jeśli uważasz, że któraś z naszych treści jest niedokładna, nieaktualna lub w inny sposób wątpliwa, wybierz ją i naciśnij Ctrl + Enter.
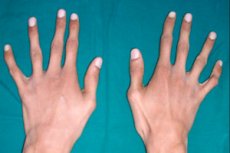
Jedną z rzadkich dziedzicznych patologii tkanki łącznej jest arachnodaktylia – deformacja palców, której towarzyszy wydłużenie kości rurkowych, krzywizny szkieletu, zaburzenia układu sercowo-naczyniowego i narządu wzroku.
Chorobę po raz pierwszy opisali dr Williams i francuski pediatra Marfan, którzy nazwali ją dolichostenomelia. Później w medycynie światowej pojawił się termin zespół Marfana, a od 1902 roku używa się nazwy arachnodaktylia. Patologia ta jest związana z wrodzonymi zaburzeniami tkanki łącznej, a za jeden z głównych objawów uważa się wydłużone, cienkie i zakrzywione palce „pajączka”. [ 1 ]
Epidemiologia
Arachnodaktylia jest uważana za dziedziczną, monogenową patologię tkanki łącznej, dziedziczoną w sposób autosomalny dominujący, o dużej penetracji i różnym stopniu ekspresji.
W około 75-80% przypadków choroba ma charakter dziedziczny, w pozostałych przypadkach powstaje w wyniku spontanicznych mutacji (w szczególności mutacji typu point missense). [ 2 ]
Udowodniono, że cechy patogenetyczne arachnodaktylii są spowodowane zmianami w kilku genach (w 95% przypadków):
- w genie fibryliny-1 (zbadano około tysiąca mutacji) na chromosomie 15q21.1;
- Gen TGFβR1 lub TGFβR2 na chromosomie 9 i 3p24.2-P25.
Zmiany te mają bezpośredni wpływ na zakres objawów klinicznych.
Mutacje w łańcuchu α-2 kolagenu typu I opisano u 5% pacjentów.
Częstość występowania arachnodaktylii wynosi około 2 przypadki na 5 tysięcy osób. Nie ma determinacji rasowej ani płciowej. [ 3 ]
Przyczyny arachnodaktylia
Arachnodaktylia występuje w wyniku spontanicznej mutacji. Choroba nie charakteryzuje się powszechnie znanymi objawami wrodzonych patologii dziedzicznych, a wydłużone palce manifestują się głównie w zespole Marfana i homocystynurii.
Choroba jest rzadka, a u wszystkich pacjentów stwierdzono mutację genu FBN1 (genu fibryliny) zlokalizowanego na chromosomie 15 w regionie q21.1. Kliniczny polimorfizm zespołu można wyjaśnić masą mutacji, przy czym około 15% to zmiany mutacyjne, które wystąpiły w trakcie poczęcia. [ 4 ]
Nietypowe odmiany arachnodaktylii spowodowane są mutacjami w innych genach: odkryto związek pomiędzy rozwojem patologii a mutacjami w genie LTBP3, R, który zlokalizowany jest na chromosomie 14 w regionie q24 i transformuje czynnik wzrostu.
Zdecydowana większość mutacji to tzw. mutacje missense (około 57%). Ponad 20% to małe delecje, z utratą części chromosomów, około 12% to mutacje miejsc splicingowych, 8% to mutacje nonsensowne, a 2% to przegrupowania i delecje na dużą skalę. [ 5 ]
Wrodzona arachnodaktylia skurczowa jest spowodowana zaburzeniem syntezy czynnika białkowego fibryliny-2. Problem jest spowodowany mutacją w genie FBN2, zlokalizowanym na piątym chromosomie w regionie q23-q31. Wszystkie mutacje są przeważnie mutacjami punktowymi, zmieniającymi kodon, aby kodował inny aminokwas. [ 6 ]
Homocystynuria rozwija się na tle upośledzonego metabolizmu niezbędnego aminokwasu metioniny. Podstawą patologii może być utrata aktywności lub jej spadek w następujących substancjach enzymatycznych:
- Enzym beta-syntazy cystationiny (CBS). Patologia jest oporna na B6 i objawia się objawami charakterystycznymi dla formy niezależnej od B6 , jednak wprowadzenie preparatu witaminy B6 nie prowadzi do poprawy.
- Enzym N5, N10 reduktaza metylenotetrahydrofolianowa (MTHFR). Ten czynnik enzymatyczny jest substratem, który powoduje demetylację homocysteiny i jej przekształcenie w metioninę, niezbędny aminokwas, który jest składnikiem wielu substancji białkowych i peptydowych.
- Enzym N5 metylenotetrahydrofolian. Mówimy o zależnej od witaminy B 6 formie patologii, która rozwija się wraz z niedoborem witaminy B 6. Wprowadzenie preparatu witaminowego do organizmu pozwala na poprawę stanu pacjenta.
- Enzym transmetylaza homocysteiny. Rozwija się na tle zaburzeń metabolicznych kobalaminy – witaminy B 12.
Czynniki ryzyka
Arachnodaktylia to genetycznie uwarunkowana choroba charakteryzująca się systemowym uszkodzeniem tkanki łącznej. Patologia jest związana ze zmianami w genie fibryliny 1, zlokalizowanym na krótkim ramieniu chromosomu 15 w locus 21.1.
Arachnodaktylia jest dziedziczona w sposób autosomalny dominujący, z wysoką penetracją i zmienną ekspresją. Patologia może objawiać się zarówno po stronie męskiej, jak i żeńskiej.
Patogeneza
Ponad 50% masy ciała człowieka stanowią struktury tkanki łącznej, w szczególności szkielet, skóra, sieć naczyniowa, limfa i krew.
Komórki tkanki łącznej reprezentowane są przez fibroblasty i ich podtypy: osteoblasty, chondrocyty, keratoblasty, odontoblasty, a także makrofagi i komórki tuczne.
Tkanka łączna zarodkowa jest materiałem do tworzenia składników konstytucyjnych, genetycznych i epigenetycznych. Choroby tkanki łącznej odbijają się w mniejszym lub większym stopniu na całym ciele jako całości, na jego zdolnościach funkcjonalnych i konstytucji.
W arachnodaktylii występuje substytucja nukleotydów w genie zawierającym informacje strukturalne o peptydzie fibryliny-1. Ta substancja białkowa należy do grupy glikoprotein, uczestniczy w układzie mikrofibrylarnym i tworzy podstawę włókienek sprężystych tkanki łącznej.
Tkanka utrzymuje stabilną strukturę dzięki macierzy międzykomórkowej, która zawiera wiele czynników wzrostu zapewniających systematyczną odnowę komórkową. Duże naczynia i więzadła zawierają liczne włókienka elastyny, których uszkodzenie powoduje główne objawy arachnodaktylii.
Znacznemu uszkodzeniu ulega transformujący czynnik wzrostu β – jego nieaktywna forma nie ulega wiązaniu, co prowadzi do wzrostu aktywności biologicznej tego czynnika.
Zaburzenia fibrylarne prowadzą do nieprawidłowego tworzenia się włókien, czego skutkiem jest utrata wytrzymałości i elastyczności skóry oraz innych struktur tkanki łącznej.
Gdy struktura kolagenu ulega zaburzeniu, podstawowe ogniwo hemostazy zostaje przerwane.
Eksperci zauważają udział zaburzeń hormonalnych w powstawaniu i postępie anomalii w strukturach tkanki łącznej, w tym arachnodaktylii. Objawy zakrzepowe są determinowane przez zaburzenia reologiczne - w szczególności zmiany lepkości krwi w zmodyfikowanych naczyniach okolicy ramienno-głowowej.
Przewód pokarmowy jest dotknięty zaburzeniami kolagenu: obserwuje się hipomotoryczną dyskinezę dróg żółciowych, przepuklinę ujścia przełyku przepony, anomalie wątroby i dróg żółciowych, przewlekłą postać „zatartego” zapalenia żołądka i dwunastnicy, dolichosigma.
Jak dziedziczy się arachnodaktylię?
Arachnodaktylia jest dziedziczona jako cecha autosomalna dominująca, ale może również wystąpić w wyniku spontanicznych mutacji. Oznacza to, że patologia niekoniecznie musi ujawniać się u jednego z bliskich krewnych - na przykład u rodziców, dziadków. Mutacje leżące u podstaw patologii mogą ujawniać się losowo.
Objawy arachnodaktylia
W medycynie rozróżnia się arachnodaktylię utajoną i jawną. W arachnodaktylii utajonej zmiany są obecne, ale są izolowane i ograniczone do jednego lub dwóch układów narządów. Jawna arachnodaktylia objawia się wieloma widocznymi zaburzeniami o różnym nasileniu objawów. W tym przypadku stan pacjenta może być stosunkowo stabilny przez dziesięciolecia lub stale postępować, objawiając się w odniesieniu do innych narządów i układów.
Często zespół arachnodaktylii można wykryć już w pierwszych dniach po urodzeniu dziecka.
Głównym zewnętrznym objawem arachnodaktylii są cienkie i wydłużone palce, które ze względu na krótkie ścięgna nabierają typowej krzywizny i przypominają nogi pająka.
Palce pająka lub arachnodaktylia stają się wyraźnie widoczne niemal od okresu noworodkowego. Jednak znak ten staje się bardziej oczywisty w wieku około trzech lat.
Charakterystyczne są również wskaźniki wzrostu: dzieci są zazwyczaj wysokie, przedramiona i piszczele są długie, kończyny są nieproporcjonalne i cienkie. Dysproporcja ta jest szczególnie widoczna w wysokim umiejscowieniu talii i rzepek kolanowych. [ 7 ]
Inne choroby układu kostnego obejmują:
- zwężony i wydłużony kształt czaszki (dolichocefaliczny) z nieprawidłowo ukształtowaną częścią twarzową;
- lejkowaty kształt klatki piersiowej (tzw. „ptak”);
- wygięty kręgosłup;
- wrodzone zwichnięcia stawu biodrowego;
- nawykowe zwichnięcia stawu kolanowo-barkowego;
- skrzywienie kości piętowej;
- formacje osteofitowe – narośla kostne;
- płaskostopie;
- niewystarczający rozwój warstwy tłuszczu.
Dodatkowe objawy arachnodaktylii mogą obejmować:
- krótkowzroczność;
- niebieskawa twardówka;
- podwichnięcie soczewki;
- choroby serca i naczyń krwionośnych (wady serca, tętniak aorty);
- wyraźna szczupłość;
- nadmierna ruchomość stawów;
- "łukowate" niebo.
Arachnodaktylia charakteryzuje się wydłużonymi kośćmi rurkowatymi, powodującymi różne krzywizny szkieletu. Ponadto wielu pacjentów ma zaburzenia piramidowe, asymetrię odruchów ścięgnistych, anosokorię i oczopląs na tle prawidłowego rozwoju umysłowego.
Jeśli mówimy o arachnodaktylii, której towarzyszy homocystynuria, to u pacjenta mogą wystąpić następujące objawy:
- okresowe ataki drgawek;
- jaskra wtórna z podwichnięciem soczewki;
- odwarstwienie siatkówki, astygmatyzm;
- uszkodzenia pni tętniczych (m.in. nerek, mózgu);
- osteoporoza;
- zakrzepica;
- upośledzenie umysłowe.
Arachnodaktylia u noworodków
W większości przypadków arachnodaktylia może być zidentyfikowana u dziecka w ciągu pierwszych kilku dni jego życia. Jednak wraz z wiekiem objawy mają tendencję do pogarszania się.
Pierwszymi objawami pozwalającymi podejrzewać chorobę są zazwyczaj:
- niezwykle długie kończyny i palce;
- niedowaga przy odpowiedniej kondycji fizycznej dziecka;
- wydłużona, długa twarz;
- brak tkanki tłuszczowej, słabo rozwinięte mięśnie;
- nadmierna elastyczność stawów.
Od około czwartego roku życia na tle arachnodaktylii zaczynają się zmieniać klatka piersiowa, kręgosłup wygina się, rozwijają się płaskostopie.
W zakresie narządów wzroku obserwuje się krótkowzroczność, ektopię soczewki, zmienioną konfigurację rogówki, zeza, procesy hipoplastyczne tęczówki i siatkówki. Tego typu zaburzenia można zauważyć już w pierwszych 2-3 latach życia dziecka, choć z biegiem lat postępują.
Największe niebezpieczeństwo stwarzają zaburzenia układu sercowo-naczyniowego. Jeśli takie zaburzenia występują, to przy braku odpowiedniego leczenia istnieje wysokie ryzyko zgonu pacjenta już w dzieciństwie. Wśród szczególnie niebezpiecznych patologii można wyróżnić uszkodzenia ścian naczyń, wady rozwojowe serca, wady naczyń wieńcowych. Czasami u dzieci w pierwszym roku życia wykrywa się już narastającą niewydolność serca.
Arachnodaktylia może być połączona z uszkodzeniem innych narządów, w szczególności układu nerwowego, oskrzeli i płuc, skóry i układu moczowo-płciowego. Takie zaburzenia są wykrywane podczas procedur diagnostycznych.
Komplikacje i konsekwencje
Najczęstsze skutki uboczne arachnodaktylii to uszkodzenia serca i narządów oddechowych. Ponadto pojawiają się problemy ze wzrokiem, aż do jego utraty włącznie.
Pacjenci z arachnodaktylią wymagają kompleksowej terapii wszystkich istniejących patologii. Jeśli takie leczenie nie jest przeprowadzane, oczekiwana długość życia pacjentów ulega znacznemu skróceniu: rzadko zdarza się, że pacjenci bez interwencji medycznej dożywają 40 lat. Z biegiem lat nasilają się problemy z układem sercowo-naczyniowym, wzrasta ryzyko rozległych krwotoków o tragicznym przebiegu.
Osoby cierpiące na arachnodaktylię powinny regularnie poddawać się badaniom i leczyć towarzyszące patologie. Tylko wówczas mają szansę na długie życie bez poważnych powikłań.
Zespół Marfana i arachnodaktylia wymagają szczególnej uwagi, jeśli pacjentka zajdzie w ciążę. W takiej sytuacji ważne jest regularne i dokładne badanie pacjentki oraz medyczne wsparcie stanu jej układu sercowo-naczyniowego. Tylko w ten sposób można zagwarantować pomyślną ciążę i bezpieczny poród dziecka.
Aby uniknąć skutków ubocznych, pacjenci z arachnodaktylią powinni być regularnie badani przez lekarzy, zapobiegać rozwojowi patologii układu sercowo-naczyniowego i mięśniowo-szkieletowego. Zaleca się im prowadzenie wyłącznie zdrowego trybu życia, z umiarkowaną aktywnością fizyczną.
Diagnostyka arachnodaktylia
Diagnostyka kliniczna arachnodaktylii obejmuje zbieranie skarg, wywiad rodzinny, ocenę fenotypu, a także badania antropometryczne i fizykalne. Ważne jest ustalenie obecności objawów patologii tkanki łącznej u krewnych w linii prostej: w tym celu przeprowadza się badanie genealogiczne. [ 8 ]
Diagnostyka laboratoryjna arachnodaktylii obejmuje badanie stanu określonych typów tkanki łącznej, reprezentowanych przez tkankę kostną i chrzęstną, krew i limfę. Za najbardziej pouczające uważa się badanie poziomu oksyproliny i glikozaminoglikanów w dobowej objętości moczu. Ponadto ocenia się zawartość lizyny, proliny i oksyproliny we krwi. Aby określić zmienione stosunki różnych typów kolagenów i nieprawidłowości strukturalne włókien kolagenowych, zaleca się typowanie metodą pośredniej immunofluorescencji z wykorzystaniem przeciwciał poliklonalnych do kolagenu i fibronektyny. [ 9 ] W zależności od wskazań wykonuje się następujące badania w celu odzwierciedlenia jakości procesów metabolicznych tkanki łącznej:
- glikozaminoglikany, fibrylina, fibronektyna;
- badanie hydroksyproliny, markerów biosyntezy kolagenu typu 1, aminokońcowych propeptydów prokolagenu typu 1, markerów degradacji kolagenu typu 1, galaktozyloksylizyny, deoksypirydynoliny;
- analiza regulacji metabolizmu kolagenu (badanie metaloproteinaz macierzy i tkankowych inhibitorów metaloproteinaz macierzy, transformującego czynnika wzrostu);
- analiza mikro- i makroelementów (zawartość wapnia i magnezu, fosforu, żelaza, siarki i miedzi, kobaltu i selenu, cynku i manganu, fluoru i wanadu, krzemu i boru);
- badanie markerów tworzenia tkanki kostnej i tempa procesów przebudowy (analiza zawartości osteokalcyny, kostnej fosfatazy alkalicznej, parathormonu, hormonu somatotropowego, prolaktyny, witaminy D3 , pentozydyny, homocysteiny w moczu i krwi).
Diagnostyka instrumentalna ma na celu identyfikację istniejących wad rozwojowych i ocenę stanu czynnościowego narządów i układów. Zaburzenia układu krążenia w arachnodaktylii wymagają obowiązkowego uwzględnienia w diagnostycznej liście takich procedur jak:
- elektrokardiografia;
- 24-godzinny monitoring EKG;
- badanie ultrasonograficzne serca i naczyń krwionośnych.
Anomalie naczyniowe bada się za pomocą tomografii komputerowej lub obrazowania metodą rezonansu magnetycznego. Dodatkowe procedury diagnostyczne mogą obejmować:
- USG narządów jamy brzusznej, układu moczowo-płciowego;
- Zdjęcie rentgenowskie narządów klatki piersiowej, stawów biodrowych; [ 10 ]
- TK lub MRI kręgosłupa.
Po wykonaniu wszystkich niezbędnych badań pacjent kierowany jest na poradnictwo genetyczne.
Diagnostyka różnicowa
Istnieje podobieństwo fenotypowe między zespołem Bealsa a arachnodaktylią w zespole Marfana (mutacje odpowiednio genów FBN2 i FBN1), co wynika z niemal całkowitej identyczności substancji białkowych fibryliny 1 i fibryliny 2. Nie jest zaskakujące, że drugą nazwą zespołu Bealsa jest arachnodaktylia przykurczowa. [ 11 ]
Różnicowanie przeprowadza się również w przypadku innych patologii tkanki łącznej:
- Zespół Sticklera;
- zespół Ehlersa-Danlosa;
- homocystynuria;
- artrogrypoza.
Zespół Bealsa charakteryzuje się fenotypem marfanoidalnym, wrodzonymi przykurczami zgięciowymi dużych i małych stawów, arachnodaktylią nadgarstka i stopy, krzywizną kręgosłupa i nieprawidłowym kształtem uszu (tzw. „pogniecione” małżowiny uszne). W celu potwierdzenia diagnozy przeprowadza się analizę molekularną genu FBN2.
Artrogrypoza charakteryzuje się licznymi przykurczami stawów, niskim wzrostem i obniżoną inteligencją. Kształt palców i uszu jest nieistotny. [ 12 ]
Zespół Ehlersa-Danlosa charakteryzuje się kifoskoliozą, lejkowatym wygięciem klatki piersiowej, wyraźnym płaskostopiem i upośledzoną refrakcją. Typowe są zwiększona ruchomość i zwichnięcia stawów, duża rozciągliwość skóry i wrażliwość.
Zespół Sticklera charakteryzuje się zmianami objętości stawów i ich sztywnością.
Z kim się skontaktować?
Leczenie arachnodaktylia
Arachnodaktylia jest patologią genetyczną, a obecnie medycyna nie dysponuje metodami korygowania defektów genetycznych. Dlatego leczenie ma na celu optymalizację stanu pacjenta, zapobieganie zaostrzeniu patologii i eliminację objawów objawowych. Zalecana jest kompleksowa terapia, angażująca kilku specjalistów medycznych jednocześnie, w zależności od rodzaju najbardziej wyraźnych objawów: często konieczne jest dodatkowo skontaktowanie się z ortopedą, kardiologiem, okulistą, gastroenterologiem i lekarzami innych specjalności. [ 13 ]
Wśród zaleceń dotyczących postępowania klinicznego z pacjentami za zasady ogólne uznaje się:
- ograniczenie aktywności fizycznej, ale nie jej całkowita eliminacja (w ramach wspomagania układu sercowo-naczyniowego);
- terapia farmakologiczna;
- w razie konieczności – korekcja chirurgiczna najbardziej dotkniętych obszarów serca i naczyń krwionośnych;
- korekta ortopedyczna;
- leczenie uzdrowiskowe, fizjoterapia, ćwiczenia lecznicze.
Dieta pacjentów z arachnodaktylią powinna zawierać wystarczającą ilość produktów wysokobiałkowych wzbogaconych o mikroelementy, witaminy i kwasy tłuszczowe. Zaleca się spożywanie mięsa, ryb, owoców morza, fasoli i orzechów. Jeśli arachnodaktylia jest spowodowana homocystynurią, wówczas spożycie białka zwierzęcego jest mocno ograniczone.
Dzieciom o szczupłej budowie i wysokim wzroście zaleca się wprowadzenie do diety oleju bawełnianego i sojowego, nasion słonecznika, tłuszczu wieprzowego i smalcu od najmłodszych lat. Ponadto oferują preparaty zawierające wielonienasycone kwasy tłuszczowe, takie jak Omega, które hamują produkcję hormonu somatotropowego.
Aby znormalizować metabolizm białek, zaleca się witaminy z grupy B. Można je również uzyskać z produktów spożywczych: gryki, grochu, wątróbki.
Bardzo ważne jest, aby kwas askorbinowy dostał się do organizmu pacjenta wraz z pożywieniem. W tym celu do diety koniecznie należy włączyć napar z dzikiej róży, paprykę, kapustę, owoce cytrusowe, a także rokitnik i por.
W razie potrzeby pacjentom proponuje się korekcję ortopedyczną, która jest konieczna, aby zmniejszyć obciążenie kręgosłupa i stawów. W tym celu stosuje się obuwie ortopedyczne, aparaty na kolana i inne, wkładki, bandaże elastyczne.
Leczenie chirurgiczne przeprowadza się w zależności od wskazań.
Leki
Leczenie farmakologiczne arachnodaktylii przeprowadza się 1-2 razy w roku, w zależności od stanu pacjenta i nasilenia objawów patologicznych. Czas trwania kuracji ustalany jest indywidualnie i wynosi średnio 4 miesiące. [ 14 ]
W celu stymulacji produkcji kolagenu przepisuje się następujące leki: Piaskledin 300, L-lizynę lub L-prolinę w połączeniu ze złożonymi preparatami multiwitaminowymi zawierającymi kwas askorbinowy, witaminy z grupy B, tokoferol, magnez, cynk, selen, miedź.
Spośród chondroprotektorów najbardziej optymalne zastosowanie ma siarczan chondroityny i siarczan glukozaminy - leki biorące udział w regulacji metabolizmu chondrocytów, hamowaniu syntezy enzymów, zwiększaniu wrażliwości chondrocytów na działanie enzymów, stymulacji procesów anabilistycznych itp. Za optymalne środki łączone uważa się takie leki: Teraflex, Arthroflex, Arthra itp.
Metabolizm minerałów jest stymulowany przez leki normalizujące procesy fosforowo-wapniowe. Lekami z wyboru są często aktywne formy witaminy D: Alpha D 3 - Teva, Oxidevit, Bonviva itp. Jednocześnie stosuje się preparaty fosforowe, wapniowe i magnezowe. Podczas leczenia mniej więcej raz na 20 dni sprawdza się poziom wapnia i fosforu we krwi lub moczu, a także wykonuje się badanie krwi na fosfatazę alkaliczną.
Aby poprawić stan bioenergetyczny organizmu można przepisać Phosphaden, Riboxin, Lecithin, Elkar, Coenzyme Q10.
Przybliżony schemat leczenia może wyglądać następująco:
- Chondroprotector w dawce odpowiedniej do wieku, przyjmowany z jedzeniem i odpowiednią ilością wody. Czas trwania jednego cyklu leczenia wynosi 3-4 miesiące.
- L-prolinę w dawce 500 mg (dla dzieci od 12 lat i dorosłych) przyjmuje się pół godziny przed posiłkiem, 1-2 razy dziennie, przez sześć tygodni. Jeśli jest to wskazane, można dodatkowo przepisać kompleks aminokwasów - L-prolinę, L-lizynę, L-leucynę w ilości 10-12 mg/kg masy ciała. Przyjmowanie odbywa się 1-2 razy dziennie, przez dwa miesiące.
- Kompleks witaminowo-mineralny Centrum, lub Vitrum, lub Unicap, w dawkowaniu uwzględniającym wiek. Czas podawania wynosi 4 tygodnie.
Ten schemat leczenia jest odpowiedni, gdy pacjent z arachnodaktylią skarży się na problemy z układem mięśniowo-szkieletowym, a wyniki badań wskazują na zwiększone wydalanie glikozaminoglikanów w codziennym badaniu moczu i obniżone stężenie wolnych aminokwasów we krwi.
Z reguły leczenie jest dobrze odbierane przez pacjentów, bez żadnych szczególnych skutków ubocznych. Jeśli zostaną wykryte reakcje nadwrażliwości, leki są wymieniane, a schemat leczenia dostosowywany.
Leczenie fizjoterapeutyczne
Procedury fizjoterapeutyczne w przypadku arachnodaktylii są przepisywane zgodnie ze wskazaniami. Na przykład w przypadku niewystarczającej osteogenezy, w celu poprawy gojenia złamań kości lub w przypadku objawów osteoporozy zaleca się elektroforezę z 5% chlorkiem wapnia, 4% siarczanem magnezu, 2% siarczanem miedzi lub 2% siarczanem cynku.
W przypadku stwierdzenia zaburzeń wegetatywno-naczyniowych stosuje się 1% roztwór benzoesanu kofeiny sodowej, chlorowodorek efedryny lub mezaton.
W celu pobudzenia czynności kory nadnerczy zaleca się elektroforezę leków z 1,5% etimizolem i terapię decimetrem okolicy nadnerczy. [ 15 ]
Aby ustabilizować napięcie naczyń krwionośnych, zaleca się zabiegi wodne, które promują „gimnastykę” naczyniową. Doskonałe są kąpiele z dwutlenkiem węgla, sosną, chlorkiem wodoru, siarkowodorem i radonem. Praktykuje się rozcieranie, polewanie, natryski kontrastowe, kąpiele pianowe i solne.
W celu poprawy stanu tkanki chrzęstnej stosuje się terapię magnetyczną, indukcję, terapię laserową oraz elektroforezę z zastosowaniem dimetylosulfotlenku (Dimexide).
Leczenie chirurgiczne
Operacje chirurgiczne w przypadku arachnodaktylii przepisuje się ściśle według wskazań. Przykładowo, jeśli na tle wypadania płatków zastawkowych wykryto poważne zaburzenia hemodynamiczne, wykonuje się masywne tętniaki aorty, wymianę zastawki i uszkodzenie odcinka aorty. [ 16 ]
W przypadku wyraźnych zaburzeń czynnościowych układu oddechowego i sercowo-naczyniowego, które są konsekwencją znacznego skrzywienia klatki piersiowej, wykonuje się torakoplastykę.
W przypadku postępującego zespołu bólowego spowodowanego ciężką skoliozą 3-4 stopni wskazana jest również interwencja chirurgiczna. Z punktu widzenia okulistycznego bezwzględnymi wskazaniami do usunięcia soczewki są podwichnięcie soczewki powikłane jaskrą wtórną, a także zaćma i zmiany zwyrodnieniowe siatkówki o wysokim ryzyku odwarstwienia.
Wszelkie zabiegi chirurgiczne u pacjentów z arachnodaktylią i innymi zaburzeniami struktur tkanki łącznej wykonuje się dopiero na etapie względnej ulgi klinicznej i biochemicznej. Po zabiegu konieczna jest długotrwała obserwacja lekarska i intensywna terapia lekami poprawiającymi metabolizm tkanki łącznej.
Zapobieganie
Arachnodaktylia to rzadka patologia genetyczna. Czasami występuje spontanicznie u pozornie zdrowych rodziców. Dlatego bardzo, bardzo trudno jest zapobiec chorobie z wyprzedzeniem.
Jeśli jeden z potencjalnych rodziców ma obciążony wywiad rodzinny - czyli wiadomo, że ktoś w rodzinie cierpiał na arachnodaktylię - wówczas małżonkowie powinni udać się do genetyka i poddać się badaniu genetycznemu na etapie planowania dziecka. Po potwierdzeniu ciąży lekarz przeprowadza diagnostykę prenatalną, w tym badanie USG płodu oraz szereg badań biochemicznych:
- badanie krwi matki;
- analiza płynu owodniowego;
- pobieranie kosmówki kosmówki;
- analiza komórek łożyska i krwi pępowinowej.
Pacjenci z arachnodaktylią są pod opieką lekarską przez całe życie. Działania profilaktyczne u pacjentów mają na celu zapobieganie powikłaniom. W tym celu wykonuje się korektę kardiochirurgiczną, przepisuje się leczenie farmakologiczne w celu wyeliminowania ryzyka tworzenia się skrzepu. Okresowo stosuje się kuracje antybiotykowe.
Prognoza
Rokowanie co do życia pacjentów z arachnodaktylią jest determinowane przede wszystkim przez ciężkość współistniejących schorzeń - w szczególności chorób układu sercowo-naczyniowego, układu mięśniowo-szkieletowego i narządów wzroku. Najczęściej patologię komplikuje pęknięcie i rozwarstwienie aorty. Należy to wziąć pod uwagę i wykonać terminową korektę kardiochirurgiczną, która pomoże przedłużyć życie pacjenta i poprawić jego jakość.
Jeśli diagnoza została postawiona w odpowiednim czasie, a zalecenia lekarza są przestrzegane, rokowanie można nazwać warunkowo korzystnym. Pomoc medyczna znacznie łagodzi przebieg arachnodaktylii, a pacjenci mają możliwość prowadzenia normalnego i stosunkowo pełnego życia bez rozwoju poważnych powikłań.

