Zawory serca
Ostatnia recenzja: 23.04.2024

Cała zawartość iLive jest sprawdzana medycznie lub sprawdzana pod względem faktycznym, aby zapewnić jak największą dokładność faktyczną.
Mamy ścisłe wytyczne dotyczące pozyskiwania i tylko linki do renomowanych serwisów medialnych, akademickich instytucji badawczych i, o ile to możliwe, recenzowanych badań medycznych. Zauważ, że liczby w nawiasach ([1], [2] itd.) Są linkami do tych badań, które można kliknąć.
Jeśli uważasz, że któraś z naszych treści jest niedokładna, nieaktualna lub w inny sposób wątpliwa, wybierz ją i naciśnij Ctrl + Enter.
Wcześniej uważano, że wszystkie zastawki serca są prostymi strukturami, których wkład w jednokierunkowy przepływ krwi jest po prostu biernym ruchem w odpowiedzi na działający gradient ciśnienia. Takie rozumienie "struktur biernych" doprowadziło do powstania "pasywnych" mechanicznych i biologicznych substytutów zastawek.
Teraz staje się jasne, że zastawki serca mają bardziej złożoną strukturę i funkcję. Dlatego stworzenie "aktywnego" substytutu zastawki serca sugeruje znaczne podobieństwo w jego strukturze i funkcji z naturalnym zastawieniem serca, które w długim okresie jest całkiem możliwe dzięki rozwojowi inżynierii tkankowej.
Zawory serca rozwijają się z embrionalnych pączków tkanki mezenchymalnej podczas wprowadzania endokardium. W procesie morfogenezy powstaje kanał przedsionkowo-komorowy (zastawki trójdzielnej i zastawki mitralnej) i komorowy przewód odpływowy (aortalne i płucne zastawki serca).
Jak układają się zawory serca?
Początek badań nad dopływem krwi do zastawek został postawiony przez Luschkę (1852), za pomocą zastrzyku naczyń sercowych o kontrastującej masie. Znalazł liczne naczynia krwionośne w zastawkach zastawki przedsionkowo-komorowej i półksiężycowej aorty i tętnicy płucnej. Jednak w wielu przewodnikach dotyczących anatomii i histologii patologicznej istniały przesłanki, że niezmienionych ludzkich zastawek serca nie zawierają żadnych naczyń krwionośnych i ten ostatni występujący tylko w zaworach w różnych procesów patologicznych - miażdżycy o różnej etiologii i wsierdzia. Informacje o nieobecności naczyń krwionośnych opierały się głównie na badaniach histologicznych. Założono, że przy braku naczyń krwionośnych w wolnej części zastawek ich odżywianie następuje poprzez filtrowanie płynu z plazmy krwi, która wymiata zastawki. Obserwowano penetrację kilku naczyń wraz z włóknami prążkowanej tkanki mięśniowej do podstawy zastawek i ścięgien ścięgnistych.
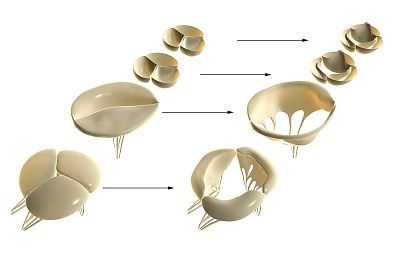
Jednakże, gdy naczynia wtrysku serca różnych barwników (osnowa z żelatyny, bizmut żelatyny zawiesiny wodnej czarny tusz do rzęs, roztwory karmin lub błękitu trypanu), stwierdzono, że zbiorniki przenikać zawory cerdechnye przedsionkowo-komorowych tętnicy aorty i płucnych, wraz z tkanki mięśnia sercowego , nieznacznie nie osiągając wolnej krawędzi liścia.
W kruchej włóknistej tkance łącznej zastawek zastawek przedsionkowo-komorowych stwierdzono oddzielne główne naczynia, które zespalają się z naczyniami szeregu zlokalizowanych obszarów mięśnia poprzecznego serca.
Największa liczba naczyń krwionośnych była zlokalizowana u podstawy i stosunkowo mniej - w wolnej części tych zaworów.
Według KI Kulchitsky i wsp. (1990) w zastawce dwudzielnej znajduje się większa średnica naczyń tętniczych i żylnych. U podstawy zaworów tego zaworu znajdują się głównie główne naczynia z wąską pętlą sieci kapilar wchodzących w podstawową część zaworu i zajmujące 10% jego powierzchni. W zastawce trójdzielnej naczynia tętnicze mają mniejszą średnicę niż w zastawce mitralnej. W zaworach tego zaworu znajdują się głównie naczynia rozproszone i stosunkowo szerokie pętle naczyń włosowatych. W zastawce mitralnej, przedni liść intensywniej przepływa krwi, w zastawce trójdzielnej, zastawce przedniej i tylnej, które pełnią funkcję głównego zamknięcia. Stosunek średnic naczyń tętniczych i żylnych w zastawkach przedsionkowo-komorowych serca osób dojrzałych wynosi 1: 1,5. Pętle kapilarne są wielokątne i usytuowane prostopadle do podstawy klapek zaworu. Statki tworzą płaską sieć zlokalizowaną pod śródbłonkiem od strony przedsionków. Naczynia krwionośne znajdują się również w akordach ścięgien, gdzie przenikają z mięśni brodawkowatych prawej i lewej komory do odległości do 30% długości cięciwy ścięgna. Liczne naczynia krwionośne tworzą łukowate pętle u podstawy ścięgien ścięgnistych. Zawory serca aorty i pnia płucnego w celu ukrwienia znacznie różnią się od przedsionkowo-komorowych. Główne naczynia o stosunkowo mniejszej średnicy pasują do podstawy półksiężycowatych zaworów zastawek aortalnych i płucnych. Krótkie gałęzie tych naczyń kończą się pętlami kapilarnymi o nieregularnym kształcie owalnym i wielokątnym. Są one zlokalizowane głównie w pobliżu podstawy półksiężycowatych skrzydeł. Naczynia żylne w podstawie zastawek aorty i tętnicy płucnej mają również mniejszą średnicę niż u podstawy zastawek przedsionkowo-komorowych. Stosunek średnic naczyń tętniczych i żylnych w zastawkach aorty i tętnicy płucnej serca osób dojrzałych wynosi 1: 1,4. Z większych naczyń rozgałęziają się krótkie gałęzie boczne, zakończone kapilarami o niewłaściwym kształcie owalnym i wielokątnym.

Z wiekiem jest wulgaryzowaniem włókien tkanki łącznej, takich jak kolagen oraz elastynę, jak również zmniejszenie liczby luźnych włókien tkanki łącznej nieregularnym tworzy płat tkanki stwardnienie-komorowego, zawory i Płatki zastawek półksiężycowatych aorty i tętnicy płucnej. Zmniejszone włókna długość zastawki serca mięśni prążkowanych, a tym samym zmniejsza ilość i liczbę penetracji w głąb zawory naczyń krwionośnych. W związku z tymi zmianami zastawki serca tracą swoje właściwości sprężyste i elastyczne, co wpływa na mechanizm zamykania zaworów i hemodynamiki.
Zawory serca mają sieci naczyń limfatycznych i niewielką liczbę naczyń limfatycznych wyposażonych w zastawki. Limfatyczne kapilary zaworów mają charakterystyczny wygląd: ich światło jest bardzo nieregularne, ta sama kapilara w różnych obszarach ma inną średnicę. Na styku kilku kapilar powstają przedłużenia - luki o różnych kształtach. Pętle sieciowe są często nieregularne wielokątne, rzadziej owalne lub okrągłe. Często pętle sieci limfatycznej nie są zamknięte, a kapilary limfatyczne kończą się ślepo, a pętle kapilarne limfatyczne są zorientowane częściej w kierunku od swobodnej krawędzi zastawki do podstawy. W wielu przypadkach w zaworach zastawki przedsionkowo-komorowej znaleziono dwuwarstwową sieć naczyń limfatycznych.
Pleksy nerwowe śródskładka znajdują się w różnych warstwach, głównie pod śródbłonkiem. Na swobodnym brzegu klap zaworowych znajdują się włókna nerwowe, głównie promieniowo, łączące się z włóknami ścięgien. Bliżej podstawy zaworów znajduje się splot dużego splotu, który łączy się ze splotem wokół pierścieni włóknistych. Na zastawkach półkulistych sieć neuronowa wsierdzia jest rzadsza. W miejscu zamocowania zaworów staje się gruby i wielowarstwowy.
Struktura komórkowa zastawek serca
Komórki śródmiąższowe zastawki odpowiedzialne za utrzymanie konstrukcji zaworu mają wydłużony kształt z dużą liczbą cienkich procesów, które rozciągają się przez całą macierzy zaworu. Istnieją dwie populacje komórek śródmiąższowych zastawki, różniących się morfologią i strukturą; niektóre mają właściwości kurczliwe i charakteryzują się obecnością kurczliwych włókienek, inne mają właściwości wydzielnicze i mają dobrze rozwiniętą retikulum endoplazmatyczną i aparat Golgiego. Funkcja kurczliwości jest odporna na ciśnienie hemodynamiczne i jest dodatkowo wspierana przez wytwarzanie zarówno białek kurczliwych, jak i szkieletowych, które obejmują ciężkie łańcuchy alfa i beta-miozyny oraz różne izoformy troponiny. Skurcz zaworu zastawki serca wykazano w odpowiedzi na szereg czynników wazoaktywnych sugerujących koordynujące działanie biologicznego bodźca dla pomyślnego funkcjonowania zastawki.
Komórki śródmiąższowe są również niezbędnymi składnikami układu redukcyjnego struktur, takich jak zastawki serca. Ciągły ruch zaworów i odkształcanie powiązanej z nimi tkanki łącznej powoduje uszkodzenie, na które komórki śródmiąższowe zastawki reagują, aby utrzymać integralność zaworu. Proces odzyskiwania jest kluczowy dla prawidłowego funkcjonowania zastawki, a brak tych komórek we współczesnych modelach sztucznych zastawek prawdopodobnie przyczynia się do strukturalnego uszkodzenia bioprotezy.
Ważnym kierunkiem w badaniu komórek śródmiąższowych jest badanie interakcji między nimi a otaczającą je matrycą, w której pośredniczy przyleganie cząsteczek do ognisk. Zrosty ogniskowe są wyspecjalizowanymi interakcjami między komórką a matrycą, które wiążą cytoszkielet komórki z białkami macierzy poprzez integryny. Działają one również jako miejsca sygnalizacji transdukcji, przekazując informacje mechaniczne z macierzy pozakomórkowej, które mogą wywoływać odpowiedzi, w tym, ale nie wyłącznie, adhezję, migrację, wzrost i różnicowanie komórek. Zrozumienie biologii komórkowej śródmiąższowych komórek śródmiąższowych jest niezbędne do ustalenia mechanizmów, dzięki którym komórki te oddziałują wzajemnie na siebie i na otoczenie, dzięki czemu ta funkcja może być odtwarzana w sztucznych zastawkach.
W związku z rozwojem obiecującego kierunku inżynierii tkankowej zastawek serca, badania komórek śródmiąższowych prowadzone są przy użyciu szerokiej gamy technik. Po walidacji cytoszkieletu komórek barwiących wimentynie, desminy, troponiny, alfa-aktyna mięśni gładkich i miozyny ciężkiego łańcucha alfa i beta-łańcucha lekkiego miozyny-2 miozyny sercowej, alfa i beta-tubuliny. Komórki kurczliwości potwierdzonych pozytywnych odpowiedzi na epinefrin angiotensyny II bradykinina karbachol, chlorek potasu, śródbłonek I. Komórkowa związek funkcjonalny i zweryfikować szczelinowe interakcji karboksiflyuorestseina mikroiniekcji. Wydzielanie matrycy zainstalowany barwienie na prolilo-4-hydroksylazy / kolagenu typu II, fibronektynę, lamininę, siarczan chondroityny. Unerwienie jest zainstalowany blisko zakończeń nerwów motorycznych zbliżeniowego, co wpływa na aktywność hydroksylazy tyrozynowej neuropeptydu Y, acetylocholina, naczyniowoczynnego polipeptydu jelitowego, substancja P, kaptsitonin peptyd związany z genem. Czynników mitogennych oceniano dziedziczona płytkowy czynnik wzrostu, czynnik wzrostu fibroblastów, serotonina (5-HT). Fibroblasty badane komórki śródmiąższowe charakteryzują niekompletnego błony podstawnej, długie, cienkie procesy cytoplazmatyczne w pobliżu połączenia z matrycy rozwiniętej szorstkiej siateczki śródplazmatycznej i aparatu Golgiego, bogactwo mikrowłókien, z utworzeniem wiązania kleju.
Komórki śródkomorowe tworzą funkcjonalną, atromobogenną otoczkę wokół każdego zastawki serca, podobną do śródbłonka naczyniowego. Powszechnie stosowana metoda wymiany zastawki eliminuje funkcję ochronną endokardium, co może prowadzić do odkładania się płytek i fibryny na sztucznych zastawkach, rozwoju infekcji bakteryjnych i zwapnienia tkanek. Inną prawdopodobną funkcją tych komórek jest regulacja leżących poniżej śródmiąższowych komórek śródmiąższowych, podobna do regulacji komórek mięśni gładkich przez śródbłonek. Złożona interakcja istnieje między śródbłonkiem i sąsiednimi komórkami, częściowo za pośrednictwem rozpuszczalnych czynników wydzielanych przez komórki śródbłonka. Komórki te tworzą ogromną powierzchnię, pokrytą mikroostronami po stronie światła, co zwiększa narażenie i możliwą interakcję z substancjami metabolicznymi krwi krążącej.
Śródbłonka często wykazuje cechy morfologiczne i funkcjonalne różnic spowodowanych przez naprężenia ścinające przy ścianie naczynia występujące podczas ruchu krwi, i to samo odnosi się do zaworu komórki osierdziowego otrzymujące zarówno wydłużony i wielokąta. Zmiany struktury komórki mogą wystąpić w wyniku działania miejscowej hemodynamiki na składniki cytoszkieletu komórki lub efektu wtórnego wywołanego przez zmiany w podstawowej macierzy pozakomórkowej. Na poziomie ultrastruktury wnękowe komórki wsierdzia mają połączenia międzykomórkowe, pęcherzyki osocza, nierówną retikulum endoplazmatyczną i aparat Golgiego. Pomimo tego, że powodują czynnika von Willebranda zarówno in vivo jak i w sztucznym środowisku, brak im cielęcia Weibel-Palade (specyficzne granulek zawierających czynnik von Willebranda), które są organellami specyficzne dla śródbłonka naczyniowego. Komórki wsierdzia zastawkowe charakteryzują się silnymi stawami, interakcjami między funkcjonalnymi szczelinami i nakładaniem się fałd marginalnych.
Komórki osierdziowego zachowują aktywność metaboliczną nawet in vitro: generowanie Willebranda, prostacykliny, syntazy tlenku azotu wykazują aktywność z inhibitorami enzymu przekształcającego angiotensynę, silnie wyizolowanych cząsteczek adhezyjnych ICAM-1 i ELAM-1, które są krytyczne dla wiązania komórek jednojądrzastych w rozwoju odpowiedzi immunologicznej. Wszystkie te znaczniki powinny być zawarte w uprawie idealnego hodowli komórkowej, aby stworzyć sztuczną zastawkę przez inżynierii tkankowej, ale immunostymulujące potencjał komórek wsierdzia zastawki sami mogą ograniczyć ich stosowanie.
Zewnątrzkomórkowej Metrix zastawki serca składa się z włókien kolagenu i elastyny makrocząsteczek proteoglikanów i glikoprotein. Kolagen stanowi - 60% suchej masy zastawki, elastyny - 10% i proteoglikanów - 20%. Składnik kolagenowy zapewnia podstawową stabilność mechaniczną zaworu i jest reprezentowany przez kolagen I (74%). II (24%) i V (2%) typy. Wiązki włókien kolagenu są otoczone elastyczną osłoną, która oddziela je od siebie. Łańcuchów bocznych glikozaminoglikanów proteoglikanu cząsteczki mają tendencję do tworzenia substancję podobną do żelu, w których inne cząsteczki oddziałują tworząc trwałe połączenia macierzy i innych składników złożeniu. Glikozoaminoglikany zawór ludzkiego serca składa się głównie z kwasu hialuronowego, w mniejszym stopniu - z siarczanem dermatanu, chondroitynę, 4-siarczan chondroityny, 6 i siarczanu, przy minimalnej siarczanu heparanu. I przebudowa tkanki matrycy aktualizacji reguluje metaloproteinaz macierzy (MMP) i ich inhibitorów tkankowych (Ti). Cząsteczki te uczestniczą również w wielu procesach fizjologicznych i patologicznych Niektóre metaloproteinaz, w tym śródmiąższowe kolagenazy (MMP-1, MMP-13), żelatynazy (MMP-2, MMP-9), i ich inhibitorów tkankowych (Ti-1, pięcio- 2, TI-3) znajdują się we wszystkich zastawkach serca. Nadmierne wytwarzanie metaloproteinazy jest typowe dla stanów patologicznych zastawki serca.
 [6], [7], [8], [9], [10], [11], [12], [13], [14], [15], [16]
[6], [7], [8], [9], [10], [11], [12], [13], [14], [15], [16]
Zastawki serca i ich struktura morfologiczna
Zawory serca składają się z trzech morfologicznie różnych i funkcjonalnie istotnych warstw matrycy zastawki - włóknistej, gąbczastej i komorowej.
Warstwa włóknista tworzy odporną na obciążenie ramę klapy zaworu, składającą się z warstw włókien kolagenowych. Te włókna są rozmieszczone promieniowo w postaci fałd dla możliwości rozciągania zaworów tętniczych po zamknięciu. Warstwa włóknista znajduje się w pobliżu zewnętrznej powierzchni wylotowej tych zaworów. Włókniste warstwy zastawek przedsionkowo-komorowych służą jako kontynuacja wiązek kolagenu w pasmach ścięgien. Znajduje się pomiędzy warstwami gąbczastymi (wejście) i komorowymi (wyjściowymi).
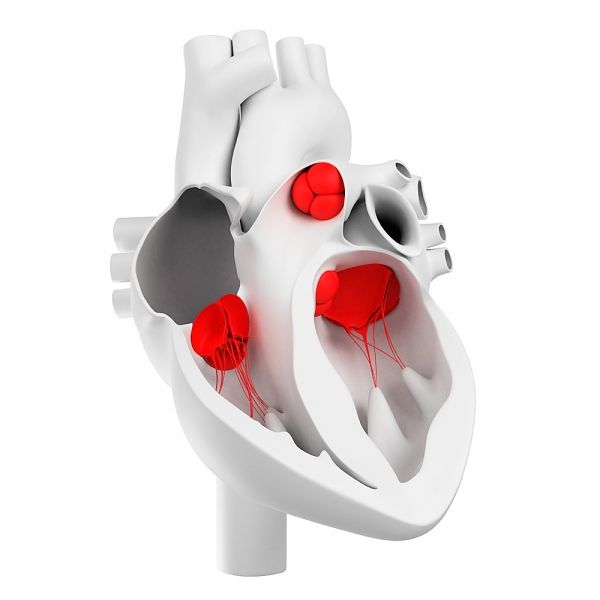
Między włóknistą a komorową znajduje się warstwa gąbczasta (spongiosa). Warstwa gąbczasta składa się ze źle zorganizowanej tkanki łącznej w lepkim ośrodku. Dominującymi składnikami matrycy tej warstwy są proteoglikany o arbitralnie ukierunkowanym kolagenie i cienkich warstwach elastyny. Łańcuchy boczne cząsteczek proteoglikanów niosą silny ładunek ujemny, co wpływa na ich wysoką zdolność wiązania wody i tworzenia porowatego żelu matrycy. Warstwa gąbczastej matrycy zmniejsza naprężenia mechaniczne w zaworach zastawek serca i utrzymuje ich elastyczność.
Warstwa komorowa jest znacznie cieńsza niż inne i jest pełna elastycznych włókien, które pozwalają tkankom wytrzymać ciągłe odkształcenie. Elastyna ma gąbczastą strukturę, która otacza i łączy włókna kolagenowe i zapewnia ich utrzymanie w stanie neutralnego złożenia. Warstwa wlotowa zaworu (komora dla zastawek tętniczych i gąbczasta dla zastawek przedsionkowo-komorowych) zawiera większą ilość elastyny niż wylot, co zapewnia zmiękczenie uderzenia hydraulicznego podczas zamykania zaworów. Ta zależność między kolagenem i elastyną umożliwia rozszerzenie zaworów do 40% bez trwałego odkształcenia. Pod wpływem małego obciążenia struktury kolagenu tej warstwy są zorientowane w kierunku obciążenia, a jego odporność na dalszy wzrost obciążenia wzrasta.
Tak więc idea zastawek serca jako bezczynności powielania endokardium jest nie tylko uproszczona, ale także w rzeczywistości niepoprawna. Zawory serca to narząd o złożonej strukturze, w tym prążkowane włókna mięśniowe, naczynia krwionośne i limfatyczne oraz elementy nerwowe. Zarówno w swojej strukturze, jak i funkcjonowaniu zawory tworzą jedną całość ze wszystkimi strukturami serca. Analiza normalnej funkcji zaworu musi uwzględniać jego organizację komórkową, a także oddziaływanie komórek między nimi a matrycą. Wiedza zdobyta dzięki takim badaniom prowadzi do projektowania i rozwoju wymiany zastawek za pomocą inżynierii tkankowej.

