Patogenese av hepatitt B
Ostatnia recenzja: 19.11.2021

Cała zawartość iLive jest sprawdzana medycznie lub sprawdzana pod względem faktycznym, aby zapewnić jak największą dokładność faktyczną.
Mamy ścisłe wytyczne dotyczące pozyskiwania i tylko linki do renomowanych serwisów medialnych, akademickich instytucji badawczych i, o ile to możliwe, recenzowanych badań medycznych. Zauważ, że liczby w nawiasach ([1], [2] itd.) Są linkami do tych badań, które można kliknąć.
Jeśli uważasz, że któraś z naszych treści jest niedokładna, nieaktualna lub w inny sposób wątpliwa, wybierz ją i naciśnij Ctrl + Enter.
W patogenezie zapalenia wątroby typu B można wyróżnić kilka wiodących ogniw łańcucha patogenetycznego:
- wprowadzenie patogenu - zakażenie;
- fiksacja na hepatocytach i przenikanie do komórki;
- rozmnażanie wirusa i "pchanie" go na powierzchnię hepatocytów, a także do krwi;
- włączenie reakcji immunologicznych mających na celu wyeliminowanie patogenu;
- immunokompleksowe uszkodzenie narządów i układów;
- tworzenie odporności, uwalnianie z patogenu, regeneracja.
Ponieważ zakażenie wirusem zapalenia wątroby typu B zawsze występuje pozajelitowo, możemy przyjąć, że moment zakażenia jest prawie równy penetracji wirusa do krwi. Próby części naukowców do izolacji w fazie dojelitowej i regionalnej zapalenia wątroby typu B są słabo uziemione. Istnieje więcej powodów, aby sądzić, że w krwiobiegu wirus natychmiast wchodzi do wątroby.
Tropizm wirusa zapalenia wątroby typu B do tkanki wątroby jest wcześniej określony przez obecność w HBsAg specjalnego receptora - polipeptydu o masie cząsteczkowej 31 000 Da (RZ1), który wykazuje aktywność wiązania albuminy. Podobna strefa albuminy znajduje się na błonach hepatocytów ludzkiej wątroby i szympansa niż w istocie i jest określona tropizmem HBV do ludzkiej wątroby i szympansa.
Przy penetracji wirusa są uwalniane do hepatocytów wirusowego DNA, który wchodzi do jądra komórek wątroby i działa jako matryca do syntezy kwasów nukleinowych, wprowadza się szereg kolejnych reakcjach biologicznych, którego wynikiem będzie montaż nukleokapsydu wirusa. Nukleokapsyd migruje przez błonę jądrową do cytoplazmy, gdzie następuje ostateczny montaż cząstek Duńczyka - całkowitego wirusa zapalenia wątroby typu B.
Należy jednak zauważyć, że gdy hepatocyt jest zainfekowany, proces może przebiegać na dwa sposoby - replikacyjny i integracyjny. W pierwszym przypadku rozwija się obraz ostrego lub przewlekłego zapalenia wątroby, aw drugim przypadku wirus przenoszący.
Przyczyny, które predeterminują dwa typy interakcji wirusowego DNA i hepatocytów, nie zostały dokładnie ustalone. Najprawdopodobniej typ reakcji jest określany genetycznie.
W wyniku interakcji się replikacyjne struktury montażowe korovskogo antygenu (w rdzeniu) i cały zespół wirusa (w cytoplazmie), a następnie poprzez przedstawienie kompletnego wirusa lub jego antygeny na błonie lub struktury błon hepatocytów.
Uważa się, że replikacja wirusa nie prowadzi do uszkodzenia komórek na poziomie hepatocytów, ponieważ wirus zapalenia wątroby typu B nie wykazuje efektu cytopatycznego. Taka sytuacja nie może być uznane za pewne, ponieważ opiera się na danych doświadczalnych, że choć nie ma dowodów efektu cytopatycznego wirusa zapalenia wątroby typu B, ale produkowane w hodowli tkankowej, a zatem nie może być w pełni odnieść do wirusowego zapalenia wątroby typu B u ludzi. W każdym razie kwestia braku uszkodzenia hepatocytów podczas fazy replikacji wymaga dodatkowych badań.
Jednak niezależnie od charakteru interakcji wirusa z komórką, wątroba jest następnie włączana do procesu immunopatologicznego. Zatem uszkodzenie hepatocytów, ze względu na fakt, że ekspresja antygenów wirusowych na błonie hepatocytów i wydzielanie antygenów wirusowych u wolnego obwodu cyrkulacyjnej włączone kolejnych komórkowych i humoralnych odpowiedzi immunologicznych skierowanych ostatecznie usunięcie z organizmu ylo wirusów. Proces ten odbywa się w pełnej zgodności z ogólnymi wzorami odpowiedzi immunologicznej w infekcjach wirusowych. Dla eliminacji patogenu obejmują cytotoksycznych odpowiedzi komórkowych, w których pośredniczy różnych klas komórek efektorowych: K-komórek, komórek T, komórek NK, makrofagów. W trakcie tej reakcji jest zniszczenie zakażonych hepatocytów, której towarzyszy uwolnienia antygenów wirusowych (HBcAg, NVeAg HBsAg), sygnał z układu przeciwciała, przy czym specyficzne przeciwciała gromadzą się w krwi, a zwłaszcza krów - antygenowi HBc oraz e - HBeAg . W konsekwencji uwolnienie komórki wątrobowej z wirusa następuje podczas jej śmierci w wyniku reakcji cytolizy komórkowej.
Jednocześnie specyficzne przeciwciała akumulujące się w krwi wiążą antygeny wirusa, tworząc kompleksy immunologiczne fagocytowane przez makrofagi i wydzielane przez nerki. Tak więc nie może być różne immunologicznymi jak uszkodzenie kłębuszków nerkowych, tętnic, bóle stawów, wysypki skórne i inne. Ponieważ udział swoistych przeciwciał oczyszcza organizm z patogenem i jest całkowite wyleczenie.
Zgodnie z patogenezą Powyższe pojęcie zapalenia wątroby typu B Wszystkie różnorodne warianty kliniczne choroby podjęte w celu wyjaśnienia możliwości oddziaływania wirusów i komórek odpornościowych podwykonawców, innymi słowy, siła odpowiedzi immunologicznej na obecność antygenów wirusowych. Według współczesnych pomysłów siła odpowiedzi immunologicznej jest określana genetycznie i związana z antygenami zgodności tkankowej locus HLA pierwszej klasy.
Powszechnie uważa się, że w warunkach odpowiedniej odpowiedzi immunologicznej na antygeny wirusowe opracowano klinicznie ostre zapalenie wątroby o przebiegu cyklicznym i całkowitym wyleczeniu. W przypadku obniżenia odpowiedzi immunologicznej na antygeny, ulegające ekspresji wirusowego immunologiczny cytolizy nieznacznie, tak że nie jest skuteczne eliminowanie zakażonych komórek wątroby, co prowadzi do klinicznych objawów łagodnych przedłużonej trwałości wirusa i może rozwinąć się przewlekłe zapalenie wątroby. W tym przypadku, przeciwnie, w przypadku genetycznie uwarunkowanej silnej odpowiedzi immunologicznej i masywność infekcji (transfuzji krwi) powodują komórek wątrobowych rozległe strefy zniszczenia, które odpowiadają klinicznie ciężkiej i złośliwych postaci choroby.
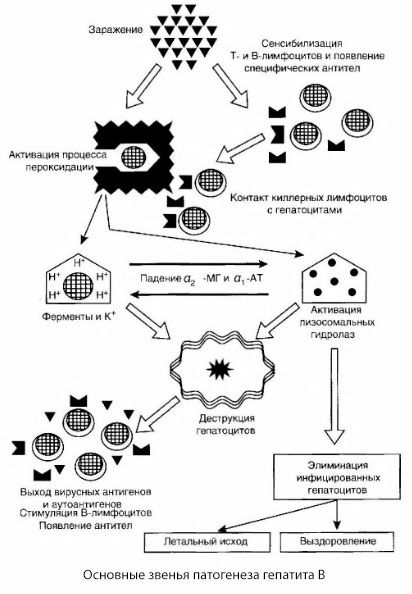
Przedstawiony schemat patogenezy zapalenia wątroby typu B wyróżnia się harmonią, niemniej jednak jest w nim wiele kontrowersyjnych i mało zbadanych momentów.
Jeśli będziemy postępować zgodnie z koncepcją zapalenia wątroby typu B jako choroby immunopatologicznej, możemy spodziewać się wzrostu reakcji cytotoksyczności komórkowej ze wzrostem nasilenia choroby. Jednak w ciężkich postaciach wskaźniki ogniw ogniowych odporności są znacznie zmniejszone, w tym wielokrotny spadek w porównaniu z tymi u zdrowych dzieci i wskaźnik cytotoksyczności komórek K. Gdy postać złośliwą podczas rozwoju masywnej martwicy wątroby i śpiączki wątroby szczególnie wyraźny braku możliwości wybuchu transformacji limfocytów pod wpływem fitogemattlyutinina, Staphylococcus endotoksyny i HBsAg. Ponadto, nie ma możliwości migracji leukocytów według inhibicji migracji leukocytów reakcji (RTML) i wykazały znaczne zwiększenie przepuszczalności błony komórkowej limfocytów z badań im fluorescencyjnej sondy tetracykliny.
Tak więc, jeśli wskaźniki fluorescencji limfocytów zdrowych ludzi wynoszą 9,9 ± 2% i typowo zapalenia wątroby typu B z łagodnym przebiegu unoszą się do 22,3 ± 2,7%, a ilość form fluoryzujących złośliwych limfocytów osiąga przeciętnie 63,5 ± 5,8%. Ponieważ wzrost przepuszczalności błon komórkowych jednoznacznie oceniano w literaturze jako wiarygodny wskaźnik niepełnosprawności funkcjonalnej, można stwierdzić, że wirusowe zapalenie wątroby typu B, w szczególności w postaci złośliwej, uszkodzenie brutto występuje limfocytów. Potwierdzają to również wskaźniki aktywności cytotoksycznej komórek K. W przypadku ciężkiej choroby 1-2 tygodni cytotoksyczności 15,5 ± 8,8%, natomiast w postaci złośliwej 1. Tygodniu - 6,0 ± 2,6, na 2 - 22,0 ± 6,3% norma to 44,8 ± 2,6%.
Przedstawione dane wyraźnie pokazują wyraźne zaburzeniom odporności komórkowej u pacjentów z ostrym zapaleniem wątroby typu B, to jest jasne, że zmiany te występują w czasie, po drugie, w wyniku upadku komórek odpornościowych przez toksyczne metabolity i ewentualnie krążących kompleksów immunologicznych.
Badania wykazały, że u pacjentów z ciężką postacią zapalenia wątroby, zwłaszcza w przypadku masywnej martwicy wątroby, surowica krwi spływającą miano HVsAg i NVeAg i jednocześnie zaczynają być wykrywana w wysokich mian przeciwciał do antygenu powierzchniowego, który jest bardzo niezwykłe dla łagodnej postaci tej choroby, przy który anty-HBV pojawia się tylko w 3-5 miesiącu choroby.
Szybki zanik zapalenia wątroby typu B, antygeny wirusowe, przy jednoczesnym wygląd wysokich mian przeciwciał przeciwwirusowych, co wskazuje na tworzenie się kompleksów immunologicznych a ich możliwy udział w patogenezie masywnej martwicy wątroby.
Zatem rzeczywiste materiały nie pozwalają jednoznacznie interpretować zapalenia wątroby typu B jedynie z punktu widzenia agresji immunopatologicznej. I to nie tylko fakt, że nie można znaleźć zależność między głębokości i rozległości zmian morfologicznych w wątrobie, z jednej strony, a stopień komórkowych czynników odpornościowych - z drugiej. Teoretycznie, fakt ten może być dalej wyjaśnione daty badania odporności komórkowej, komórki odpornościowe, które poddawane są liczne efekty toksyczne ze względu na rosnące funkcjonalnego uszkodzenia wątroby. Można oczywiście założyć, że cytolizy odpornościowy hepatocytów występuje w najwcześniejszych stadiach infekcji, być może nawet przed pojawieniem się objawów klinicznych ciężkiej choroby wątroby. Jednakże, takie założenie jest mało prawdopodobne, ponieważ u pacjentów z ostrym (pioruna) przebiegu choroby ujawniły podobne wskaźniki odporności komórkowej, a ponadto morfologiczny badanie tkanki wątroby nie stwierdzono masowe limfocytarne infiltracji jednocześnie wykrywane stałego pola martwiczych nabłonek bez oznak resorpcji i limfocytowe agresja.
Wyjaśnij obraz morfologiczny w ostrym zapaleniu wątroby tylko z punktu widzenia cytolizy komórek immunologicznych jest bardzo trudny, więc we wczesnych pracach nie wykluczał cytotoksycznego działania wirusa zapalenia wątroby typu B.
Obecnie założenie częściowo potwierdzają odkrycie Studies wirusa zapalenia wątroby typu B, wykazało, że częstość wykrywania markerów wirusowego zapalenia wątroby typu D jest wprost proporcjonalna do stopnia ciężkości choroby: łagodny ich formy znajdują się w 14%, średni - 18 r, ciężkie - 30 złośliwy - u 52% pacjentów. Biorąc pod uwagę, że wirus zapalenia wątroby typu D ma nekrozogennym efekt cytopatyczny, ustalono, że w rozwoju piorunującego zapalenia wątroby typu B form współpracy infekcji wielkie znaczenie wirusy zapalenia wątroby typu B i D.
Patogenezę zapalenia wątroby typu B można przedstawić następująco. Po przeniknięciu wirusa zapalenia wątroby typu B do hepatocytów, wywołuje się atak immunologiczny na zakażone hepatocyty T-killerów, które uwalniają limfotoksyny w kierunku komórek wątroby.
Intymne mechanizmy uszkodzenia hepatocytów w wirusowym zapaleniu wątroby typu B nie zostały dotychczas ustalone. Główną rolę odgrywa aktywowany proces peroksydacji lipidów i hydrolaz lizosomalnych. Punktem wyjściowym mogą być limfotoksyny uwalniane z komórek efektorowych, gdy wchodzą w kontakt z hepatocytami, ale możliwe jest, że sam wirus może być inicjatorem procesów ponownego utleniania. W przyszłości proces patologiczny najprawdopodobniej rozwija się w następującej sekwencji.
- Oddziaływanie czynników agresji (lymphotoxins lub wirusa) z makrocząsteczek biologicznych (ewentualnie ze składnikami retikulum błony siateczki, zdolne do udziału w procesie detoksykacji, przez analogię z innymi czynniki uszkadzające, jak to zostało przedstawione w odniesieniu do czterochlorku węgla).
- Tworzenie wolnych rodników, aktywacja procesów peroksydacji lipidów i wzrost przepuszczalności wszystkich błon wątrobowych (zespół cytolityczny).
- Ruch substancji biologicznie czynnych wzdłuż gradientu stężenia jest utratą enzymów o różnej lokalizacji wewnątrzkomórkowej, dawcach energii, potasu itp. Akumulacja w siarze sodu, wapnia i pH przesuwa się w kierunku kwasicy wewnątrzkomórkowej.
- Aktywacja i wydajność hydrolaz lizosomalnych (RNA-aza, DNA-azy, katepsyn itp.) Wraz z rozpadem komórki wątrobowej i uwalnianiem autoantygenów.
- Stymulacja systemów odpornościowych T i B z wytworzeniem swoistego uczulenia limfocytów T na lipoproteiny wątrobowe, jak również tworzenie autoprzeciwciał humoralnych przeciwko wątrobie.
W zaproponowanym schemacie patogenezie zapalenia wątroby typu B, jako czynnika wyzwalającego to antygeny wirusowe, których intensywne produkty obserwowano w najwcześniejszych stadiach choroby i całego ostrego okresu, z wyjątkiem form złośliwych, w którym wytwarzanie antygenów wirusowych prawie zatrzymuje się na moment masywnej martwicy wątroby, co jest cechą szybka redukcja replikacji wirusa.
Jest również oczywiste, że antygeny wirusowe aktywują odporność na T i B. Podczas tego procesu następuje charakterystyczna redystrybucja subpopulacji limfocytów T, mająca na celu zapewnienie odpowiedniej odpowiedzi immunologicznej, wyeliminowanie zakażonych hepatocytów, neutralizację wirusowych antygenów, sanogenezę i regenerację
W reakcji komórek odpornościowych do antygenów wirusowych na hepatocyty lub membrany w trakcie replikacji wirusa w hepatocytach, istnieją warunki aktywacji peroksydacji lipidów, kontroli, co jest znane, przepuszczalność błon komórkowych i subkomórkowych,
Z tej perspektywy staje się zrozumiałe, że takie naturalne i wysoce charakterystyczne dla wirusowego zapalenia wątroby pojawienie się zespołu cytolizy - zwiększona przepuszczalność błon komórkowych
Ostatecznym wynikiem zespołu cytolizy może być całkowita dysocjacja oksydacyjnej fosforylacji, odpływ materiału komórkowego, śmierć miąższu wątroby.
Jednak w przeważającej większości przypadków procesy te nie przynoszą tak fatalnego rozwoju. Tylko w złośliwych form patologicznego procesu chorobowego występuje lawinowo, a nieodwracalne, ponieważ istnieje ogromne zakażenia, oznaczony proces immunologiczny, nadmierna aktywacja przetwarza overoxidation i lizosomalne zjawiskom gidrodaz autoimmunologiczne agresję.
Takie same mechanizmy zaobserwowano korzystnego przebiegu zapalenia wątroby typu B, jedyną cechę, że są realizowane na jakościowo innym poziomie. W przeciwieństwie do przypadku masywnej martwicy wątroby, korzystnego przebiegu klinicznego zakażonych hepatocytów, oraz obszar stąd immunopatologiczne cytolizy mniej peroksydację lipidów wzmacniany nie jest tak znaczące, aktywacja hydrolaz kwasu prowadzi jedynie do ograniczonego autolizy z nieznacznym uwolnieniem autoantygenów, a co za tym idzie, bez masywnej autoagresji, to znaczy wszystkie etapy patogenezy w sprzyjającym prądzie są przeprowadzane w ramach ciągłej organizacji strukturalnej na renhimy ograniczonej systemy ochronne (przeciwutleniacze, inhibitory, itd) i w związku z tym wątroby i nie ma takiego destrukcyjnego działania.
Przyczyny objawów zatrucia wirusowym zapaleniem wątroby nie są w pełni badane. Propozycję rozróżnienia między tak zwanym pierwotnym, lub wirusowym, zatruciem i wtórnym (metabolicznym lub metabolicznym) można uznać za pozytywne, chociaż nie ujawnia to intymnego mechanizmu występowania ogólnego zespołu toksycznego. Po pierwsze, wirusy zapalenia wątroby nie mają właściwości toksycznych, a po drugie, stężenie wielu metabolitów nie zawsze koreluje z ciężkością choroby i stopniem objawów zatrucia. Wiadomo również, że stężenie wirusowych antygenów nie jest ściśle skorelowane z ciężkości zatrucia. Wręcz przeciwnie, wraz ze wzrostem nasilenia choroby i, w konsekwencji, zwiększeniem stopnia toksyczności, stężenie HBsAg zmniejsza się i jest najniższe w złośliwych postaciach w momencie wystąpienia głębokiej śpiączki wątrobowej. Jednak częstotliwość wykrywania i miana swoistych przeciwciał przeciwwirusowych zależy bezpośrednio od ciężkości choroby.
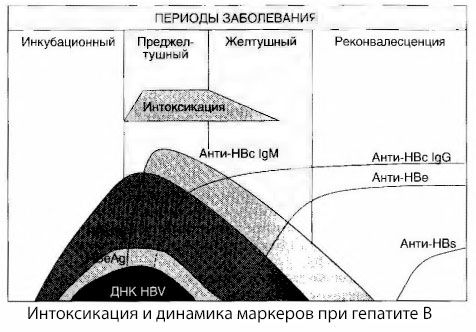
Zatrucie nie pojawia się w czasie rejestracji antygenów wirusowych, a okres obieg środka przeciwwirusowego krwi przeciwciała IgM z antygenem oraz antygenu korovskomu systemu E. Ponadto, gdy ciężkie, a zwłaszcza złośliwych stanowi istotny składnik krwi pacjentów pojawiają się nawet anty-HBs, które typowo nigdy nie zaobserwowano przy łagodnych i umiarkowanych postaciach choroby.
Prezentowane dane pozwalają na stwierdzenie, że toksykozy zespół wirusowego zapalenia wątroby i zapalenia wątroby typu B w szczególności nie powstają w wyniku antygenów wirusowych we krwi i jest wynikiem interakcji antygenów wirusowych z przeciwwirusowe przeciwciała IgM. Rezultatem takiej interakcji, jak wiadomo, jest tworzenie kompleksów immunologicznych i ewentualnie aktywnych substancji toksycznych.
Objawy zatrucia występują w momencie pojawienia się kompleksów immunologicznych w swobodnym krążeniu, ale w przyszłości nie można prześledzić takiej korelacji.
Częściowe wyjaśnienie tego można znaleźć w badaniu składu kompleksów immunologicznych. U pacjentów z ciężką krążyć krwi systemy przeważnie średnich i ich kompozycji w wysokości toksycznych zespołem zdominowane klas przeciwciał, podczas gdy w cofnięciu, oraz objawy kliniczne systemów odzyskiwania stają się większe, i zaczyna dominować w skład przeciwciał IgG.
Przedstawione dane dotyczą mechanizmów rozwoju zespołu toksycznego w początkowym okresie choroby, ale z toksykozą występującą na wysokości objawów klinicznych, mają one tylko częściowe znaczenie, a zwłaszcza w rozwoju śpiączki wątrobowej.
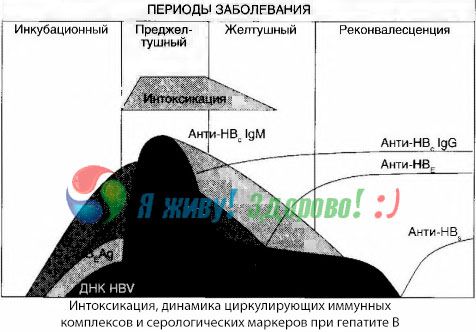
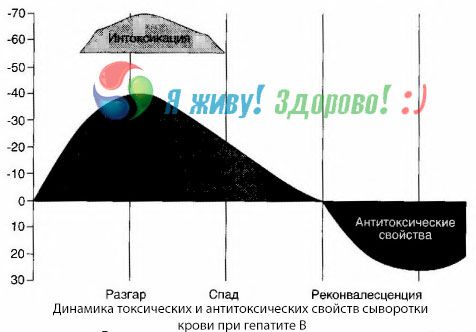
Za pomocą metody hekultur udało się wykazać, że w wirusowym zapaleniu wątroby typu B krew stale gromadzi toksyny uwalniane z uszkodzonej, rozkładającej się tkanki wątrobowej. Stężenie tych toksyn jest proporcjonalne do ciężkości choroby, mają one charakter białkowy.
W okresie rekonwalescencji przeciwciała przeciwko tej toksynie pojawiają się we krwi; ale w przypadku śpiączki wątrobowej stężenie toksyny we krwi gwałtownie wzrasta, a przeciwciała we krwi nie są wykrywane.
Patomorfologia zapalenia wątroby typu B
Ze względu na zmiany morfologiczne istnieją trzy formy ostrego zapalenia wątroby typu B:
- forma cykliczna,
- masywna martwica wątroby;
- cholestatyczne pericholangiolityczne zapalenie wątroby.
Gdy cykliczne forma zapalenia wątroby typu B, zwyrodnieniowe zmiany zapalne, proliferacyjne i były bardziej wyraźne w płacikach w centrum, a zapalenie wątroby typu A są umieszczone na obwodzie w plastry, rozprzestrzenia się do środka. Różnice te tłumaczy się różnymi sposobami przenikania wirusa do miąższu wątroby. Wirus zapalenia wątroby typu przechodzi przez wątrobę do żyły wrotnej i rozciąga się w środku płatów, wirus zapalenia wątroby typu B wpływa do tętnicy wątrobowej i kapilary rozgałęzienia równomierne dostarczanie wszystkich odcinków, aż do ich środka.
Stopień porażenia miąższu wątroby w większości przypadków odpowiada nasileniu objawów klinicznych choroby. W łagodniejszych form zwykle obserwuje ogniskową martwicę hepatocytów i w umiarkowanych i ciężkich formach - strefowo martwicy (ze skłonnością do tworzenia się mostków fuzyjnych i martwicy ostre formy choroby).
Największe zmiany morfologiczne w miąższu obserwuje się na wysokości objawów klinicznych, co zwykle pokrywa się z pierwszą dekadą choroby. Podczas drugiej, a zwłaszcza trzeciej dekady, procesy intensyfikacji są zintensyfikowane. W tym czasie zmiany nekrobiotyczne prawie całkowicie zanikają, a procesy infiltracji komórkowej z powolnym późniejszym przywróceniem struktury płytek komórek wątrobowych zaczynają dominować. Jednak całkowite przywrócenie struktury i funkcji miąższu wątroby występuje tylko 3 do 6 miesięcy po wystąpieniu choroby, a nie u wszystkich pacjentów.
Ogólny charakter zakażenia wirusowym zapaleniem wątroby typu B potwierdza się po wykryciu HBsAg nie tylko w hepatocytach, ale także w nerkach, płucach, śledzionie, trzustce, komórkach szpiku kostnego itp.
Cholestatyczne (periholangiolitichesky) zapalenie wątroby - szczególną postać tej choroby, przy czym największe zmiany morfologiczne są wykrywane przez wewnątrzwątrobowych dróg żółciowych, a także z periholangiolita obraz holangiolita. W postaci cholestatycznej rozwija się cholestaza z powiększeniem żółciowych naczyń włosowatych z zastojem żółci w nich, z proliferacją cholangiol i naciekami komórek wokół nich. Komórki wątrobowe z tą postacią zapalenia wątroby są nieznacznie zmienione. Klinicznie choroba charakteryzuje się przedłużonym przebiegiem z przedłużoną żółtaczką. Wykazano, że przyczyną tak szczególnego przebiegu choroby jest dominujący wpływ wirusa na ściany cholangiolu z niewielkim wpływem na hepatocyty.

