Ekspert medyczny artykułu
Nowe publikacje
przedwczesna ciąża
Ostatnia recenzja: 04.07.2025

Cała zawartość iLive jest sprawdzana medycznie lub sprawdzana pod względem faktycznym, aby zapewnić jak największą dokładność faktyczną.
Mamy ścisłe wytyczne dotyczące pozyskiwania i tylko linki do renomowanych serwisów medialnych, akademickich instytucji badawczych i, o ile to możliwe, recenzowanych badań medycznych. Zauważ, że liczby w nawiasach ([1], [2] itd.) Są linkami do tych badań, które można kliknąć.
Jeśli uważasz, że któraś z naszych treści jest niedokładna, nieaktualna lub w inny sposób wątpliwa, wybierz ją i naciśnij Ctrl + Enter.
Ciąża po terminie należy do problemów, które tradycyjnie budzą duże zainteresowanie naukowe i praktyczne, spowodowane przede wszystkim niekorzystnymi wynikami okołoporodowymi w tej patologii.
W położnictwie krajowym uważa się, że ciąża po terminie, trwająca ponad 287–290 dni, wiąże się z wewnątrzmacicznym cierpieniem płodu i kończy się urodzeniem dziecka z objawami biologicznej naddojrzałości, co determinuje wysokie ryzyko wystąpienia zespołu stresu przedporodowego i wewnątrzporodowego oraz trudnej adaptacji noworodka.
Epidemiologia
Częstość występowania ciąży po terminie wynosi około 7% wszystkich ciąż (Martin i in., 2007).
American College of Obstetricians and Gynecologists definiuje ciążę po terminie jako taką, która trwa dłużej niż 42 tygodnie (294 dni). Jej częstość występowania wynosi średnio około 10%. W większości krajów europejskich ciąża po terminie jest definiowana jako taka, która trwa 294 dni lub dłużej, z wyjątkiem Portugalii (287 dni lub więcej) i Irlandii (292 dni lub więcej). Częstość występowania ciąży po terminie w Europie wynosi około 3,5–5,92%.
Jednocześnie dziecko z objawami przekwitania nie zawsze rodzi się z przekwitaniem, wręcz przeciwnie, objawy przekwitania można zauważyć u płodu urodzonego przed upływem 290 dni ciąży, co prawdopodobnie wynika z indywidualnego czasu i cech rozwoju ciąży. Jednak stan funkcjonalny płodu przekwitającego zasługuje na większą uwagę, biorąc pod uwagę wysoką częstość występowania tak poważnych powikłań, jak zespół aspiracji smółki, niedotlenieniowo-niedokrwienne uszkodzenie ośrodkowego układu nerwowego, mięśnia sercowego, nerek, jelit, prowadzące do śmierci płodu przed i wewnątrzporodowej.
Ciąża po terminie jest uważana za czynnik zwiększający częstość powikłań podczas porodu i prowadzący do wzrostu zachorowalności i śmiertelności okołoporodowej. Najbardziej typowymi powikłaniami okołoporodowymi ciąży po terminie są martwe urodzenie, uduszenie i uraz okołoporodowy. E. Ya. Karaganova, IA Oreshkova (2003), przeprowadzając dokładną analizę wyników okołoporodowych u 499 pacjentek z ciążą po terminie w zależności od wieku ciążowego, stwierdziły, że wraz ze wzrostem wieku ciążowego z 41 do 43 tygodnia, odsetek zachorowalności okołoporodowej wzrasta. Tak więc w 43 tygodniu ciąży częstość niedotlenieniowo-niedokrwiennego uszkodzenia ośrodkowego układu nerwowego wzrasta 2,9 razy, uduszenia - 1,5 razy, zespołu aspiracji - 2,3 razy w porównaniu do noworodków urodzonych o czasie z wiekiem ciążowym nie dłuższym niż 41 tydzień. W przypadku ciąży trwającej powyżej 41. tygodnia objawy zagrożenia płodu przed rozpoczęciem porodu stwierdzono u 67,1% płodów (u połowy z nich w przypadku ciąży trwającej 42–43 tydzień), domieszkę smółki w płynie owodniowym – u 31,6%, małowodzie – u 50,9% pacjentek.
Przyczyny przedwczesna ciąża
Najczęstszą przyczyną ciąży po terminie jest niedokładne datowanie (Neilson, 2000; Crowley, 2004). Stosowanie standardowych kryteriów klinicznych do określania szacowanej daty porodu (EDD) ma tendencję do zawyżania wieku ciążowego, a tym samym zwiększa częstość występowania ciąży po terminie (Gardosi i in., 1997; Taipale i Hiilermaa, 2001). Kryteria kliniczne powszechnie stosowane do potwierdzenia wieku ciążowego obejmują ostatnią miesiączkę (LMP), wielkość macicy ocenianą za pomocą badania bimanualnego w pierwszym trymestrze, percepcję ruchów płodu, osłuchiwanie tonów serca płodu i wysokość dna macicy. ciąża pojedyncza.
Jeśli dojdzie do ciąży po terminie, przyczyna jest zwykle nieznana.
Czynniki ryzyka
Analizując wywiad somatyczny, położniczy i ginekologiczny oraz charakterystykę obecnej ciąży, zwraca się uwagę na czynniki ryzyka, które wskazują na możliwość wystąpienia ciąży po terminie i przedłużonej.
Czynniki ryzyka ciąży po terminie:
- kobieta w ciąży ma ponad 30 lat;
- historia chorób przenoszonych drogą płciową (STI) i przewlekłych chorób zapalnych przydatków macicy;
- wskazanie historii opóźnień w dostawie;
- „niedojrzała” lub „niewystarczająco dojrzała” szyjka macicy w 40. tygodniu ciąży lub później.
Czynniki ryzyka przedłużonej ciąży:
- wiek kobiety ciężarnej wynosi od 20 do 30 lat;
- dysfunkcja jajników z nieregularnym lub przedłużonym (≥ 35 dni) cyklem miesiączkowym;
- rozbieżność między wiekiem ciążowym ustalonym na podstawie pierwszego dnia ostatniej miesiączki a badaniem USG.
Do ogólnych czynników ryzyka zalicza się pierworództwo, wcześniejszą ciążę po terminie (Alfirevic i Walkinshaw, 1994; Mogren i in., 1999; Olesen i in., 1999), płód męski (Divon i in., 2002), otyłość (Usha Kiran i in., 2005; Stotland i in., 2007), czynniki hormonalne i predyspozycje genetyczne (Laursen i in., 2004).
Nie wiadomo, jak wskaźnik masy ciała (BMI) wpływa na czas trwania ciąży i termin porodu, ale co ciekawe, kobiety otyłe częściej doświadczają ciąży po terminie (Usha Kiran i in., 2005), podczas gdy kobiety z niskim BMI mają większe ryzyko ciąży po terminie i porodu przedwczesnego (poród przed 37. tygodniem ciąży) (Hickey i in., 1997). Ponieważ tkanka tłuszczowa jest hormonalnie aktywna (Baranova i in., 2006), a kobiety otyłe mogą mieć zmieniony status metaboliczny, możliwe jest, że czynniki endokrynologiczne zaangażowane w początek porodu są zmienione u kobiet otyłych.
Czynniki genetyczne mogą być związane z przedłużeniem ciąży. Kobiety, które same były w ciąży po terminie, mają większe ryzyko ciąży po terminie (względne ryzyko 1,3) (Mogren i in., 1999). Kobiety, które były w ciąży po terminie, mają zwiększone ryzyko kolejnej ciąży po terminie (27% w przypadku jednej ciąży po terminie i 39% w przypadku dwóch wcześniejszych przedłużonych ciąż) (Kistka i in., 2007).
Patogeneza
Patogeneza ciąży po terminie nie jest w pełni poznana. Jak pokazano powyżej, zidentyfikowano niektóre czynniki ryzyka związane z ciążą po terminie wraz z możliwymi wyjaśnieniami, jednak patogeneza tego stanu nie jest jeszcze jasna. Pomimo poprawy zrozumienia porodu w ostatnich latach, nadal brakuje nam jasności co do dokładnych mechanizmów, które inicjują poród i promują jego postęp. Aby lepiej zrozumieć patogenezę ciąży po terminie, ważne jest, aby rzucić światło na patofizjologię porodu i spróbować zrozumieć, dlaczego te mechanizmy nie są wyzwalane w ciąży po terminie lub odwrotnie, są wyzwalane wcześniej w porodzie przedwczesnym. Wydaje się logiczne, że istnieje rzeczywiście wspólna podstawa lub związek między tymi trzema stanami. Mechanizmy porodu obejmują interakcję między procesami hormonalnymi, mechanicznymi i zapalnymi, w których łożysko, matka i płód odgrywają kluczową rolę.
Produkcja peptydu uwalniającego kortykotropinę (CRH) przez łożysko jest związana z czasem trwania ciąży (McLean i in., 1995). Synteza CRH przez łożysko wzrasta wykładniczo w miarę postępu ciąży i osiąga szczyt w momencie porodu. Kobiety rodzące przedwcześnie mają szybszy wykładniczy wskaźnik wzrostu niż kobiety rodzące w terminie, podczas gdy kobiety rodzące później mają wolniejszy wskaźnik wzrostu (Ellis i in., 2002; Torricelli i in., 2006). Dane te sugerują, że poród po terminie jest spowodowany zmienionymi mechanizmami biologicznymi regulującymi czas trwania ciąży. Może to być spowodowane dziedziczną predyspozycją wynikającą z polimorfizmów w genach w fizjologicznej ścieżce łączącej CRH z porodem. Możliwe jest również, że fenotyp matki może zmieniać odpowiedź tkanek matki na normalne sygnały hormonalne w momencie porodu, co może mieć miejsce u kobiet otyłych.
CRH może bezpośrednio stymulować nadnercza płodu do produkcji DHEA, prekursora syntezy estriolu przez łożysko (Smith i in., 1998). Stężenia CRH w osoczu matki korelują ze stężeniami estriolu (Smith i in., 2009). Wzrost estriolu wywołany przez CRH wzrasta szybciej niż poziom estradiolu w późnej ciąży, co skutkuje zwiększonym stosunkiem estriolu do estradiolu, który uważa się za tworzący środowisko estrogenne w ostatnich tygodniach ciąży. Jednocześnie wzrost progesteronu w osoczu matki, który występuje w czasie ciąży, spowalnia lub nawet zmniejsza się w późnej ciąży. Może to być spowodowane hamowaniem przez CRH syntezy progesteronu przez łożysko (Yang i in., 2006). Tak więc efekt progesteronu promujący ciążę (promujący rozluźnienie) zmniejsza się wraz ze wzrostem efektu estriolu promującego poród (promującego skurcze macicy). Te zmiany w proporcjach obserwowano w przypadku ciąż wcześniaczych, donoszonych pojedynczych i bliźniaczych (Smith i in., 2009). Sytuacja w przypadku ciąż po terminie jest nieznana.
Objawy przedwczesna ciąża
Zespół objawów przejrzałego płodu został po raz pierwszy opisany przez Ballantyne'a (1902) i Runge'a (1948), dlatego nazywa się go zespołem Ballantyne'a-Runge'a, obejmującym brak serowatego tłuszczu, suchość i macerację skóry noworodka (stopy „kąpielowe”, dłonie), a także w pachwinach i fałdach pachowych, długie paznokcie, gęste kości czaszki, wąskie szwy i zmniejszone rozmiary ciemiączek, zielonkawe lub żółtawe zabarwienie skóry, błon płodowych, pępowiny. Inne obserwacje wskazują na przedłużoną ciążę.
Przedłużona ciąża, trwająca ponad 287 dni, nie wiąże się z cierpieniem płodu i kończy się urodzeniem zdrowego dziecka bez oznak przerostu. Tak więc przedłużona ciąża jest uważana za stan fizjologiczny, mający na celu ostateczne dojrzewanie płodu.
Komplikacje i konsekwencje
Ciąża po terminie wiąże się ze zwiększoną mobilnością i zachorowalnością płodu i noworodka, a także zachorowalnością matki. Ryzyko to jest większe niż pierwotnie sądzono. W przeszłości ryzyko było niedoszacowane z dwóch powodów. Po pierwsze, wcześniejsze badania dotyczące ciąży po terminie zostały opublikowane, zanim badanie ultrasonograficzne stało się rutynową metodą definiowania ciąży. W rezultacie wiele ciąż uwzględnionych w badaniach nie było w rzeczywistości ciążami po terminie. Drugi powód jest związany z samą definicją urodzenia martwego dziecka. Wskaźniki urodzeń martwych tradycyjnie obliczano na podstawie ciąż urodzonych w danym wieku ciążowym, a nie trwających (nienarodzonych) ciąż. Zmniejszy to wskaźnik urodzeń martwych dzieci w ciążach po terminie, ponieważ po urodzeniu płód nie jest już narażony na wewnątrzmaciczną śmierć płodu (IUFD). Właściwym mianownikiem nie są zatem wszystkie urodzenia w danym wieku ciążowym, lecz trwające (nienarodzone) ciąże (Rand i in., 2000; Smith, 2001; Caughey i in., 2003).
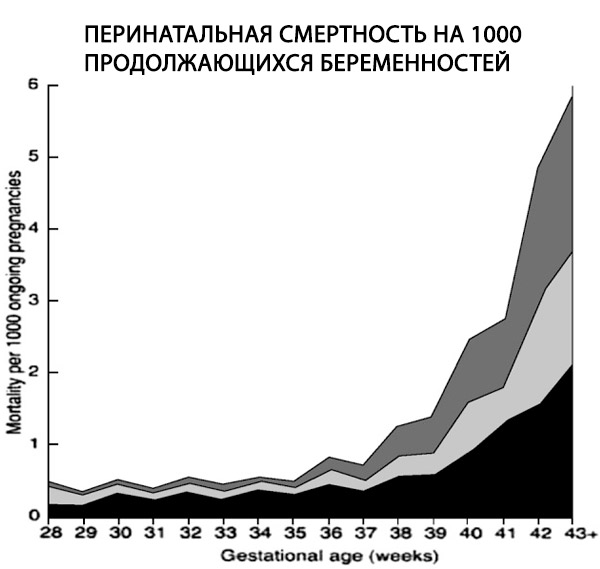
Jedno retrospektywne badanie obejmujące ponad 170 000 urodzeń pojedynczych, przeprowadzone przy użyciu odpowiedniego mianownika, wykazało 6-krotny wzrost wskaźnika urodzeń martwych w przypadku ciąż po terminie, z 0,35 do 2,12 na 1000 trwających ciąż (Hilder i in., 1998).
Powikłania u płodu i noworodka
Śmiertelność okołoporodowa, definiowana jako martwe urodzenia plus wczesne zgony noworodków, jest dwukrotnie wyższa w 42. tygodniu ciąży niż w terminie (odpowiednio 4–7 w porównaniu z 2–3 na 1000 urodzeń). Zwiększa się czterokrotnie w 43. tygodniu i pięciokrotnie do siedmiokrotnie w 44. tygodniu (Bakketeig i Bergsjo, 1989; Feldman, 1992; Hilder i in., 1998; Cotzias i in., 1999). Dane te pokazują również, że w przeliczeniu na 1000 trwających ciąż wskaźniki śmiertelności płodów i noworodków gwałtownie rosną po 40. tygodniu (Hilder i in., 1998) (Hilder i in., 1998).
Za główne przyczyny zwiększonej śmiertelności okołoporodowej w tych przypadkach uważa się niewydolność maciczno-łożyskową, zachłyśnięcie się smółką i zakażenie wewnątrzmaciczne (Hannah, 1993).
Zachorowalność płodów jest również zwiększona w ciążach po terminie i ciążach trwających dłużej niż 41 tygodni. Obejmuje to pasaż smółki, zespół aspiracji smółki, makrosomię i dysmaturię. Ciąża po terminie jest również niezależnym czynnikiem ryzyka niskiego pH pępowiny (kwasica noworodkowa), niskich wyników w skali Apgar w 5. minucie (Kitlinski i in., 2003), encefalopatii noworodkowej (Badawi i in., 1998) i śmiertelności niemowląt w pierwszym roku życia (Hilder i in., 1998; Cotzias i in., 1999; Rand i in., 2000). Chociaż niektóre z tych zgonów niemowląt są wyraźnie wynikiem powikłań okołoporodowych, takich jak zespół aspiracji smółki, większość z nich ma nieznaną przyczynę.
Około 20% płodów po terminie ma zespół niedojrzałości, który odnosi się do noworodków z cechami przypominającymi przewlekłe wewnątrzmaciczne zahamowanie wzrostu z powodu niewydolności maciczno-łożyskowej (Vorherr, 1975; Mannino, 1988). Należą do nich cienka, pomarszczona, łuszcząca się skóra (nadmierne łuszczenie), szczupła budowa ciała (niedożywienie), długie włosy i paznokcie, małowodzie i częste wydalanie smółki. U tych kobiet w ciąży występuje zwiększone ryzyko ucisku pępowiny z powodu małowodzia, aspiracji smółki i krótkotrwałych powikłań noworodkowych, takich jak hipoglikemia, drgawki i niewydolność oddechowa.
Ryzyko dla matek
Ciąża po terminie wiąże się ze znacznym ryzykiem dla matki. Ryzyko jest zwiększone:
- dystocja porodowa (9-12% w porównaniu do 2-7% w terminie);
- poważne pęknięcia krocza (pęknięcia III i IV stopnia) związane z makrosomią (3,3% w porównaniu do 2,6% w terminie porodu);
- poród drogą pochwową; i
- podwojenie wskaźnika cięć cesarskich (CS) (14% w porównaniu z 7% w terminie) (Rand i in., 2000; Campbell i in., 1997; Alexander i in., 2000; Treger i in., 2002).
Cięcie cesarskie wiąże się z większą częstością występowania zapalenia błony śluzowej macicy, krwawień i chorób zakrzepowo-zatorowych (Alexander i in., 2001; Eden i in., 1987).
Podobnie jak w przypadku noworodków, zachorowalność matek również wzrasta wraz z ciążą donoszoną do 42. tygodnia ciąży. Powikłania takie jak zapalenie błon płodowych, poważne pęknięcia krocza, cesarskie cięcie, krwotok poporodowy i zapalenie mięśnia macicy nasilają się po 39. tygodniu ciąży (Yoder i in., 2002; Caughey i Bishop, 2006; Heimstad i in., 2006; Caughey i in., 2007; Bruckner i in., 2008;).
Diagnostyka przedwczesna ciąża
Tradycyjna diagnostyka ciąży po terminie polega na odpowiednim obliczeniu wieku ciążowego. Jednocześnie najdokładniejsze metody na obecnym etapie obejmują obliczenia oparte na pierwszym dniu ostatniej miesiączki oraz na danych z badania USG z 7. do 20. tygodnia ciąży. Wielu autorów uważa te dwie metody za równoważne. Jednak niektórzy badacze sugerują, aby przy określaniu wieku ciążowego w ciąży po terminie opierać się wyłącznie na danych biometrycznych USG. Wśród czynników ryzyka ciąży po terminie wyróżnia się szereg cech wywiadu somatycznego, położniczego i ginekologicznego oraz przebiegu obecnej ciąży.
Z wywiadu somatycznego wielu autorów podkreśla wiek rodziców powyżej 30 lat, obecność patologii pozagenitalnej u matki. Wśród cech wywiadu położniczo-ginekologicznego należy zwrócić uwagę na zaburzenia miesiączkowania, obecność poronień i poronień samoistnych, choroby zapalne przydatków macicy, historię późnych porodów i 3 lub więcej zbliżających się porodów.
Diagnostyka laboratoryjna ciąży po terminie
W miarę wydłużania się okresu ciąży po terminie następuje stopniowe wyczerpywanie się układu kallekreina-kinina, co objawia się skrajnie niską zawartością kininogenu (0,25–0,2 μg/ml, przy N=0,5 μg/ml), niską aktywnością kallekreiny i jej inhibitorów oraz spontaniczną aktywnością esterazy w osoczu krwi po 41. tygodniu ciąży.
W ciąży po terminie obserwuje się nasilenie procesów peroksydacji lipidów zarówno w organizmie kobiety ciężarnej, jak i płodu, co przyczynia się do zahamowania enzymów wiążących błony struktur subkomórkowych. W rezultacie funkcje detoksykacyjne i energetyczne są znacznie upośledzone, a w konsekwencji następuje akumulacja toksycznych metabolitów egzogennych i endogennych, rozwija się endotoksemia, postępująca wraz z wydłużaniem się okresu ciąży. Nasilenie endotoksemii można ocenić na podstawie pojemności sorpcyjnej erytrocytów oraz stężenia białek średniocząsteczkowych. Wzrost peroksydacji i zatrucia endogennego koreluje z ciężkością niedotlenienia płodu.
Ciąża po terminie charakteryzuje się niskim poziomem prostaglandyny F2α, która jest syntetyzowana w błonie doczesnej i mięśniu macicy i jest głównym modulatorem rozwoju porodu.
W przypadku ciąży trwającej powyżej 41 tygodni obserwuje się wzrost lepkości osocza, stężenia kwasu moczowego oraz zmniejszenie stężenia fibrynogenu, antytrombiny III i liczby płytek krwi. Stężenie fibronektyny płodowej > 5 ng/ml w wydzielinie szyjkowo-pochwowej u kobiet z ciążą trwającą powyżej 41 tygodni wskazuje na wysoką biologiczną gotowość organizmu do porodu i jego samoistne rozpoczęcie w ciągu następnych 3 dni. Czułość i swoistość tej metody wynoszą odpowiednio 71 i 64%.
Niezwykle ważne jest badanie cech stanu funkcjonalnego kompleksu płodowo-łożyskowego i płodu w ciąży po terminie (badania ultrasonograficzne, dopplerowskie i kardiotokograficzne). Podczas badania echograficznego wykonuje się fetometrię w celu określenia szacunkowej masy płodu i oceny jego rozwoju anatomicznego. W 12,2% przypadków wykrywa się IUGR I–II stopnia, co nie różni się istotnie od częstości wykrywania zespołu w przedłużonej ciąży. Jednocześnie w 80% przypadków wykryliśmy postać asymetryczną, a w 20% postać symetryczną. Ciąża po terminie charakteryzuje się wykryciem echograficznych objawów wyraźnych zmian inwolucyjno-dystroficznych (GIII z petryfikacjami). Średnia wartość wskaźnika objętości płynu owodniowego w grupie ciąży po terminie wyniosła 7,25±1,48, typowa dla ciąży po terminie jest detekcja zmniejszonej ilości płynu owodniowego.
Badanie Dopplera
Najważniejszym czynnikiem prognozowania wyników okołoporodowych jest określenie stopnia zaburzeń hemodynamicznych płodu w czasie ciąży po terminie.
- Stopień I - zaburzenie przepływu krwi wewnątrzłożyskowej i płodowo-łożyskowej. Na tym etapie nie występują zaburzenia hemodynamiki tętniczej i żylnej płodu. Obserwuje się wzrost oporu naczyniowego w tętnicy pępowinowej i jej odgałęzieniach końcowych, a także w tętnicach spiralnych. Wskaźniki składu gazowego i równowagi kwasowo-zasadowej krwi pępowinowej mieszczą się w granicach normy.
- Stadium II - centralizacja krążenia krwi płodu. Hipoksemia jest zauważalna we krwi noworodka przy urodzeniu. Na tym etapie rozróżnia się dwa kolejne stadia.
- IIa - początkowe objawy centralizacji krążenia tętniczego płodu przy niezmienionym przepływie krwi żylnej i wewnątrzsercowej, charakteryzujące się:
- spadek oporu w tętnicy środkowej mózgu (nie więcej niż o 50%) lub wzrost oporu naczyniowego w aorcie;
- obniżenie wskaźnika CPC (do 0,9);
- wzrost oporu w tętnicach nerkowych płodu nie większy niż 25% normy.
- IIb - umiarkowanie wyrażona centralizacja krążenia krwi z upośledzonym przepływem krwi w przewodzie żylnym i zwiększonym przepływem krwi na zastawce aorty. Na tym etapie wykrywa się:
- jednoczesny wzrost oporu naczyniowego w aorcie i spadek oporu w tętnicy mózgowej środkowej;
- spadek CPC;
- wzrost średniej prędkości przepływu krwi (Tamx) w przewodzie żylnym;
- wzrost średniej liniowej i objętościowej prędkości przepływu krwi przez zastawkę aorty.
- IIa - początkowe objawy centralizacji krążenia tętniczego płodu przy niezmienionym przepływie krwi żylnej i wewnątrzsercowej, charakteryzujące się:
- Stopień III - wyraźna centralizacja krążenia płodowego z upośledzonym odpływem żylnym i dekompensacją hemodynamiki centralnej i wewnątrzsercowej. W krwi pępowinowej noworodka przy urodzeniu stwierdza się hipoksemię połączoną z kwasicą i hiperkapnią. Wskaźniki dopplerometryczne na tym etapie charakteryzują się:
- spadek oporu naczyniowego w tętnicy krezkowej dolnej o ponad 50% normy, spadek CPC poniżej 0,8;
- postępujący wzrost oporu naczyniowego w aorcie i tętnicach nerkowych o ponad 80%;
- w przewodzie żylnym - wzrost wskaźnika S/A, PIV (powyżej 0,78) i spadek Tamx;
- w żyle głównej dolnej - wzrost wskaźników PIV, IPI i %R (powyżej 36,8%);
- w żyłach szyjnych - wzrost wskaźnika S/A, PIV (powyżej 1,1) i spadek Tamx;
- zmniejszenie średniej prędkości liniowej i objętościowej na zastawkach aorty i pnia płucnego;
- przyspieszone tętno, zmniejszona objętość wyrzutowa, objętość końcowoskurczowa i końcoworozkurczowa lewej komory oraz rzut serca.
Zidentyfikowane stadia zmian hemodynamicznych płodu odzwierciedlają stały postęp zaburzeń jego stanu czynnościowego w warunkach przewlekłego niedotlenienia wewnątrzmacicznego w czasie ciąży po terminie. Gdy hipoksemia połączona z hiperacidemią i hiperkapnią zostanie wykryta we krwi pępowinowej noworodka, częstość niekorzystnych wyników okołoporodowych jest 4,8 razy wyższa w porównaniu z grupą z izolowaną hipoksemią. W konsekwencji, hiperacidemia i hiperkapnia odzwierciedlają wyraźne zaburzenia metaboliczne płodu i postępujące pogorszenie jego stanu w warunkach przewlekłego niedotlenienia w czasie ciąży po terminie.
Kardiotokografia
Podczas przeprowadzania tej metody w stadium I wykrywa się początkowe objawy przewlekłego niedotlenienia wewnątrzmacicznego (20,93%) i umiarkowanego niedotlenienia płodu (6,97%). W stadium IIa częstość początkowych objawów niedotlenienia płodu wzrasta 2-krotnie, przy niedotlenieniu umiarkowanym – 4,13-krotnie. W stadium IIb częstość umiarkowanego i ciężkiego niedotlenienia płodu wzrasta znacząco. W stadium III wykrywa się tylko ciężkie (65,1%) i umiarkowane (30,2%) niedotlenienie płodu.
Program badań przesiewowych kobiet w ciąży obejmuje:
- identyfikacja kobiet ciężarnych zagrożonych ciążą po terminie;
- fetometria ultrasonograficzna z oceną oznak dojrzałości noworodka;
- ocena ilości i jakości płynu owodniowego;
- ocena stopnia dojrzałości łożyska;
- kardiotokografia;
- ocena hemodynamiki płodu (tętnica środkowa mózgu, aorta, przewód żylny, żyła główna dolna);
- ocena profilu biofizycznego płodu;
- ocena dojrzałości szyjki macicy;
- amnioskopia.
Jak zbadać?
Diagnostyka różnicowa
Podczas kompleksowego badania kobiet z przedłużoną ciążą ujawnia się:
- w 26,5% obserwacji - II stopień, w 51,8% - III stopień dojrzałości łożyska;
- w 72,3% obserwacji - prawidłowa ilość płynu owodniowego;
- w 89,2% obserwacji - prawidłowe wskaźniki przepływu krwi płodowo-łożyskowej i w 91,6% - prawidłowy wskaźnik mózgowo-łożyskowy;
- w 100% obserwacji – prawidłowe wskaźniki centralnej hemodynamiki płodu, jego przepływu krwi przezzastawkowego i żylnego;
- spadek CPC przy prawidłowych wskaźnikach przepływu krwi przez łożysko i płod, wskazuje na obecność nieprawidłowości w stanie czynnościowym płodu i jest charakterystyczny dla IUGR, zakażenia wewnątrzmacicznego i przewlekłego niedotlenienia płodu.
Z kim się skontaktować?
Leczenie przedwczesna ciąża
Dokładne datowanie ciąży ma kluczowe znaczenie dla diagnozy i leczenia ciąży po terminie (Mandruzzato i in., 2010). Ostatnia miesiączka była tradycyjnie używana do obliczania przewidywanej daty porodu (EDD). Jednak wiele niedokładności może występować z powodu nieregularności cyklu, niedawnego stosowania antykoncepcji hormonalnej lub krwawienia we wczesnej ciąży.
Wykazano, że rutynowe badanie ultrasonograficzne w celu wykrycia ciąży zmniejsza liczbę fałszywie dodatnich diagnoz, a tym samym ogólny wskaźnik ciąż po terminie z 10–15% do około 2–5%, minimalizując w ten sposób konieczność przeprowadzenia niepotrzebnych interwencji (Bennett i in., 2004; Caughey i in., 2008a; 2009).
Celem leczenia ciąży po terminie jest: korekcja zaburzeń hemodynamicznych płodu, zapobieganie rozwojowi płodu w czasie porodu, przygotowanie kanału rodnego do porodu, indukcja porodu.
Wskazania do hospitalizacji
Przekroczenie wieku ciążowego o 40 tygodni i 3 dni przy precyzyjnie wyliczonym terminie porodu, występowanie czynników ryzyka ciąży po terminie oraz niedostateczne przygotowanie kanału rodnego.
Leczenie farmakologiczne ciąży po terminie
W celu poprawy stanu płodu w okresie ciąży po terminie stosuje się preparat hesobendin + etamivan + etofilin (instenon) - lek złożony o działaniu neuroprotekcyjnym, opierającym się na wzajemnym potencjale działania jego składników.
Wskazania do stosowania leku hesobendin + etamivan + etofilina:
- upośledzenie przepływu krwi w tętnicy pępowinowej płodu (SDO > 2,7, IR > 0,65);
- obniżenie współczynnika mózgowo-łożyskowego (CPC < 1,10);
- wstępne objawy centralizacji krążenia płodowego;
- wstępne objawy niedotlenienia płodu według danych CTG. Wymienione czynniki wskazujące na wstępne objawy zagrożenia płodu nie wymagają porodu w trybie nagłym, ale wskazują na konieczność skorygowania jego stanu poprzez zwiększenie zdolności adaptacyjnych mózgu płodu w trakcie porodu.
Przygotowanie do porodu w ciąży po terminie
Mechaniczne metody drażnienia szyjki macicy:
- Oderwanie dolnego bieguna pęcherza płodowego. Oderwanie dolnego bieguna pęcherza płodowego może również prowadzić do zwiększonej syntezy prostaglandyn i „dojrzewania” szyjki macicy. Oderwanie dolnego bieguna pęcherza płodowego, wykonywane codziennie lub 2-3 razy w tygodniu, pomaga przygotować szyjkę macicy do porodu i wywołać poród. Ta metoda jest wysoce skuteczna, łatwa do wykonania, ma niską częstotliwość występowania skutków ubocznych i jest niedroga. Jej wady obejmują dyskomfort odczuwany przez ciężarną podczas badania, rzadkie krwawienie i możliwość pęknięcia błon płodowych.
- Rozszerzanie szyjki macicy balonem. Do rozszerzania szyjki macicy balonem stosuje się cewnik Foleya. Jest on wprowadzany i nadmuchiwany do kanału szyjki macicy. Ta metoda mechanicznie rozszerza kanał szyjki macicy i zwiększa syntezę prostaglandyn. Poprzez cewnik możliwe jest wprowadzenie roztworu soli fizjologicznej do przestrzeni pozaowodniowej, rozszerzając dolny odcinek macicy, a także ułatwiając rozpoczęcie porodu.
- Mechaniczne rozszerzacze pochodzenia naturalnego i syntetycznego. Do przygotowania szyjki macicy do porodu stosuje się rozszerzacze szyjki macicy pochodzenia naturalnego - laminaria i syntetyczne - dilapan, gipan, lamicel, które są sondami o średnicy od 2 do 4 mm i długości 60-65 mm. Laminaria jest wykonana z naturalnego materiału z alg Laminaria japonicum. Syntetyczne rozszerzacze powstają z chemicznie i biologicznie obojętnych polimerów o dobrej higroskopijności. Sondy-rozszerzacze wprowadza się do kanału szyjki macicy w wymaganej ilości. Ze względu na higroskopijność pochłaniają one płyn zawarty w kanale szyjki macicy, znacznie rozszerzają się i wywierają radialny nacisk na kanał szyjki macicy. Mechanicznie otwierają szyjkę macicy i ułatwiają rozpoczęcie porodu. Syntetyczne rozszerzacze kanału szyjki macicy nie powodują dyskomfortu i są dobrze tolerowane przez pacjentki. Ograniczone stosowanie syntetycznych rozszerzaczy wiąże się z ostrożnością ze względu na ich długi pobyt w kanale szyjki macicy, zwiększający ryzyko infekcji wstępującej. Opisane mechaniczne metody działania na szyjkę macicy powodują reakcję odpowiedzi syntezy endogennych prostaglandyn E2 w szyjce macicy, które przyczyniają się do zmniejszenia ilości i destabilizacji kolagenu w jej strukturze, działając rozkurczająco na mięśnie gładkie. Ponadto prostaglandyny E2 są uważane za dominujące na początku porodu.
Leki
Stosuje się preparaty z grupy prostaglandyn E2. Do najczęstszych, sprawdzonych w praktycznym położnictwie, środków leczniczych przygotowujących szyjkę macicy do porodu i indukujących poród należą preparaty prostaglandyn E2. Prostaglandyny E2 są dostępne w różnych formach dawkowania: w postaci żeli do stosowania wewnątrzszyjkowego, tabletek dopochwowych i pesariów. Skuteczność prostaglandyn E2 w dojrzewaniu szyjki macicy i inicjowaniu porodu sięga 80–83%. Jednak ich stosowanie może skutkować rozwojem nieskoordynowanego, gwałtownego porodu i przedwczesnym odklejeniem się prawidłowo położonego łożyska. W związku z tym prostaglandyny E2 powinny być podawane wyłącznie w szpitalach położniczych z obowiązkowym kardiotokograficznym monitorowaniem czynności serca płodu i kurczliwości macicy.
Edukacja pacjenta
Koniecznie:
- nauczanie kobiet prowadzenia kalendarza menstruacyjnego w celu umożliwienia im dokładnego obliczenia wieku ciążowego i terminu porodu; liczenie ruchów płodu w celu szybkiego określenia ryzyka niedotlenienia płodu w przypadku spadku lub wzrostu jego aktywności ruchowej;
- poinformowanie pacjentki o konieczności szczegółowej oceny stanu płodu w przypadku ciąży trwającej dłużej niż 40 tygodni i 3 dni oraz ewentualnej hospitalizacji w przypadku występowania niekorzystnych czynników prognostycznych.
Dalsze zarządzanie
Standardy badania i postępowania z kobietami, u których ciąża trwa dłużej niż 40 tygodni:
- Przeprowadzanie diagnostyki różnicowej ciąży przenoszonej i przedłużonej.
Ciążę przenoszoną należy brać pod uwagę w następujących przypadkach: pierwszy poród u kobiety ciężarnej powyżej 30. roku życia, regularny cykl menstruacyjny, historia chorób przenoszonych drogą płciową i przewlekłych chorób zapalnych przydatków macicy, oznaki późnego porodu, zgodność wieku ciążowego obliczonego na podstawie pierwszego dnia ostatniej miesiączki i danych z badania USG wykonanego między 7. a 20. tygodniem ciąży, obecność „niedojrzałej” lub „niewystarczająco dojrzałej” szyjki macicy, wykrycie łożyska w stadium GIII lub małowodzia podczas badania USG.
O przedłużonej ciąży świadczą: wiek kobiety ciężarnej od 20 do 30 lat; dysfunkcja jajników z nieregularnym lub przedłużonym (>35 dni) cyklem miesiączkowym; rozbieżność między wiekiem ciążowym określonym na podstawie pierwszego dnia ostatniej miesiączki a badaniem USG; stwierdzenie „dojrzałej” szyjki macicy; łożysko o dojrzałości GI i GIII bez skamienienia oraz prawidłowa ilość płynu owodniowego w badaniu USG.
- Aby prawidłowo ocenić stan płodu i zapobiec niekorzystnym skutkom okołoporodowym, wszystkie kobiety w ciąży trwającej dłużej niż 40 tygodni muszą poddać się badaniu ultrasonograficznemu Dopplera w celu oceny hemodynamiki tętniczej płodu.
- Jeżeli hemodynamika płodu pozostaje bez zmian, organizm kobiety przygotowuje się do porodu poprzez podawanie estrogenów, doszyjkowe podanie żelu prostaglandyny E2, dynamiczną kontrolę KTG (codziennie) i monitorowanie stanu przepływu krwi u płodu (co 3 dni).
- W przypadku stwierdzenia centralizacji krążenia krwi wskazane jest badanie przepływu krwi żylnej i hemodynamiki wewnątrzsercowej w celu określenia zdolności kompensacyjnych płodu oraz wyboru metody i momentu porodu.
- W czasie ciąży po terminie hemodynamika płodu zmienia się etapami:
Stopień I - zaburzenia przepływu krwi wewnątrzłożyskowej i płodowo-łożyskowej. Na tym etapie nie występują zaburzenia hemodynamiki tętniczej i żylnej płodu. Obserwuje się wzrost oporu naczyniowego w tętnicy pępowinowej i jej odgałęzieniach końcowych, a także w tętnicach spiralnych. Wskaźniki składu gazowego i stanu kwasowo-zasadowego krwi pępowinowej mieszczą się w granicach normy.
Etap II - centralizacja krążenia płodowego. Hipoksemia jest zauważalna we krwi noworodka przy urodzeniu. Na tym etapie należy wyróżnić dwa kolejne etapy:
- IIa - początkowe objawy centralizacji krążenia tętniczego płodu przy niezmienionym przepływie krwi żylnej i wewnątrzsercowej;
- IIb - umiarkowanie nasilona centralizacja krążenia krwi z upośledzeniem przepływu krwi w przewodzie żylnym i zwiększoną prędkością przepływu krwi w zastawce aorty.
Stopień III - wyraźna centralizacja krążenia płodowego z upośledzonym odpływem żylnym i dekompensacją hemodynamiki centralnej i wewnątrzsercowej. We krwi pępowinowej noworodka przy urodzeniu - niedotlenienie połączone z kwasicą i hiperkapnią.
- W przypadku zmniejszonego CPC (< 1,1), centralizacji hemodynamiki płodu (centralizacja początkowa: SDO w MCA < 2,80; w Ao > 8,00) przy jednoczesnym zwiększeniu średniej prędkości przepływu krwi w przewodzie żylnym (centralizacja umiarkowana: SDO w MCA < 2,80; w Ao > 8,00; Tamx w VP > 32 cm/s), początkowych objawów niedotlenienia płodu zgodnie z danymi KTG, wskazane jest dożylne podanie hesobendyny + etamiwanu + etofiliny w ramach przygotowania prenatalnego w celu zwiększenia zdolności adaptacyjnych mózgu płodu.
- W przypadku początkowej centralizacji (SDO w tętnicy środkowej mózgu < 2,80; lub w aorcie płodu > 8,00) przy dobrej biologicznej gotowości ciała do porodu, niepowikłanym wywiadzie położniczym i ginekologicznym, średniej wielkości płodu, możliwy jest planowy poród drogą naturalną po amniotomii pod ścisłym monitorowaniem układu sercowo-naczyniowego płodu. Brak biologicznej gotowości ciała do porodu, zaostrzony wywiad położniczy i ginekologiczny, duża wielkość płodu dyktują konieczność przeprowadzenia planowanego cięcia cesarskiego.
- W przypadku umiarkowanie wyrażonej centralizacji hemodynamiki płodu (SDO w tętnicy środkowej mózgu < 2,80 i w aorcie > 8,00; Tamx w tętnicy szyjnej > 32 cm/s) z powodu napięcia wszystkich mechanizmów kompensacyjnych płodu i braku rezerwowych zdolności do porodu, wskazane jest planowe rozwiązanie ciąży drogą cesarskiego cięcia.
- Wykrycie zaburzeń w tętniczych i żylnych kanałach przepływu krwi u płodu (znaczna centralizacja: SDO w tętnicy środkowej mózgu < 2,80 i w aorcie > 8,00; w VPr S/A > 2,25, PIV > 1,00; w IVC %R > 16%, PIV > 1,2) w połączeniu z umiarkowanym lub ciężkim niedotlenieniem płodu zgodnie z danymi KTG wskazuje na dekompensację hemodynamiki płodu i wymaga rozwiązania ciąży poprzez cesarskie cięcie.
Zapobieganie
- Identyfikacja grupy ryzyka ciąży po terminie wśród kobiet poszukujących opieki prenatalnej.
- Zapobieganie niewydolności łożyska i dużym płodom.
- Dokładne obliczenie czasu trwania ciąży i daty porodu, biorąc pod uwagę datę ostatniej miesiączki (w przypadku regularnego cyklu miesiączkowego) oraz badanie USG wykonane przed 20 tygodniem ciąży.
- Terminowa hospitalizacja kobiety ciężarnej w celu przygotowania kanału rodnego do porodu i oceny stanu płodu.
Prognoza
Przy terminowej i dokładnej ocenie stanu płodu oraz odpowiedniej taktyce położniczej rokowanie jest korzystne. Wskaźniki rozwoju fizycznego i neuropsychicznego dzieci nie różnią się od tych w niepowikłanych terminowych porodach. Jednak wraz z rozwojem powikłań, zwłaszcza ciężkiego niedotlenienia płodu, urazu okołoporodowego, zachłyśnięcia smółką, rokowanie jest mniej korzystne. Straty okołoporodowe wynoszą do 7%, uszkodzenia niedotlenieniowo-niedokrwienne ośrodkowego układu nerwowego - do 72,1%.


 [
[