Arachnodactyly
Ostatnia recenzja: 18.10.2021

Cała zawartość iLive jest sprawdzana medycznie lub sprawdzana pod względem faktycznym, aby zapewnić jak największą dokładność faktyczną.
Mamy ścisłe wytyczne dotyczące pozyskiwania i tylko linki do renomowanych serwisów medialnych, akademickich instytucji badawczych i, o ile to możliwe, recenzowanych badań medycznych. Zauważ, że liczby w nawiasach ([1], [2] itd.) Są linkami do tych badań, które można kliknąć.
Jeśli uważasz, że któraś z naszych treści jest niedokładna, nieaktualna lub w inny sposób wątpliwa, wybierz ją i naciśnij Ctrl + Enter.
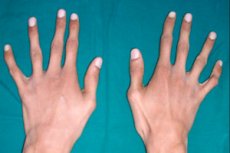
Jedną z rzadkich dziedzicznych patologii tkanki łącznej jest arachnodaktylia - deformacja palców, której towarzyszy wydłużenie kości rurkowych, skrzywienie szkieletu, zaburzenia układu sercowo-naczyniowego i narządu wzroku.
Choroba została po raz pierwszy opisana przez dr Williamsa i francuskiego pediatrę Marfana, który nazwał ją dolichostenomelią. W medycynie światowej pojawił się później termin zespół Marfana, a od 1902 roku zaczęto używać nazwy arachnodaktylia. Patologia dotyczy wrodzonych wad tkanki łącznej, a jednym z głównych objawów są wydłużone, przerzedzone i zakrzywione palce „pająka”. [1]
Epidemiologia
Arachnodaktylia jest uważana za dziedziczną monogenną patologię tkanki łącznej, dziedziczoną autosomalnie dominująco, o wysokiej penetracji i różnym stopniu ekspresji.
W około 75-80% przypadków choroba jest dziedziczna, w pozostałych przypadkach następuje w wyniku spontanicznych mutacji (w szczególności mutacji punktowych). [2]
Udowodniono, że patogenetyczne cechy arachnodaktyli wynikają ze zmian w kilku genach (w 95% przypadków):
- w genie fibryliny-1 (zbadano około tysiąca mutacji) na chromosomie 15q21.1;
- gen TGFβR1 lub TGFβR2 na dziewiątym i 3p24.2-P25 chromosomie.
Zmiany te bezpośrednio wpływają na skalę objawów klinicznych.
U 5% pacjentów opisano mutacje w łańcuchu α-2 kolagenu typu I.
Częstość występowania arachnodaktyli wynosi około 2 przypadków na 5 tysięcy osób. Nie ma determinizmu rasowego ani płciowego. [3]
Przyczyny arachnodaktylia
Arachnodaktylia występuje w wyniku spontanicznej mutacji. Choroba nie charakteryzuje się dobrze znanymi objawami wrodzonych i dziedzicznych patologii, a wydłużone palce objawiają się głównie w zespole Marfana i homocystynurii.
Choroba jest rzadka, a wszyscy wykrywani pacjenci mieli mutację w genie FBN1 (gen fibryliny) zlokalizowanym na chromosomie 15 w regionie q21.1. Kliniczny polimorfizm zespołu można wyjaśnić masą mutacji, a około 15% to zmiany mutacyjne, które wystąpiły podczas poczęcia. [4]
Nietypowe odmiany arachnodaktyli są wywoływane przez mutacje z innych genów: stwierdzono związek między rozwojem patologii a mutacjami genu LTBP3, R zlokalizowanego na chromosomie 14 w regionie q24, który przekształca czynnik wzrostu.
Przytłaczająca większość mutacji to mutacje typu missense (około 57%). Ponad 20% to małe delecje z utratą części chromosomowych, około 12% mutacji w miejscu splicingowym, 8% nonsensownych mutacji i 2% rearanżacji i delecji na dużą skalę. [5]
Wrodzony przykurcz pajęczynówki jest spowodowany upośledzoną syntezą czynnika białkowego fibryliny-2. Problem jest spowodowany mutacją w genie FBN2, zlokalizowanym na piątym chromosomie w regionie q23-q31. Wszystkie mutacje są przeważnie mutacjami punktowymi, zmieniającymi kodon na kodowanie innego aminokwasu. [6]
Homocystynuria rozwija się na tle upośledzonego metabolizmu niezbędnego aminokwasu metioniny. Podstawą patologii może być utrata aktywności lub jej zmniejszenie ze strony takich substancji enzymatycznych:
- Enzym beta syntazy cystationiny (CBS). Patologia jest oporna na witaminę B 6 i objawia się objawami charakterystycznymi dla postaci niezależnej od witaminy B 6, jednak wprowadzenie preparatu witaminowego B 6 nie prowadzi do poprawy.
- Enzym N5, N10 reduktaza metylenotetrahydrofolianu (MTHFR). Ten środek enzymatyczny jest substratem, który powoduje demetylację homocysteiny i jej przemianę w metioninę, niezbędny aminokwas, z którego składa się wiele substancji białkowych i peptydowych.
- Enzym N5 to metylenotetrahydrofolian. To jest B 6 forma zależna od patologii, która rozwija się z niedoborem witaminy B 6. Wprowadzenie preparatu witaminowego do organizmu poprawia stan pacjenta.
- Enzym transmetylazy homocysteiny. Rozwija się na tle zaburzeń metabolicznych kobalaminy - witaminy B 12.
Czynniki ryzyka
Arachnodaktylia jest chorobą uwarunkowaną genetycznie, charakteryzującą się ogólnoustrojowym uszkodzeniem tkanki łącznej. Patologia jest związana ze zmianami w genie fibryliny 1 zlokalizowanymi na krótkim ramieniu chromosomu 15 w locus 21.1.
Arachnodaktylia jest dziedziczona w sposób autosomalny dominujący i charakteryzuje się dużą penetracją i zróżnicowaną ekspresją. Patologia może objawiać się zarówno po stronie męskiej, jak i żeńskiej.
Patogeneza
Ponad 50% masy ciała człowieka to struktury tkanki łącznej, w szczególności - szkielet, skóra, układ naczyniowy, chłonka i krew.
Komórki tkanki łącznej reprezentowane są przez fibroblasty i ich podtypy: osteoblasty, chondrocyty, keratoblasty, odontoblasty, a także makrofagi i komórki tuczne.
Embrionalna tkanka łączna jest materiałem do tworzenia komponentów konstytucyjnych, genetycznych i epigenetycznych. Choroby tkanki łącznej odbijają się w różnym stopniu na całym ciele jako całości, na jego funkcjonalnej zdolności i budowie.
W przypadku arachnodaktyli odnotowuje się substytucję nukleotydów w genie, który zawiera informacje strukturalne o peptydzie fibryliny-1. Ta substancja białkowa należy do grupy glikoprotein, uczestniczy w układzie mikrofibrylarnym i stanowi podstawę elastycznych włókienek tkanki łącznej.
Tkanka zachowuje stabilną strukturę, dzięki macierzy zewnątrzkomórkowej zawierającej wiele czynników wzrostu zapewniających systematyczną odnowę komórkową. Duże naczynia i więzadła zawierają liczne włókienka elastyny, przy porażce której obserwuje się główne objawy arachnodaktyli.
Znacząco wpływa to na transformujący czynnik wzrostu β: jego nieaktywna forma nie wiąże się, co pociąga za sobą wzrost aktywności biologicznej tego czynnika.
Zaburzenia fibryliny wiążą się z niewłaściwym tworzeniem się włókien, w wyniku czego dochodzi do utraty siły i elastyczności skóry oraz innych struktur tkanki łącznej.
Jeśli struktura kolagenu jest zaburzona, zaburzone zostaje główne ogniwo hemostazy.
Eksperci zwracają uwagę na udział zaburzeń hormonalnych w pojawieniu się i progresji nieprawidłowości w obrębie struktur tkanki łącznej, w tym arachnodaktyli. O objawach zakrzepowych decydują zaburzenia reologiczne - w szczególności zmiana lepkości krwi w zmodyfikowanych naczyniach okolicy ramienno-głowowej.
Na skutek zaburzeń kolagenu dochodzi do zaburzeń w przewodzie pokarmowym: dyskinezy hipomotorycznej dróg żółciowych, przepukliny rozworu przełykowego, wady wątroby i dróg żółciowych, przewlekła postać „wymazanego” zapalenia żołądka i dwunastnicy, dolichosigma.
W jaki sposób dziedziczona jest arachnodaktylia?
Arachnodaktylia jest dziedziczona w sposób autosomalny dominujący, ale może również wystąpić w wyniku spontanicznych mutacji. Oznacza to, że nie jest wcale konieczne, aby patologia objawiała się u któregokolwiek z bliskich krewnych - na przykład u rodziców i dziadków. Mutacje leżące u podstaw patologii mogą objawiać się w przypadkowej kolejności.
Objawy arachnodaktylia
W medycynie dzielą wymazany i oczywisty przebieg arachnodaktyli. W przypadku wymazanego przebiegu zmiany są obecne, ale są one pojedyncze i ograniczone do jednego lub dwóch układów narządów. Wyraźny przebieg objawia się wieloma widocznymi zaburzeniami o różnym nasileniu objawów. Jednocześnie stan pacjenta może być względnie stabilny przez dziesięciolecia lub może się stale rozwijać, objawiając się w odniesieniu do innych narządów i układów.
Często zespół arachnodaktyli można wykryć już w pierwszych kilku dniach po urodzeniu dziecka.
Głównym zewnętrznym objawem arachnodaktyli są smukłe i wydłużone palce, które dzięki krótkim ścięgnom nabierają typowej krzywizny i przypominają nogi pająka.
Palce pająka lub arachnodaktylia stają się wyraźnie widoczne prawie od okresu noworodkowego. Ale objaw pojawia się wyraźniej w wieku około trzech lat.
Charakterystyczne są również wskaźniki wzrostu: dzieci są zwykle wysokie, przedramiona i nogi długie, kończyny nieproporcjonalne i cienkie. Dysproporcja jest szczególnie widoczna przy wysokim umiejscowieniu talii i kolan. [7]
Inne zaburzenia szkieletowe obejmują:
- zwężony i wydłużony kształt czaszki (dolichocefaliczny) z nieprawidłowo uformowaną częścią twarzy;
- konfiguracja klatki piersiowej w kształcie lejka (tzw. „ptak”);
- zakrzywiony kręgosłup;
- wrodzone zwichnięcia stawu biodrowego;
- nawykowe zwichnięcia stawu kolanowego;
- skrzywienie kości piętowej;
- formacje osteofityczne - narośla kostne;
- płaskostopie;
- niedostateczny rozwój tkanki tłuszczowej.
Dodatkowymi oznakami arachnodaktyli mogą być:
- krótkowzroczność;
- niebieskawa twardówka;
- podwichnięcie soczewki;
- zaburzenia pracy serca i naczyń krwionośnych (wady serca, tętniak aorty);
- wyraźna cienkość;
- hipermobilność stawów;
- Niebo „łukowate”.
Arachnodaktylia charakteryzuje się wydłużeniem kości rurkowych, powodując różne krzywizny szkieletu. Ponadto wielu pacjentów ma zaburzenia piramidalne, asymetrię odruchów ścięgnistych, anosocoria i oczopląs na tle normalnego rozwoju umysłowego.
Jeśli mówimy o arachnodaktyli, współistniejącej homocystynurii, wówczas pacjent może mieć następujące objawy:
- okresowe napady padaczkowe;
- jaskra wtórna z podwichnięciem soczewki;
- odwarstwienie siatkówki, astygmatyzm;
- uszkodzenie pni tętniczych (w tym nerek, mózgu);
- osteoporoza;
- zakrzepica;
- zaburzenia psychiczne.
Arachnodaktylia u noworodków
W większości przypadków arachnodaktylia może zostać wykryta u dziecka w ciągu pierwszych kilku dni jego życia. Co więcej, w przyszłości wraz z wiekiem objawy nasilają się.
Pierwsze oznaki podejrzenia choroby są zwykle następujące:
- niezwykle długie kończyny i palce;
- brak wagi przy odpowiedniej kondycji fizycznej dziecka;
- wydłużona wydłużona twarz;
- niedobór tkanki tłuszczowej, słabo rozwinięte mięśnie;
- nadmierna elastyczność stawowa.
Od około czterech lat na tle arachnodaktyli klatka piersiowa zaczyna się zmieniać, kręgosłup zgina się i rozwijają się płaskie stopy.
Od strony narządów wzroku obserwuje się krótkowzroczność, ektopię soczewki, zmienioną konfigurację rogówki, zez, procesy hipoplastyczne w tęczówce i siatkówce. Takie naruszenia można zauważyć już w pierwszych 2-3 latach życia dziecka, chociaż postępują one z biegiem lat.
Największe niebezpieczeństwo stwarzają naruszenia układu sercowo-naczyniowego. Jeśli dochodzi do takich naruszeń, to na tle braku odpowiedniego leczenia istnieje duże ryzyko śmierci pacjenta nawet w dzieciństwie. Wśród najniebezpieczniejszych patologii można wyróżnić uszkodzenia ścian naczyniowych, wady rozwojowe serca, wady naczyń wieńcowych. Czasami u dzieci w pierwszym roku życia wykrywa się już narastającą niewydolność serca.
Arachnodaktyli może towarzyszyć uszkodzenie innych narządów - w szczególności układu nerwowego, oskrzeli i płuc, skóry, układu moczowo-płciowego. Takie naruszenia są wykrywane w trakcie działań diagnostycznych.
Komplikacje i konsekwencje
Najczęstszymi działaniami niepożądanymi arachnodaktyli są uszkodzenia serca i układu oddechowego. Ponadto pojawiają się problemy ze wzrokiem, a nawet utrata.
Pacjenci z arachnodaktylią wymagają kompleksowej terapii wszystkich istniejących patologii. Jeśli takie leczenie nie zostanie przeprowadzone, oczekiwana długość życia pacjentów jest znacznie zmniejszona: rzadcy pacjenci potrafią dożyć 40 roku życia bez interwencji medycznej. Z biegiem lat problemy z układem sercowo-naczyniowym nasilają się, wzrasta ryzyko rozległych krwotoków z tragicznym skutkiem.
Osoby cierpiące na arachnodaktylia powinny być regularnie badane i leczone pod kątem współistniejących patologii: tylko pod tym warunkiem mają wszelkie szanse na długie życie i bez poważnych komplikacji.
Zespół Marfana i arachnodaktylia wymagają szczególnej uwagi, jeśli pacjentka zajdzie w ciążę. W takiej sytuacji ważne jest, aby regularnie i dokładnie badać pacjentkę, przyjmować leki, aby utrzymać stan układu sercowo-naczyniowego. Tylko w ten sposób można zagwarantować udaną ciążę i bezpieczny poród.
Aby uniknąć niepożądanych konsekwencji, pacjenci z arachnodaktylem powinni być regularnie badani przez lekarzy, aby zapobiec rozwojowi patologii sercowo-naczyniowych i układu mięśniowo-szkieletowego. Zaleca się im wyjątkowo zdrowy tryb życia, przy umiarkowanej aktywności fizycznej.
Diagnostyka arachnodaktylia
Diagnostyka kliniczna arachnodaktyli obejmuje gromadzenie skarg, wywiad dziedziczny i rodzinny, ocenę fenotypu, a także badania antropometryczne i fizyczne. Ważne jest, aby określić obecność objawów patologii tkanki łącznej u bezpośrednich krewnych: w tym celu przeprowadza się badanie genealogiczne. [8]
Diagnostyka laboratoryjna arachnodaktyli obejmuje badanie stanu niektórych typów tkanki łącznej, reprezentowanych przez tkankę kostną i chrzęstną, krew, limfę. Najbardziej pouczające jest badanie poziomu hydroksyproliny i glikozoaminoglikanów w dziennej objętości moczu. Dodatkowo ocenia się zawartość lizyny, proliny, hydroksyproliny we krwi. Aby określić zmienione proporcje różnych typów kolagenów i zaburzenia strukturalne włókien kolagenowych, typowanie jest przepisywane metodą immunofluorescencji pośredniej z użyciem przeciwciał poliklonalnych przeciwko kolagenowi i fibronektynie. [9] W zależności od wskazań wykonywane są następujące analizy odzwierciedlające jakość procesów metabolicznych tkanki łącznej:
- glikozaminoglikany, fibrylina, fibronektyna;
- badanie hydroksyproliny, markerów biosyntezy kolagenu typu 1, aminoterminalnych propeptydów prokolagenu typu 1, markerów degradacji kolagenu typu 1, galaktozyloksylizyny, deoksypirydynoliny;
- analiza rozdzielczości metabolizmu kolagenu (badanie metaloproteinaz macierzy i tkankowych inhibitorów metaloproteinaz macierzy, transformującego czynnika wzrostu);
- analiza mikro i makroelementów (zawartość wapnia i magnezu, fosforu, żelaza, siarki i miedzi, kobaltu i selenu, cynku i magnezu, fluoru i wanadu, krzemu i boru);
- badanie markerów tworzenia się tkanki kostnej i szybkości procesów przebudowy (analiza zawartości osteokalcyny, fosfatazy alkalicznej kości, parathormonu, hormonu somatotropowego, prolaktyny, witaminy D 3, pentozydyny, homocysteiny w moczu i krwi).
Diagnostyka instrumentalna ma na celu identyfikację istniejących wad rozwojowych oraz ocenę stanu funkcjonalnego narządów i układów. Zaburzenia sercowo-naczyniowe z arachnodaktylią wymagają obowiązkowego wpisania na listę diagnostyczną takich procedur jak:
- elektrokardiografia;
- codzienne monitorowanie EKG;
- badanie ultrasonograficzne serca i naczyń krwionośnych.
Nieprawidłowości naczyniowe są badane za pomocą tomografii komputerowej lub rezonansu magnetycznego. Dodatkowe procedury diagnostyczne mogą obejmować:
- USG narządów jamy brzusznej, układu moczowo-płciowego;
- RTG klatki piersiowej, stawów biodrowych; [10]
- CT lub MRI kręgosłupa.
Po wykonaniu wszystkich niezbędnych badań pacjentka kierowana jest na poradę genetyczną.
Diagnostyka różnicowa
Istnieje podobieństwo fenotypowe między zespołem Bealsa a arachnodaktylią w zespole Marfana (mutacje odpowiednio genów FBN2 i FBN1), co wynika z niemal całkowitej identyczności substancji białkowych fibryliny 1 i fibryliny 2. Nic dziwnego, że druga nazwa zespołu Bealsa to przykurcz pajęczynowy. [11]
Różnicowanie przeprowadza się z innymi patologiami tkanki łącznej:
- Zespół Sticklera;
- Zespół Ehlersa-Danlosa;
- homocystynuria;
- artrogrypoza.
Zespół Bealsa charakteryzuje się fenotypem marfanoidalnym, wrodzonymi przykurczami zgięciowymi dużych i małych stawów, pajęczakiem nadgarstka i stopy, skrzywieniem kręgosłupa, nieregularnym kształtem uszu (tzw. „Zgniecione” małżowiny uszne). W celu potwierdzenia rozpoznania przeprowadza się analizę molekularną genu FBN2.
Artrogrypoza charakteryzuje się licznymi przykurczami stawowymi, niskim wzrostem i obniżoną inteligencją. Kształt palców i uszu był normalny. [12]
W przypadku zespołu Ehlersa-Danlosa obserwuje się kifoskoliozę, lejkowatą krzywiznę klatki piersiowej, wyraźne płaskie stopy i upośledzoną refrakcję. Typowe są zwiększona ruchliwość i zwichnięcia stawów, wysoka elastyczność i wrażliwość skóry.
Zespół Sticklera charakteryzuje się zmianą objętości i sztywności stawów.
Z kim się skontaktować?
Leczenie arachnodaktylia
Arachnodaktylia należy do kategorii patologii genetycznych, a obecnie medycyna nie dysponuje metodami korygowania defektów genów. Dlatego leczenie ukierunkowane jest na optymalizację stanu pacjenta, zapobieganie zaostrzeniu patologii i eliminację objawów objawowych. Zalecana jest kompleksowa terapia, z udziałem kilku lekarzy specjalistów jednocześnie, co zależy od przynależności do najbardziej wyraźnej symptomatologii: często dodatkowo trzeba skontaktować się z ortopedą, kardiologiem, okulistą, gastroenterologiem i innymi lekarzami. [13]
Wśród zaleceń dotyczących postępowania klinicznego z pacjentami za zasady ogólne uważa się:
- ograniczenie aktywności fizycznej, ale nie całkowite jej zaniechanie (w ramach wspomagania układu sercowo-naczyniowego);
- terapia lekowa;
- jeśli to konieczne, chirurgiczna korekcja najbardziej dotkniętych obszarów serca i naczyń krwionośnych;
- korekcja ortopedyczna;
- leczenie uzdrowiskowe, fizjoterapia, ćwiczenia fizjoterapeutyczne.
Żywność dietetyczna pacjentów z arachnodaktylem powinna zawierać wystarczającą ilość pokarmów wysokobiałkowych, wzbogaconych pierwiastkami śladowymi, witaminami, kwasami tłuszczowymi. Zalecane jest użycie mięsa, ryb, owoców morza, fasoli, orzechów. Jeśli arachnodaktylia jest spowodowana homocystynurią, wówczas stosowanie białka zwierzęcego jest mocno ograniczone.
Dzieciom o szczupłej sylwetce i wysokim wzroście zaleca się wprowadzanie do diety oleju bawełnianego i sojowego, nasion słonecznika, słoniny i smalcu od najmłodszych lat. Dodatkowo oferują preparaty zawierające wielonienasycone kwasy tłuszczowe typu Omega, które hamują produkcję hormonu somatotropowego.
Aby znormalizować metabolizm białek, przepisuje się witaminy z grupy B. Można je również uzyskać z pożywienia: gryki, grochu, wątroby.
Bardzo ważne jest, aby kwas askorbinowy dostał się do organizmu pacjenta wraz z pożywieniem. W tym celu do diety koniecznie wprowadza się napar z dzikiej róży, paprykę, kapustę, owoce cytrusowe, a także rokitnik zwyczajny, pory.
W razie potrzeby pacjentom oferuje się korektę ortopedyczną niezbędną do zmniejszenia obciążenia kręgosłupa i stawów. W tym celu stosuje się buty ortopedyczne, kolana i inne przyrządy, podpórki podbicia, bandaże elastyczne.
Leczenie operacyjne przeprowadza się zgodnie ze wskazaniami.
Leki
Leczenie farmakologiczne arachnodaktyli przeprowadza się 1-2 razy w roku, co zależy od stanu pacjenta i nasilenia objawów patologicznych. Czas trwania kuracji ustalany jest indywidualnie i wynosi średnio 4 miesiące. [14]
Aby stymulować tworzenie kolagenu, leki Piaskledin 300, L-lizyna lub L-prolina są przepisywane w połączeniu ze złożonymi preparatami multiwitaminowymi zawierającymi kwas askorbinowy, witaminy z grupy B, tokoferol, magnez, cynk, selen, miedź.
Spośród chondroprotektorów najbardziej optymalne wykorzystanie siarczanu chondroityny i siarczanu glukozaminy - leków, które biorą udział w regulacji metabolizmu chondrocytów, hamowaniu syntezy enzymów, zwiększaniu wrażliwości chondrocytów na działanie enzymów, w stymulacji procesów anabolicznych itp.
Metabolizm minerałów jest stymulowany przez leki normalizujące procesy fosforowo-wapniowe. Często lekami z wyboru stają się aktywne formy witaminy D: Alpha D 3 -Teva, Oxydevit, Bonviva itp. Jednocześnie stosowane są preparaty z fosforu, wapnia, magnezu. W trakcie leczenia mniej więcej raz na 20 dni sprawdza się poziom wapnia i fosforu we krwi lub moczu oraz wykonuje się badanie krwi na obecność fosfatazy zasadowej.
Aby poprawić stan bioenergetyczny organizmu, można przepisać fosfaden, ryboksynę, lecytynę, elkar, koenzym Q10.
Przybliżony schemat terapii może wyglądać następująco:
- Chondroprotector w odpowiedniej dawce, przyjmowany z jedzeniem i wystarczającą ilością wody. Czas trwania jednego kursu leczenia wynosi 3-4 miesiące.
- L-prolina w dawce 500 mg (dla dzieci od 12 roku życia i dorosłych) przyjmuje się pół godziny przed posiłkiem 1-2 razy dziennie przez sześć tygodni. Jeśli jest to wskazane, dodatkowo można przepisać kompleks aminokwasów - L-prolinę, L-lizynę, L-leucynę w ilości 10-12 mg / kg wagi. Odbiór odbywa się 1-2 razy dziennie przez dwa miesiące.
- Kompleksowe preparaty witaminowo-mineralne Centrum lub Vitrum lub Unicap w dawkach uwzględniających wiek. Czas przyjęcia to 4 tygodnie.
Ten schemat leczenia jest odpowiedni, jeśli pacjent z pajęczakiem skarży się na problemy z układem mięśniowo-szkieletowym, a wyniki badań wskazują na zwiększone wydalanie glikozoaminoglikanów w 24-godzinnym badaniu moczu i obniżoną zawartość wolnych aminokwasów we krwi.
Z reguły zabieg jest dobrze odbierany przez pacjentów, bez żadnych specjalnych skutków ubocznych. W przypadku wykrycia reakcji nadwrażliwości leki są wymieniane, schemat leczenia jest dostosowywany.
Zabieg fizjoterapeutyczny
Procedury fizjoterapeutyczne dla arachnodaktyli są przepisywane zgodnie ze wskazaniami. Na przykład przy niewystarczającej osteogenezie, aby poprawić gojenie się złamań kości lub z objawami osteoporozy, zaleca się elektroforezę z 5% chlorkiem wapnia, 4% siarczanem magnezu, 2% siarczanem miedzi lub 2% siarczanem cynku.
W przypadku stwierdzenia wegetatywnych zaburzeń naczyniowych należy użyć 1% kofeiny, benzoesanu sodu, chlorowodorku efedryny lub mezatonu.
Aby aktywować sprawność kory nadnerczy, zaleca się elektroforezę lekową z 1,5% etymizolem i terapię decymetrową w okolicy nadnerczy. [15]
Aby ustabilizować napięcie naczyniowe, zaleca się zabiegi wodne promujące „gimnastykę” naczyniową. Kąpiele takie jak dwutlenek węgla, iglaste, solne, siarkowodór, radon są doskonałe. Ćwiczą natryski, bicze, prysznice kontrastowe, kąpiele pianowe i solankowe.
W celu poprawy stanu tkanki chrzęstnej stosuje się magnetoterapię, induktoterapię, laseroterapię, elektroforezę z dimetylosulfaksydem (dimeksydem).
Operacja
Operacje chirurgiczne dla arachnodaktyli są ściśle określone zgodnie ze wskazaniami. Na przykład po wykryciu wyraźnych zaburzeń hemodynamicznych na tle wypadnięcia płatków zastawki wykonuje się masywny tętniak aorty, protetykę zastawek i uszkodzony odcinek aorty. [16]
Jeśli występują wyraźne zaburzenia czynnościowe układu oddechowego i sercowo-naczyniowego, wynikające z silnego skrzywienia klatki piersiowej, wykonuje się torakoplastykę.
W przypadku postępującego zespołu bólowego spowodowanego ciężką postacią skoliozy 3-4 stopni wskazana jest również interwencja chirurgiczna. Z okulistycznego punktu widzenia podwichnięcie soczewki powikłane jaskrą wtórną, a także zaćma i zmiany zwyrodnieniowe siatkówki z dużym ryzykiem odwarstwienia są uważane za bezwzględne wskazania do usunięcia soczewki.
Każda operacja u pacjentów z pajęczakiem i innymi zaburzeniami rozciągającymi się na struktury tkanki łącznej jest wykonywana tylko na etapie względnej ulgi klinicznej i biochemicznej. Po zabiegu wymagany jest długotrwały nadzór lekarski i intensywna terapia lekami usprawniającymi wymianę tkanki łącznej.
Zapobieganie
Arachnodaktylia jest rzadkim zaburzeniem genetycznym. Czasami pojawia się spontanicznie u pozornie zdrowych rodziców. Dlatego bardzo, bardzo trudno jest z wyprzedzeniem zapobiec wystąpieniu choroby.
Jeśli któryś z potencjalnych rodziców ma obciążoną historię rodzinną - to znaczy wiadomo, że ktoś z rodziny miał arachnodaktylę - to małżonkowie powinni odwiedzić genetykę i przejść badanie genetyczne na etapie planowania dziecka. Po potwierdzeniu zajścia w ciążę lekarz przeprowadza diagnostykę prenatalną, która obejmuje badanie ultrasonograficzne płodu oraz szereg badań biochemicznych:
- analiza krwi matki;
- analiza płynu owodniowego;
- biopsja kosmówkowa;
- analiza komórek łożyska i krwi pępowinowej.
Pacjenci z arachnodaktylem przez całe życie pozostają pod nadzorem lekarza. Działania profilaktyczne u pacjentów mają na celu zapobieganie powikłaniom. W tym celu wykonuje się korekcję kardiochirurgiczną, przepisuje się leczenie farmakologiczne, aby wyeliminować ryzyko powstania skrzepliny. Kursy antybiotykoterapii są przeprowadzane okresowo.
Prognoza
Rokowanie w życiu pacjentów z arachnodaktylią determinuje przede wszystkim nasilenie współistniejących schorzeń - w szczególności chorób układu krążenia, narządu ruchu i narządu wzroku. Najczęściej patologię komplikuje pęknięcie i rozwarstwienie aorty. Konieczne jest uwzględnienie tego i terminowe przeprowadzenie korekcji kardiochirurgicznej, która pomoże przedłużyć życie pacjenta i poprawić jego jakość.
Jeśli diagnoza została postawiona w odpowiednim czasie, to zgodnie z zaleceniami lekarzy rokowanie można nazwać warunkowo korzystne. Wsparcie medyczne znacznie ułatwia przebieg arachnodaktyli, a pacjenci mają możliwość normalnego i stosunkowo pełnego życia bez rozwoju poważnych powikłań.

