Ekspert medyczny artykułu
Nowe publikacje
Zespół Sheehana
Ostatnia recenzja: 04.07.2025

Cała zawartość iLive jest sprawdzana medycznie lub sprawdzana pod względem faktycznym, aby zapewnić jak największą dokładność faktyczną.
Mamy ścisłe wytyczne dotyczące pozyskiwania i tylko linki do renomowanych serwisów medialnych, akademickich instytucji badawczych i, o ile to możliwe, recenzowanych badań medycznych. Zauważ, że liczby w nawiasach ([1], [2] itd.) Są linkami do tych badań, które można kliknąć.
Jeśli uważasz, że któraś z naszych treści jest niedokładna, nieaktualna lub w inny sposób wątpliwa, wybierz ją i naciśnij Ctrl + Enter.
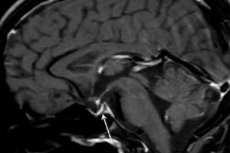
Martwica niedokrwienna przysadki mózgowej i uporczywy spadek jej funkcji z powodu krwotoku poporodowego nazywane są zespołem Sheehana. To rzadkie powikłanie porodu, któremu towarzyszy zagrażająca życiu utrata krwi, nazywane jest również poporodową niewydolnością przysadki mózgowej, poporodową niedoczynnością przysadki mózgowej, wyniszczeniem przysadkowym (międzymózgowo-przysadkowym) lub chorobą Simmondsa.
Ta patologia endokrynologiczna ma kod E23.0 zgodnie z ICD-10.
Epidemiologia
W krajach rozwiniętych, ze względu na wysoki poziom opieki położniczej, zespół Sheehana występuje rzadko: jego częstość występowania zmniejszyła się w ciągu 50 lat z 10-20 przypadków na 100 tysięcy kobiet do 0,5% wszystkich przypadków niedoczynności przysadki mózgowej u kobiet.
Według Europejskiego Towarzystwa Endokrynologicznego, pewne objawy łagodnego uszkodzenia przedniego płata przysadki mózgowej obserwuje się u 4% kobiet, które straciły dużo krwi podczas porodu. Umiarkowane objawy zespołu Sheehana diagnozuje się u 8%, a ciężkie formy poporodowej niedoczynności przysadki mózgowej występują u 50% kobiet po wstrząsie hipowolemicznym.
Międzynarodowa baza danych rejestru farmakoepidemiologicznego KIMS (Pfizer International Metabolic Database) za rok 2012 odnotowała 1034 pacjentów z niedoborem hormonu wzrostu (GH), przy czym u 3,1% pacjentek przyczyną tej patologii jest zespół Sheehana.
Niedoczynność przysadki poporodowej stanowi poważne zagrożenie dla kobiet w krajach słabo rozwiniętych i rozwijających się. Na przykład w Indiach częstość występowania zespołu Sheehana szacuje się na 2,7-3,9% wśród kobiet po porodzie w wieku powyżej 20 lat.
Przyczyny Zespół Sheehana
Wszystkie przyczyny zespołu Sheehana są wynikiem wstrząsu hipowolemicznego, który rozwija się w wyniku gwałtownego zmniejszenia objętości krwi krążącej i spadku ciśnienia krwi spowodowanego krwawieniem w trakcie porodu.
Przy dużej utracie krwi (ponad 800 ml) zaburzone zostaje ukrwienie organów i dopływ tlenu do nich. A przede wszystkim dotyczy to mózgu. Zespół Sheehana powstaje w wyniku uszkodzenia przysadki mózgowej – gruczołu mózgowego odpowiedzialnego za syntezę najważniejszych hormonów.
Najbardziej cierpią komórki produkujące hormony w jej przednim płacie, przysadce mózgowej. Podczas ciąży, pod wpływem hormonów łożyska, wielkość tego gruczołu zwiększa się, według niektórych szacunków, o 120-136%. W szczególności dochodzi do przerostu i hiperplazji laktotropocytów - komórek syntetyzujących prolaktynę, która jest niezbędna do rozwoju i przygotowania gruczołów sutkowych do produkcji mleka.
Czynniki ryzyka
Położnicy i ginekolodzy wymieniają czynniki ryzyka rozwoju zespołu Sheehana:
- zaburzenia krzepnięcia krwi u kobiet w ciąży (w szczególności trombocytopenia);
- obrzęk tkanek obwodowych (w którym aktywowany jest hormon podwzgórza – wazopresyna, zwiększający napięcie naczyń i ciśnienie krwi);
- nadciśnienie ciążowe (wysokie ciśnienie krwi);
- stan przedrzucawkowy (wysokie ciśnienie krwi i białkomocz);
- zwiększona hemoliza (niszczenie czerwonych krwinek, najczęściej związane z niewydolnością nerek).
Zwiększone ryzyko krwawienia podczas porodu i rozwoju zespołu Sheehana występuje w przypadku łożyska przodującego, jego przedwczesnego odklejenia, a także w ciążach mnogich (bliźniaczych lub trojaczych) oraz przy szybkim (burzliwym) porodzie, w trakcie którego może dojść do zatoru naczyń płucnych płynem owodniowym.
Patogeneza
Patogeneza zespołu Sheehana jest związana z niedotlenieniem tkanek przysadki i ich obumarciem. Główną rolę w zwiększonej podatności przysadki mózgowej odgrywa osobliwość jej ukrwienia: poprzez układ żyły wrotnej i sieć włośniczkowych zespoleń naczyń wrotnych. Przy silnym krwawieniu i spadku ciśnienia krwi lokalny przepływ krwi w powiększonym przednim płacie gruczołu jest nieobecny; skurcz naczyń krwionośnych odżywiających przysadkę mózgową związany ze wstrząsem prowadzi do niedoboru tlenu i martwicy niedokrwiennej gruczołu.
W rezultacie przysadka mózgowa nie produkuje wystarczających ilości następujących hormonów tropowych:
- somatotropina (STH), która aktywuje syntezę białek komórkowych, reguluje metabolizm węglowodanów i hydrolizę lipidów;
- prolaktyna (hormon luteotropowy), który stymuluje rozwój i czynność gruczołów piersiowych oraz ciałka żółtego;
- hormon folikulotropowy (FSH), który zapewnia wzrost pęcherzyków jajnikowych i procesy proliferacyjne w tkance macicy;
- hormon luteinizujący (LH), odpowiedzialny za owulację;
- hormon adrenokortykotropowy (ACTH), który aktywuje produkcję kortykosteroidów przez korę nadnerczy;
- hormon tyreotropowy (TSH), który reguluje funkcję wydzielniczą tarczycy.
Objawy Zespół Sheehana
Zaburzenia równowagi hormonów produkowanych przez przysadkę mózgową powodują różnorodne objawy w zespole Sheehana, w zależności od stopnia niedoboru wydzielania konkretnych hormonów przysadkowych.
Ilość uszkodzonych komórek przysadki mózgowej determinuje ostrą i przewlekłą postać choroby. Ostra postać odzwierciedla znaczne uszkodzenie przedniego płata gruczołu, a objawy stają się widoczne wkrótce po urodzeniu. W przypadkach przewlekłych wykryte uszkodzenia są mniejsze, a objawy mogą nie pojawić się przez miesiące lub lata po urodzeniu.
Najczęstszymi wczesnymi objawami zespołu Sheehana są agalactia, czyli brak laktacji. Z powodu długotrwałego braku estrogenów cykl menstruacyjny nie powraca we właściwym czasie po porodzie, gruczoły piersiowe zmniejszają się, a błona śluzowa pochwy staje się cieńsza. Niedobór gonadotropiny objawia się brakiem miesiączki, skąpym miesiączkowaniem i zmniejszonym libido. U niektórych kobiet miesiączka powraca i możliwa jest druga ciąża.
Charakterystyczne objawy niedoboru hormonu tyreotropowego w zespole Sheehana obejmują zmęczenie i upośledzoną termoregulację z nietolerancją zimna; suchą skórę, wypadanie włosów i łamliwe paznokcie; zaparcia i przyrost masy ciała. Objawy te zwykle rozwijają się stopniowo.
Konsekwencje niedoboru somatotropiny ograniczają się do pewnej utraty siły mięśniowej, wzrostu tkanki tłuszczowej i zwiększonej wrażliwości na insulinę. Zarówno w ostrej, jak i przewlekłej postaci mogą występować objawy moczówki prostej: intensywne pragnienie i zwiększona diureza (objętość moczu).
Objawy zespołu Sheehana obejmują również oznaki wtórnej niewydolności nadnerczy, tj. niedobór ACTH. Obejmuje to obniżony ogólny tonus i utratę wagi, hipoglikemię (niski poziom cukru we krwi), anemię i hiponatremię (niski poziom sodu). Niedobór tego hormonu prowadzi do przewlekłego niedociśnienia z omdleniami i niedociśnieniem ortostatycznym oraz niezdolnością do reagowania na stres. Obserwuje się również hipopigmentację i fałdy skóry (kilka tygodni lub miesięcy po urodzeniu).
Do zaostrzenia niewydolności nadnerczy, wymagającego natychmiastowej interwencji lekarskiej, dochodzi w przypadku ciężkich zakażeń lub interwencji chirurgicznej.
Komplikacje i konsekwencje
Ciężka niewydolność przysadki mózgowej w zespole Sheehana może prowadzić do śpiączki i śmierci.
Mniej powszechny jest również potencjalnie zagrażający życiu poporodowy panhypopituitaryzm, gdy dotknięte jest 90% tkanki przysadki mózgowej. Konsekwencje i powikłania tej ciężkiej postaci zespołu Sheehana obejmują: utrzymujące się niskie ciśnienie krwi, arytmię serca, niski poziom cukru we krwi (hipoglikemię) i niedokrwistość hipochromiczną.
Diagnostyka Zespół Sheehana
Zazwyczaj diagnoza zespołu Sheehana opiera się na cechach klinicznych i historii medycznej pacjentki, w szczególności na tym, czy wystąpiło krwawienie podczas porodu lub jakiekolwiek inne powikłania związane z porodem. Informacje dotyczące problemów z laktacją lub braku miesiączki po porodzie to dwa ważne objawy tego zespołu.
Badania krwi należy wykonać w celu sprawdzenia poziomu hormonów przysadki mózgowej (TSH, ACTH, FSH, LH, T4), kortyzolu i estradiolu.
Diagnostyka instrumentalna – wykorzystująca tomografię komputerową (TK) lub obrazowanie metodą rezonansu magnetycznego (MRI) mózgu – pozwala nam zbadać wielkość i strukturę przysadki mózgowej. We wczesnych stadiach przysadka mózgowa jest powiększona, z czasem gruczoł zanika, a następnie rozwija się diagnostyczny objaw patologii, taki jak „puste siodło tureckie”, które ujawnia się podczas skanowania, tj. brak przysadki mózgowej w dole kostnym przysadki u podstawy mózgu.
Diagnostyka różnicowa
Zadaniem diagnostyki różnicowej jest identyfikacja innych chorób, które objawiają się niedoczynnością przysadki: gruczolaków przysadki, kraniofaryngiomów, oponiaków, struniaków, wyściółczaków lub glejaków.
Przysadka mózgowa może zostać uszkodzona przez ropień mózgu, zapalenie opon mózgowych, zapalenie mózgu, neurosarkoidozę, histiocytozę, hemochromatozę, autoimmunologiczne lub limfoblastyczne zapalenie przysadki mózgowej i autoimmunologiczny zespół antyfosfolipidowy.
Z kim się skontaktować?
Leczenie Zespół Sheehana
Leczenie zespołu Sheehana polega na dożywotniej terapii hormonalnej z zastosowaniem syntetycznych analogów hormonów tropowych jajników, tarczycy i kory nadnerczy.
W ten sposób niedobór ACTH i kortyzolu jest kompensowany przez przyjmowanie glikokortykoidów (hydrokortyzonu lub prednizolonu). Preparaty tyroksyny (lewotyroksyna, tetrajodotyronina itp.) zastępują hormon tarczycy, a dane z badań krwi dotyczące poziomu wolnej tyroksyny w surowicy pomagają dostosować ich dawkowanie.
Niedobór estrogenu zazwyczaj koryguje się za pomocą doustnych środków antykoncepcyjnych, a kobiety z zespołem Sheehana muszą przyjmować te hormony aż do menopauzy.
Endokrynolodzy zauważają, że jeśli kontroluje się poziom hormonów we krwi, zazwyczaj nie występują żadne skutki uboczne. Skutki uboczne mogą wystąpić, gdy dawka leków hormonalnych jest zbyt wysoka lub zbyt niska. Dlatego pacjenci z tym zespołem są monitorowani, poddawani regularnym badaniom i mają wykonywane badania krwi na obecność hormonów.


 [
[