Ekspert medyczny artykułu
Nowe publikacje
Malaria
Ostatnia recenzja: 04.07.2025

Cała zawartość iLive jest sprawdzana medycznie lub sprawdzana pod względem faktycznym, aby zapewnić jak największą dokładność faktyczną.
Mamy ścisłe wytyczne dotyczące pozyskiwania i tylko linki do renomowanych serwisów medialnych, akademickich instytucji badawczych i, o ile to możliwe, recenzowanych badań medycznych. Zauważ, że liczby w nawiasach ([1], [2] itd.) Są linkami do tych badań, które można kliknąć.
Jeśli uważasz, że któraś z naszych treści jest niedokładna, nieaktualna lub w inny sposób wątpliwa, wybierz ją i naciśnij Ctrl + Enter.
Malaria (ang. malaria; fr. paludisme) jest ostrą antropogeniczną chorobą pierwotniakową, przenoszoną drogą płciową, o przenośnym mechanizmie zakażenia, charakteryzującą się wyraźnymi objawami zatrucia, cyklicznym przebiegiem z naprzemiennymi atakami gorączki i okresami gorączki, powiększeniem śledziony i wątroby, rozwojem niedokrwistości hemolitycznej o przebiegu progresywnym i nawrotami choroby.
Epidemiologia
Źródłem czynnika zakaźnego jest osoba chora lub nosiciel pasożyta, którego krew zawiera gametocyty. Malaria jest chorobą zakaźną przenoszoną przez ukąszenie komara. Gametocyty P. vivax, P. ovale i P. malariae znajdują się we krwi w pierwszych dniach choroby; ich liczba wzrasta po kilku cyklach schizogonii erytrocytarnej. Po zakażeniu P. falciparum osoba staje się źródłem zakażenia 10-12 dni po wystąpieniu pasożytemii i może pozostać nim przez 2 miesiące lub dłużej.
W przypadku malarii możliwe są różne mechanizmy przenoszenia zakażenia:
Mechanizm transmisji (ukąszenie komara)
Ten mechanizm jest głównym, zapewniającym istnienie zarodźca jako gatunku biologicznego. Źródłem zakażenia jest człowiek (chory na malarię lub nosiciel pasożyta), we krwi którego znajdują się dojrzałe gametocyty (męskie i żeńskie komórki rozrodcze pasożyta). Nosicielami malarii są wyłącznie samice komarów z rodzaju Anopheles.
W żołądku komara, do którego wraz z krwią dostają się męskie i żeńskie gametocyty wewnątrz erytrocytów, następuje ich dalsze dojrzewanie (po lizie erytrocytów), fuzja i wielokrotny podział z utworzeniem sporozoitów, które gromadzą się w gruczołach ślinowych komara. Bezpłciowe formy pasożyta (trofozoity, schizonty), po dostaniu się do żołądka komara, giną.
W organizmie człowieka zachodzi więc bezpłciowa droga rozwoju pasożytów (schizogonia), z powstawaniem i gromadzeniem gametocytów, a w organizmie komara następuje droga płciowa (sporogonia), czyli łączenie się gametocytów męskich i żeńskich z dalszym ich rozwojem i powstawaniem sporozoitów.
 [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ]
[ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ]
Mechanizm transmisji pionowej
Mechanizm transmisji pionowej (z matki na płód) lub z matki na noworodka (podczas porodu - mechanizm pozajelitowy). Przy transmisji pionowej płód rzadko zakaża się przez łożysko. Częściej do zakażenia dochodzi podczas porodu, gdy pewna ilość krwi matki przedostaje się do krwiobiegu noworodka, w erytrocytach których znajdują się bezpłciowe formy pasożyta.
Mechanizm transmisji pozajelitowej
Pozajelitowy mechanizm zakażenia prowadzi do rozwoju tzw. malarii schizontowej. Realizuje się ona podczas transfuzji krwi lub, rzadziej, podczas naruszenia aseptyki podczas iniekcji (np. u narkomanów stosujących tę samą strzykawkę). W przypadku zakażenia podczas transfuzji krwi źródłem zakażenia jest nosiciel-dawca-pasożyt, często z sublatentną parazytemią (liczba pasożytów wynosi mniej niż pięć w jednym μl krwi). Dlatego w regionach świata endemicznych dla malarii konieczne jest stosowanie, obok metod parazytologicznych (wykrywanie pasożyta w preparatach o gęstej kropli i rozmazach krwi), serologicznych (immunologicznych) metod diagnostyki laboratoryjnej malarii (RNIF, ELISA itp.) do kontroli krwi dawców. Biorąc pod uwagę, że przy zakażeniu pozajelitowym zwykle wprowadza się tylko niewielką ilość pasożytów (szczególnie przy zastrzykach), okres inkubacji może wydłużyć się do 3 miesięcy (przy masywnym zakażeniu okres inkubacji może być natomiast bardzo krótki – kilka dni), co jest istotne przy diagnozowaniu malarii u pacjentów, którzy przeszli operacje oraz u narkomanów.
Warunki rozprzestrzeniania się malarii
Aby malaria mogła się rozprzestrzenić w danym regionie (kraju, terytorium, obszarze), konieczne jest spełnienie następujących warunków:
- Źródło zakażenia (pacjent chory na malarię lub nosiciel pasożyta).
- Obecność skutecznego nosiciela (komary z rodzaju Anopheles). Podatność na pasożyty malaryczne jest główną cechą konkretnego gatunku komarów z rodzaju Anopheles. Liczba komarów z rodzaju Anopheles wśród populacji innych gatunków nie jest tak duża jak komarów niemalarycznych i rzadko poważnie dokuczają swoim ukąszeniom. Jednak nawet małe gatunki w innych sprzyjających okolicznościach (bliskość miejsc rozrodu komarów do siedzib ludzkich) mogą odgrywać dość poważną rolę. Ponad 70 gatunków komarów z rodzaju Anopheles (spośród ponad 200 znanych gatunków) może służyć jako skuteczni nosiciele malarii.
- Sprzyjające warunki klimatyczne: średnia dzienna temperatura powietrza powyżej 16 °C i obecność miejsc rozrodu komarów: zbiorniki wodne, zbiorniki wodne, konstrukcje irygacyjne itp. Minimalna średnia dzienna temperatura powietrza wymagana do rozwoju w ciele komara Pl. vivax wynosi 16 °C, dla Pl. falciparum - 18 °C, przy niższej temperaturze sporogonia nie występuje. Czas trwania sporogoni jest krótszy, im wyższa temperatura (do pewnego poziomu, ponieważ średnia dzienna temperatura 30 °C i powyżej jest niekorzystna dla sporogoni). Przy optymalnej średniej dziennej temperaturze (25-26 °C) sporogonia u Pl. vivax trwa 8-9 dni, u Pl. falciparum - 10-11 dni.
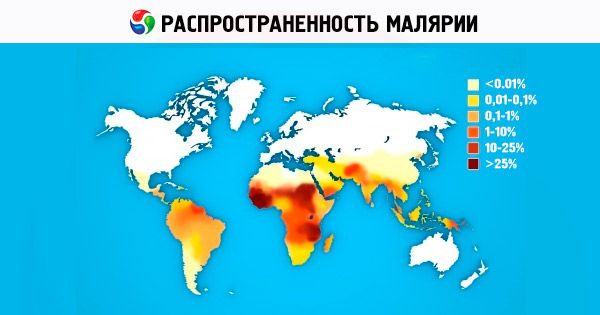
Cały obszar występowania malarii na kuli ziemskiej (od 45° N do 40° S do 64° N i 45° S w różnych latach) jest zajęty przez malarię vivax. Obszary występowania malarii falciparum i malariae są nieco mniejsze ze względu na wyższą temperaturę wymaganą do skutecznej sporogonii; obszar występowania malarii ovale znajduje się w dwóch regionach, które nie są ze sobą terytorialnie połączone: tropikalnej Afryce i państwach zachodniej części Oceanu Spokojnego (Indonezja, Wietnam, Filipiny, Nowa Gwinea itp.). W krajach górzystych ogniska malarii mogą tworzyć się na wysokościach do 1000 m w strefie klimatu umiarkowanego i do 1500-2500 m w strefie subtropikalnej i tropikalnej, przy czym ogniska tylko malarii vivax występują na dużych wysokościach (1000-1500 m i wyżej).
Malaria charakteryzuje się wyraźną sezonowością. W klimacie umiarkowanym i subtropikalnym sezon malaryczny dzieli się na okresy skutecznego zakażenia komarami, transmisji zakażenia i masowych objawów choroby. Początek okresu skutecznego zakażenia komarami (w obecności źródła zakażenia - pacjentów, nosicieli pasożytów) pokrywa się z momentem stabilnego wzrostu średniej dobowej temperatury do 16 °C. Początek okresu transmisji wiąże się z zakończeniem sporogonii w ciele komara, co zależy od konkretnych średnich dobowych temperatur danego roku. W obwodzie moskiewskim okres transmisji malarii vivax może sięgać 1,5-2 miesięcy lub więcej, do pierwszych jesiennych przymrozków. Granice okresu masowych objawów są mniej określone. W ogniskach, w których przenoszona jest tylko trzydniowa malaria, masowa zachorowalność może rozpocząć się na długo przed rozpoczęciem okresu transmisji. Obserwowane przypadki to pierwotne objawy malarii vivax z długim okresem inkubacji (3-10 miesięcy) z powodu zakażenia w poprzednim sezonie i utrzymywania się hipnozoitów w wątrobie (bez pierwotnych objawów z krótkim okresem inkubacji), a także odległe nawroty pozakrwinkowe (po serii ataków malarii z krótkim okresem inkubacji w poprzednim sezonie, bez odpowiedniego leczenia antyrefleksyjnego).
Podatność na malarię jest powszechna. Wynik zakażenia po przedostaniu się patogenu do krwiobiegu i przebieg kliniczny choroby są determinowane przez indywidualny stan immunologiczny, aktywność nieswoistych czynników oporności wrodzonej, intensywność odporności poinfekcyjnej, a w przypadku noworodków - poziom swoistych przeciwciał klasy G otrzymanych od matki. Wyjątkiem są rdzenni mieszkańcy Afryki Zachodniej i Nowej Gwinei, którzy są w większości odporni na zakażenie Pl. vivax, co wiąże się z genetycznie uwarunkowanym brakiem izoantygenów erytrocytów grupy Duffy, które działają jako receptory dla merozoitów Pl. vivax. W związku z tym w tym regionie przypadki zakażenia malarią vivax obserwuje się znacznie rzadziej niż w innych regionach tropikalnej Afryki.
Osoby, które są nosicielami nieprawidłowej hemoglobiny (talasemia, niedokrwistość sierpowatokrwinkowa, hemoglobina E, C itp.), z nieprawidłowościami w budowie cytoszkieletu erytrocytów (sferocytoza dziedziczna, owalocytoza południowo-wschodnia, eliptocytoza dziedziczna) lub które mają niedobór enzymu dehydrogenazy glukozo-6-fosforanowej erytrocytów, mają względną odporność na zakażenie wszystkimi typami malarii. W przypadku zakażenia malarią są łagodni, liczba pasożytów we krwi pozostaje na stosunkowo niskim poziomie, a przypadki postępu złośliwego (malaria mózgowa - falciparum) są praktycznie nieobecne. Z drugiej strony osoby z niedoborem dehydrogenazy glukozo-6-fosforanowej są narażone na rozwój ostrej hemolizy podczas stosowania szeregu leków przeciwmalarycznych (prymachina, chinina itp.). Mechanizmy naturalnej odporności na różne typy malarii są nadal w dużej mierze niejasne i nadal są badane.
Noworodki mają również pewną odporność na zakażenie wszystkimi formami malarii. Jest to spowodowane:
- obecność odporności biernej spowodowanej przeciwciałami klasy G, które noworodek otrzymał od matki hiperimmunizowanej (na obszarach o dużej zapadalności na malarię);
- utrzymanie swoistej odporności po urodzeniu dzięki przeciwciałom klasy A, które noworodek otrzymuje z mlekiem matki;
- obecność hemoglobiny płodowej u noworodka, która jest mało przydatna jako pokarm dla pasożyta wywołującego malarię.
Po upływie pierwszych trzech do sześciu miesięcy życia u noworodków znacznie wzrasta ryzyko wystąpienia ciężkich, złośliwych postaci malarii falciparum (zamiana czerwonych krwinek zawierających hemoglobinę płodową na czerwone krwinki zawierające prawidłową hemoglobinę; przejście na karmienie mieszane - pobieranie kwasu paraaminobenzoesowego, niezbędnego do rozwoju pasożyta, którego nie ma w mleku matki).
 [ 10 ], [ 11 ], [ 12 ], [ 13 ]
[ 10 ], [ 11 ], [ 12 ], [ 13 ]
Odporność w malarii
Odporność na malarię jest niesterylna, specyficzna dla gatunku i szczepu, niestabilna i krótkotrwała. Aby utrzymać ochronny poziom przeciwciał, konieczna jest stała stymulacja antygenowa w postaci powtarzających się zakażeń malarią. Odporność na Pl. malariae i Pl. vivax powstaje wcześniej i utrzymuje się dłużej niż na Pl. falciparum. Odporność przeciwmalaryczna obejmuje odpowiedzi komórkowe i humoralne. Procesy immunologiczne, które stymulują syntezę przeciwciał, rozpoczynają się od fagocytozy pasożytów malarii przez makrofagi. Objawia się to hiperplazją układu histiofagocytarnego śledziony, wątroby i szpiku kostnego.
Występowanie malarii
Spośród czterech gatunków ludzkich patogenów malarii, P. vivax jest najpowszechniejszy na świecie. W strefie subtropikalnej i tropikalnej w puli genowej populacji P. vivax dominują sporozoity. Wywołują chorobę po krótkiej inkubacji (10-21 dni). Na kontynencie afrykańskim P. vivax jest stale spotykany w krajach Afryki Wschodniej wśród Arabów, Hindusów, Etiopczyków i Europejczyków. W krajach Afryki Zachodniej, które zamieszkują głównie przedstawiciele rasy negroidalnej, P. vivax nie występuje, co tłumaczy się genetycznie uwarunkowaną wrodzoną odpornością murzynów afrykańskich na P. vivax [erytrocyty nie posiadają receptora dla merozoitów P. vivax - izoantygenów Duffy'ego (Fy d lub Fy b )]. Zasięg P. ovale jest niewielki i składa się z dwóch części. Główna, afrykańska część zajmuje tropikalną Afrykę od Gambii na północy do Kongo na południu kontynentu. Drugą część zasięgu stanowią kraje zachodniego Oceanu Spokojnego i Azji Południowo-Wschodniej. Zasięg geograficzny malarii tropikalnej sięga 40° szerokości geograficznej północnej i 20° szerokości geograficznej południowej. P. falciparum powoduje do 50% przypadków malarii na świecie. Czterodniowa malaria występuje obecnie w Afryce, niektórych obszarach Ameryki Środkowej i Południowej oraz na Karaibach. Azja Południowo-Wschodnia.
Większość ludzi jest podatna na malarię. Wyjątkiem jest rdzenna populacja Afryki Zachodniej. Obszary hiperendemiczne tropikalnej Afryki, gdzie dominuje P. falciparum, charakteryzują się stosunkowo stabilną strukturą odpornościową rdzennej populacji:
- Dzieci poniżej 6 miesiąca życia nie chorują ze względu na odporność bierną otrzymaną od matki:
- Większość dzieci w wieku od 6 do 24 miesięcy jest zarażona P. falciparum; odporność bierna jest osłabiona, odporność czynna jeszcze się nie rozwinęła; w tej grupie odnotowuje się najwyższą śmiertelność z powodu malarii:
- U dzieci powyżej 2 roku życia P. falciparum wykrywa się rzadziej, przebieg malarii jest łagodzony w wyniku nabytej odporności, a nasilenie pasożytemii zmniejsza się wraz z wiekiem:
- U dorosłych osobników P. falciparum jest rzadko wykrywane ze względu na wysokie napięcie układu odpornościowego; po zakażeniu nie występują żadne objawy kliniczne.
Malaria tropikalna jest również dobrze tolerowana przez nosicieli nieprawidłowej hemoglobiny S (niedokrwistość sierpowatokrwinkowa) oraz osoby z pewnymi innymi genetycznie uwarunkowanymi nieprawidłowościami hemoglobiny i enzymów czerwonych krwinek (niedobór G-6-PDH).
Historia badań nad malarią
Badania nad malarią (jedną z najstarszych chorób człowieka) są nierozerwalnie związane z historią ludzkiej cywilizacji. Przyjmuje się, że malaria zaczęła rozprzestrzeniać się na Ziemi (z regionu afrykańskiego Morza Śródziemnego) około 10 000 lat temu w wyniku intensywnego rozwoju rolnictwa, handlu i eksploracji nowych ziem. W starożytnych egipskich papirusach, starożytnej literaturze chińskiej i kanonach klasycznej starożytnej medycyny indyjskiej (ajurwedy) do dziś przetrwały opisy obrazu klinicznego i epidemii malarii; nawet wtedy zakładano możliwy związek między rozwojem choroby a ukąszeniami komarów. Później (V-VI w. p.n.e.) starożytni greccy lekarze: Hipokrates, Heradotus, Empedokles opisali obraz kliniczny malarii szczegółowo. Za twórcę odróżnienia malarii od grupy chorób gorączkowych uważa się Hipokratesa, który zaproponował rozróżnienie 3 postaci choroby: „codziennej” (ataki codzienne), „tertiannej” (ataki co drugi dzień) i „kwartannej” (ataki co 2 dni).
Początek ery odkryć naukowych w badaniu malarii wiąże się z rokiem 1640, kiedy to hiszpański lekarz i konkwistador Juan del Vego po raz pierwszy zastosował napar z kory chinowca do leczenia pacjentów z malarią, wcześniej stosowany przez Indian z Peru i Ekwadoru jako środek przeciwgorączkowy. Zasługa nadania chorobie nazwy „malaria” (wł. „mal aria” – złe powietrze) przypada Włochowi Lancisi (1717), który powiązał zarażenie ludzi malarią poprzez „trujące” opary z bagien. W 1880 roku francuski lekarz A. Laveran, pracujący w Algierii, szczegółowo opisał morfologię patogenu malarii. W 1897 roku angielski lekarz wojskowy Ronald Ross w Indiach ustalił mechanizm przenoszenia malarii.
Obecnie malaria jest jednym z najpoważniejszych problemów zdrowotnych w ponad 100 krajach Afryki, Azji i Ameryki Południowej, około połowa światowej populacji żyje narażona na zarażenie się malarią. Prawie wszystkie kraje w Europie i Ameryce Północnej co roku rejestrują setki przypadków zawleczonych malarii wśród osób przybywających z regionów, w których jest ona szeroko rozpowszechniona, liczba przypadków tzw. malarii lotniskowej rośnie. Według WHO, co roku na malarię zapada 200-250 milionów ludzi na świecie, co najmniej 80% wszystkich przypadków malarii rejestruje się w krajach afrykańskich położonych na południe od Sahary. Co roku na malarię umiera od 1 do 2 milionów osób, głównie dzieci poniżej 5 roku życia. Straty społeczne i ekonomiczne w samej Afryce szacuje się na 2 miliardy dolarów rocznie. Od 1998 roku pod auspicjami WHO, Banku Światowego i UNICEF-u realizowany jest naukowo-praktyczny program (Roll Back Malaria Initiative) dotyczący zwalczania malarii (głównie w krajach rozwijających się). Program ma trwać do 2010-2015 r. Prace nad stworzeniem skutecznej szczepionki przeciwmalarycznej są w toku, ale zajmie to co najmniej kolejne 10-15 lat. Poszukiwanie, opracowywanie i udoskonalanie leków na malarię to jeden z priorytetowych programów WHO, różnych firm farmaceutycznych i instytutów badawczych na całym świecie. W ostatnich latach Rosja odnotowała wzrost liczby przypadków malarii importowanej w wyniku zwiększonej migracji i intensywnego rozwoju turystyki międzynarodowej.
Przyczyny malaria
Nazwa choroby „malaria” w rzeczywistości uogólnia cztery odrębne choroby pierwotniakowe, wywoływane odpowiednio przez cztery rodzaje patogenów.
Malarię wywołują pasożyty należące do typu Protozoa, klasy Sporozoa, rodziny Plasmodiidae, rodzaju Plasmodium. Cztery typy patogenu pasożytują na ludziach: P. vivax wywołuje malarię trzydniową, P. malariae wywołuje malarię czterodniową, P. falciparum wywołuje malarię tropikalną; P. ovale wywołuje malarię trzydniową ovale.
Patogeny malarii
Wzbudnica |
Postać malarii (według ICD-10) |
Plasmodium (Laverania) falciparum |
Malaria wywołana przez Plasmodium falciparum (malaria falciparum) |
Plasmodium (Plasmodium) vivax |
Malaria wywołana przez Plasmodium vivax (malaria-vivax) |
Plasmodium (Plasmodium) owalne |
Malaria wywołana przez Plasmodium ovale (malaria ovale) |
Malaria Plasmodium (Plasmodium). |
Malaria wywołana przez Plasmodium malariae (malaria-malariae) |
W większości krajowych publikacji (podręczników, instrukcji, książek informacyjnych) zachowano dotychczasowe nazwy postaci malarii: malaria tropikalna (malaria-falciparum), malaria trzydniowa (malaria-vivax), malaria owalna (malaria-ovale) i malaria czterodniowa (malaria-malariae).
Każda z czterech postaci malarii charakteryzuje się własnymi cechami klinicznymi, patogenetycznymi i epidemiologicznymi. Najważniejsze miejsce zajmuje malaria falciparum, która stanowi 80-90% wszystkich przypadków malarii na świecie, a jej czynnik sprawczy należy do specjalnego podrodzaju (Laverania). Tylko malaria falciparum może przebiegać złośliwie, prowadząc do zgonu.
W trakcie cyklu życiowego patogeny malarii przechodzą następujący cykl rozwojowy, zmieniając żywiciela:
- rozwój bezpłciowy (schizogonia) zachodzi w organizmie żywiciela pośredniego – człowieka;
- Rozwój płciowy (sporogonia) zachodzi w ciele żywiciela ostatecznego – samicy komara z rodzaju Anopheles.
Sporozoity dostają się do organizmu człowieka poprzez ukąszenie zarażonego komara malarii. Po przedostaniu się do krwi sporozoity wnikają do hepatocytów z naczyń zatokowych wątroby w ciągu 15-45 minut i rozpoczynają cykl egzoerytrocytarny (schizogonia tkankowa). Selektywność i szybkość inwazji wynikają z obecności specyficznych receptorów na błonach hepatocytów. Pasożyty zwiększają swoje rozmiary, dzielą się wielokrotnie i tworzą wiele małych jednojądrowych formacji - merozoitów. Minimalny czas trwania cyklu egzoerytrocytarnego wynosi 5-7 dni dla P. falciparum, 6-8 dni dla P. vivax, 9 dni dla P. ovale i 14-16 dni dla P. malariae. Następnie merozoity opuszczają hepatocyty do krwi i wnikają do erytrocytów, gdzie zachodzi schizogonia erytrocytów. Malaria trzydniowa i owalna charakteryzują się szczególnym typem rozwoju pozakrwinkowego: wszystkie pasożyty lub niektóre z nich są zdolne do przebywania w hepatocytach przez długi czas (7-14 miesięcy i więcej) w stanie „uśpienia” (hipnozoity), a dopiero po tym okresie zaczynają przekształcać się w merozoity zdolne do zakażania erytrocytów. Stwarza to możliwość długotrwałej inkubacji i występowania odległych nawrotów do 3 lat.
Schizogonia erytrocytów wiąże się z cyklicznym rozwojem i wielokrotnym podziałem pasożytów, przy czym malaryczne zarodźce przechodzą przez następujące stadia: młody trofozoit (ma kształt pierścienia); rozwijający się trofozoit; dojrzały trofozoit (ma duże jądro): rozwijający się schizont; dojrzały schizont. Po zakończeniu procesu schizogonii erytrocyt ulega zniszczeniu. Wolne merozoity aktywnie wnikają do nowych erytrocytów, ale większość z nich ginie w wyniku działania ochronnych mechanizmów immunologicznych gospodarza. Czas trwania schizogonii erytrocytów wynosi 48 godzin u P. vivax, P. ovale, P. falciparum i 72 godziny u P. malariae. Podczas cyklu erytrocytów niektóre merozoity przekształcają się w formy płciowe - żeńskie (makrogametocyty) lub męskie (mikrogametocyty).
Gametocyty dostają się do organizmu komara-nosiciela, gdy ten żywi się krwią chorego na malarię lub nosiciela pasożyta. zawierające dojrzałe gametocyty. W żołądku komara, po 9-12 minutach, męski gametocyt wyrzuca osiem cienkich, ruchomych wici. Wolne wici (mikrogamety) wnikają do komórki żeńskiej (makrogamety); po połączeniu jąder powstaje zygota - okrągła zapłodniona komórka. Następnie kolejno rozwijają się ookinety, oocysty ze sporozoitami, ich dojrzewanie następuje w gruczołach ślinowych komara. W optymalnej temperaturze powietrza otoczenia (25 °C), sporogonia trwa 10 dni u P. vivax, 12 dni u P. falciparum, 16 dni u P. malariae i P. ovale; w temperaturze powietrza poniżej 15 °C sporozoity nie rozwijają się.
Patogeneza
Wszystkie objawy malarii są spowodowane schizogonią erytrocytarną - wzrostem i rozmnażaniem bezpłciowych form erytrocytarnych pasożyta we krwi. Schizogonia tkankowa nie objawia się klinicznie.
Atak malaryczny wiąże się z zakończeniem schizogonii erytrocytowej, masowym rozpadem erytrocytów i przedostaniem się do krwi dużej liczby merozoitów, produktów przemiany materii pasożytów o właściwościach pirogenne i toksyczne, które wywołują rozwój reakcji gorączkowej. Ze względu na cykliczny charakter schizogonii erytrocytowej ataki gorączkowe powtarzają się co 48 godzin w malarii trzydniowej, owalnej i tropikalnej oraz co 72 godziny w malarii czterodniowej. Kiedy człowiek jest zarażony, do organizmu wnika heterogenna populacja pasożytów malarii, a schizogonia w początkowym okresie zachodzi asynchronicznie, przez co rodzaj gorączki może być nieregularny. W miarę rozwoju reakcji immunologicznych zdolność pasożytowania w erytrocytach jest zachowana w jednym głównym pokoleniu plazmodia, co determinuje rytm gorączkowy charakterystyczny dla tego gatunku. Tylko w przypadku malarii tropikalnej mogą występować liczne (2-3) główne pokolenia zarodźców, dlatego gorączka jest często nieregularna.
Niedokrwistość, charakterystyczna dla malarii, jest konsekwencją niszczenia czerwonych krwinek przez pasożyty w nich znajdujące się. Wiadomo, że P. vivax i P. ovale wnikają głównie do młodych czerwonych krwinek, P. malariae - do dojrzałych. P. falciparum zakaża czerwone krwinki o różnym stopniu dojrzałości, co przyczynia się do ich większego uszkodzenia i hemolizy, dlatego w malarii tropikalnej hemoliza odgrywa wiodącą rolę w genezie niedokrwistości. Dodatkowymi czynnikami w hemolizie czerwonych krwinek są również mechanizmy autoimmunologiczne, które uszkadzają niezainfekowane czerwone krwinki. Rozwijająca się w malarii hiperplazja elementów siateczkowo-śródbłonkowych śledziony hamuje hematopoezę, co nasila niedokrwistość i trombocytopenię.
Powiększenie wątroby i śledziony jest początkowo spowodowane przekrwieniem narządów, ale wkrótce dochodzi w nich do przerostu limfoidalnego i siateczkowo-śródbłonkowego. W wyniku hemolizy erytrocytów, a także uszkodzenia hepatocytów, rozwija się żółtaczka. Spadek wchłaniania węglowodanów i zahamowanie glukoneogenezy w wątrobie powoduje hipoglikemię. Aktywacja glikolizy beztlenowej prowadzi do gromadzenia się mleczanu we krwi, płynie mózgowo-rdzeniowym i wystąpienia kwasicy mleczanowej, która jest jedną z przyczyn ciężkiej malarii tropikalnej.
W malarii tropikalnej zmieniają się właściwości erytrocytów, co powoduje zaburzenie mikrokrążenia (cytoadhezja, sekwestracja, rozeta). Cytoadhezja to przyleganie zakażonych erytrocytów do komórek śródbłonka, co jest przyczyną sekwestracji w naczyniach włosowatych i żyłkach pozawłośniczkowych. Główną rolę w cytoadhezji odgrywają specyficzne białka ligandowe (ich ekspresję na powierzchni erytrocytów indukuje pasożyt) oraz receptory zlokalizowane na zewnętrznej powierzchni komórek śródbłonka. Zamknięcie naczyń krwionośnych powoduje niedokrwienie dotkniętych narządów. Na błonach erytrocytów pojawiają się wypukłości (guzki), które stykają się z pseudopodiowymi wyrostkami utworzonymi na komórkach śródbłonka. Niektóre odmiany P. falciparum powodują przyleganie zdrowych erytrocytów do zakażonych, co powoduje tworzenie się „rozet”. Czerwone krwinki stają się sztywne, co pogarsza właściwości reologiczne krwi i nasila zaburzenia mikrokrążenia. Ważnym czynnikiem uszkadzającym jest niedotlenienie spowodowane niewystarczającą funkcją transportu tlenu przez zakażone czerwone krwinki. Tkanka mózgowa jest najmniej odporna na niedotlenienie, co przyczynia się do rozwoju malarii mózgowej. Występują zaburzenia w układzie krzepnięcia krwi: w ciężkiej malarii tropikalnej obserwuje się objawy zespołu DIC, trombocytopenii i hipofibrynogenemii. Pewną rolę w patogenezie malarii tropikalnej przypisuje się uogólnionej niespecyficznej reakcji zapalnej. Uszkodzenie naczyń jest spowodowane głównie działaniem mediatorów zapalnych. Najbardziej aktywne są produkty peroksydacji lipidów i proteazy wydzielane przez granulocyty. W patogenezie ciężkiej malarii znaczną uwagę zwraca się na cytokiny, w szczególności TNF i IL (IL-2 i IL-6). Najbardziej charakterystyczne zmiany w ciężkiej tropikalnej malarii występują w mózgu, gdzie obserwuje się obrzęk, puchnięcie substancji mózgowej, okołonaczyniowe i okołozwojowe rozrosty neuroglii (ziarniniaki Durka). Naczynia włosowate są blokowane przez zaatakowane erytrocyty i pasożyty; obserwuje się rozległą hemostazę. Rozwija się obrzęk okołonaczyniowy z krwotokami i ogniskową martwicą. Na podstawie obrazu patologicznego można wnioskować, że w przypadkach śpiączki malarycznej rozwija się specyficzne zapalenie opon mózgowo-rdzeniowych.
Zakażenie malarią może zaburzyć odpowiedź immunologiczną gospodarza, co wyzwala kaskadę reakcji immunopatologicznych. Wiązanie immunoglobulin i dopełniacza na błonach podstawnych kłębuszków nerkowych powoduje ostrą nefropatię. Zespół nerczycowy, który rozwija się u pacjentów z czterodniową malarią, jest klasyfikowany jako glomerulopatia kompleksów immunologicznych.
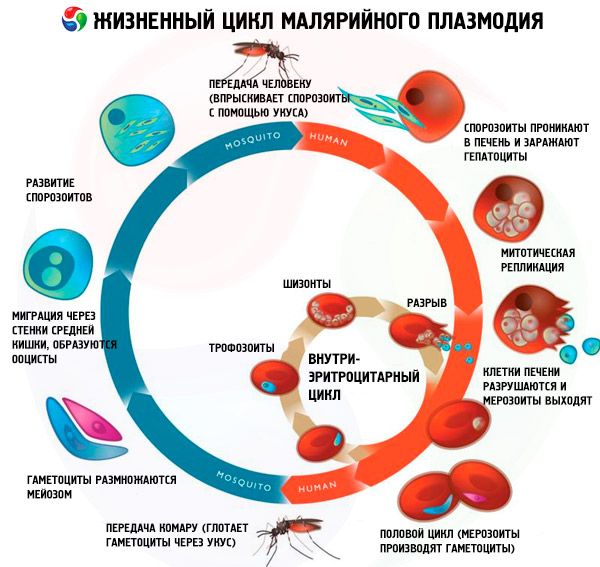
Cykl życia wszystkich patogenów malarii
Cykl życiowy wszystkich patogenów malarii obejmuje dwóch żywicieli: człowieka (schizogonia – cykl rozwoju bezpłciowego) i komary z rodzaju Anopheles (sporogonia – cykl rozwoju płciowego).
Tradycyjnie w cyklu schizogonii wszystkich gatunków pasożytów malarii wyróżnia się trzy stadia: schizogonię egzoerytrocytarną (EESh), schizogonię erytrocytarną (ESH) i gametocytogonię. Ponadto w cyklach życiowych Pl. vivax i Pl. ovale wyróżnia się osobne stadium - hibernację - ze względu na możliwość wprowadzenia do organizmu człowieka podczas ukąszenia komara morfologicznie heterogenicznej grupy sporozoitów (tachysporozoitów i bradysporozoitów lub tylko bradysporozoitów). W tych przypadkach bradysporozoity (hypnozoity) pozostają w hepatocytach przez długi czas w stanie nieaktywnym aż do wystąpienia EES.
 [ 19 ], [ 20 ], [ 21 ], [ 22 ]
[ 19 ], [ 20 ], [ 21 ], [ 22 ]
Schizogonia egzoerytrocytarna
Sporozoity wprowadzone do organizmu człowieka ze śliną komara bardzo szybko (w ciągu 15-30 minut) dostają się do wątroby z krwią, gdzie aktywnie wnikają do hepatocytów, nie uszkadzając ich. Sporozoity Pl. falciparum, Pl. malariae oraz tachysporozoity Pl. vivax i Pl. ovale natychmiast rozpoczynają EES z wytworzeniem dużej liczby merozoitów pozakrwinkowych (do 40 000 z jednego sporozoitu w malarii falciparum). Hepatocyty ulegają zniszczeniu, a merozoity ponownie dostają się do krwiobiegu z następową szybką (w ciągu 15-30 minut) penetracją do erytrocytów. Czas trwania EES dla malarii falciparum wynosi zwykle 6 dni, dla malarii vivax - 8 dni, dla malarii ovafe - 9 dni, dla malarii malariae - 15 dni.
 [ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ], [ 28 ], [ 29 ]
[ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ], [ 28 ], [ 29 ]
Faza uśpienia
W malarii vivax i ovale bradysporozoity, które wniknęły do hepatocytów, przekształcają się w formy nieaktywne - hypnozoity, które mogą pozostać bez podziału przez kilka miesięcy, a nawet lat, aż do późniejszej reaktywacji (podziału i powstania merozoitów). Zatem hypnozoity są związane z długą inkubacją (do 3-10 miesięcy lub więcej) i rozwojem odległych nawrotów pozakrwinkowych, które są charakterystyczne tylko dla tych postaci malarii.
Schizogonia erytrocytów
Po wprowadzeniu merozoitów do erytrocytów pasożyty malarii wielokrotnie (cyklicznie) sekwencyjnie przechodzą przez stadia: trofozoitu (odżywiającej się, jednojądrowej komórki), schizontu (dzielącej się komórki wielojądrowej) i moruli (uformowanego pasożyta zlokalizowanego wewnątrz erytrocytu). Następnie, po zniszczeniu erytrocytów, merozoity przedostają się do osocza krwi. Najwięcej potomnych merozoitów powstaje w malarii tropikalnej - do 40 w jednym erytrocycie. Stadium ES trwa ściśle określony czas: 48 godzin dla malarii falciparum, vivax, ovale i 72 godziny dla malarii.
Cechy cyklu schizogonii erytrocytowej i główne mechanizmy patogenetyczne rozwoju ciężkich i powikłanych postaci malarii falciparum:
- gromadzenie się (sekwestracja) zaatakowanych erytrocytów zawierających dorosłe trofozoity (od stadium trofozoitu ameboidalnego), schizontów w naczyniach narządów wewnętrznych, przede wszystkim mózgu, a także nerek, wątroby, jelit, szpiku kostnego, łożyska itp.;
- powstawanie tzw. rozet, składających się z erytrocytów zakażonych i niezakażonych;
- rozwój zaburzeń mikrokrążenia, niedotlenienie tkanek, kwasica metaboliczna (znaczne gromadzenie się kwasu mlekowego);
- aktywacja MFS (głównie odpowiedzi immunologicznej Th-1) ze zwiększoną syntezą czynnika martwicy nowotworu a, interferonu y, interleukiny-1 i innych cytokin, które uszkadzają śródbłonek naczyniowy i powodują przyleganie erytrocytów do śródbłonka naczyń krwionośnych.
W ostatnich latach zaczęto brać pod uwagę szczególną rolę zwiększonej syntezy tlenku azotu (NO) przez komórki śródbłonka naczyń mózgowych w rozwoju mózgowej postaci malarii falciparum.
Ważnym mechanizmem patofizjologicznym w rozwoju ciężkich postaci malarii falciparum, w porównaniu z innymi postaciami malarii, jest hipoglikemia, która nasila zaburzenia mikrokrążenia i metabolizmu (kwasica metaboliczna) u pacjentów, zwłaszcza u dzieci i kobiet w ciąży. Wyróżnia się trzy główne czynniki w rozwoju hipoglikemii w malarii falciparum: zmniejszona glukogeneza w wątrobie, wykorzystanie glukozy przez pasożyty i stymulacja wydzielania insuliny. Jednocześnie hipoglikemia może być konsekwencją hiperinsulinemii rozwijającej się po podaniu chininy w celu zatrzymania ataków malarii falciparum.
W wyniku długotrwałego utrzymywania się pasożyta (bez odpowiedniego leczenia) w przebiegu malarii-malariów może rozwinąć się zespół nerczycowy na skutek mechanizmu immunologicznego (odkładanie się kompleksów immunologicznych zawierających antygeny pasożyta na błonie podstawnej kłębuszków nerkowych).
Należy zauważyć, że główne objawy kliniczne wszystkich postaci malarii (zatrucie, powiększenie wątroby i śledziony, niedokrwistość) są związane ze stadium schizogonii erytrocytów (powtarzające się bezpłciowe rozmnażanie pasożytów w erytrocytach), a im wyższa zawartość pasożytów w 1 μl krwi pacjenta, oznaczona za pomocą mikroskopii grubego rozmazu krwi, tym zwykle cięższa jest malaria. Dlatego w diagnostyce laboratoryjnej malarii ważne jest nie tylko ustalenie rodzaju malarii malarycznej, ale także określenie poziomu parazytemii. Zgodnie z maksymalnym poziomem parazytemii postacie malarii są rozmieszczone w kolejności malejącej: malaria falciparum (do 100 tysięcy w μl lub więcej), malaria vivax (do 20 tysięcy w μl, rzadziej więcej), malaria ovale i malariae (do 10-15 tysięcy w μl). W przypadku malarii falciparum, przebiegającej z wysokim poziomem pasożytemii (100 tys. μl i więcej), ryzyko wystąpienia ciężkich, śmiertelnych powikłań znacznie wzrasta, co determinuje taktykę intensywnej (pozajelitowej) terapii przeciwmalarycznej.
Występowanie napadów gorączkowych w malarii jest spowodowane hemolizą erytrocytów, uwolnieniem merozoitów do osocza, zniszczeniem części z nich (druga część merozoitów zostaje ponownie wprowadzona do erytrocytów), aktywacją MFS i zwiększoną syntezą interleukiny-1, -6, czynnika martwicy nowotworu a i innych endogennych pirogenów (cytokin zapalnych), które wpływają na ośrodek termoregulacji podwzgórza.
W obecności jednego pokolenia plazmodia we krwi, regularnie naprzemiennie występują napady od pierwszych dni choroby. Często, w przypadku malarii falciparum i vivax (w regionach hiperendemicznych z intensywną transmisją malarii), osoby nieodporne doświadczają początkowej (rozpoczynającej) gorączki związanej z rozwojem kilku pokoleń patogenów w erytrocytach pacjentów jednocześnie z różnymi czasami końca cyklu rozwojowego, co prowadzi do warstwowania ataków, wygładzania okresu apireksji i zniekształcenia typowego napadu.
W miarę rozwoju choroby następuje wzrost swoistych i nieswoistych czynników obronnych (pod koniec 1-2 tygodnia), część pokoleń obumiera, a jedno (dwa) wiodące pokolenia pasożytów pozostają, rozwijając typowe napady co drugi dzień (lub codziennie).
Powiększenie wątroby i śledziony we wszystkich postaciach malarii wiąże się ze znacznym wypełnieniem ich krwią, obrzękiem i przerostem stawu przerzutowego.
Malaria z reguły zawsze prowadzi do niedokrwistości hemolitycznej niedobarwliwej, w patogenezie której istotne znaczenie ma szereg czynników:
- wewnątrznaczyniowa hemoliza zakażonych erytrocytów;
- fagocytoza zakażonych i niezakażonych erytrocytów przez komórki siateczkowo-śródbłonkowe śledziony;
- sekwestracja (gromadzenie) erytrocytów zawierających dojrzałe pasożyty w szpiku kostnym, zahamowanie hematopoezy;
- mechanizm immunologiczny (niszczenie nieuszkodzonych erytrocytów w wyniku adsorpcji kompleksów immunologicznych zawierających frakcję C-3 dopełniacza na błonie erytrocytu).
Stadium gametocytogonii jest swego rodzaju odgałęzieniem stadium ES. Część merozoitów (genetycznie uwarunkowany proces) zamiast powtarzać bezpłciowy cykl rozwojowy po wprowadzeniu do erytrocytu, przekształca się w formy płciowe - gametocyty (męskie i żeńskie).
Cechy stadium gametocytogoniów w malarii falciparum:
- gametocyty pojawiają się we krwi obwodowej nie wcześniej niż 10-12 dnia choroby;
- Gametocyty, gromadzące się w trakcie trwania choroby, mogą krążyć we krwi przez długi czas (nawet 4-6 tygodni i dłużej).
W przypadku innych postaci malarii (vivax, ovale, malariae) gametocyty można wykryć we krwi obwodowej już w pierwszych dniach choroby, a następnie szybko (w ciągu kilku godzin lub dni) obumierają.
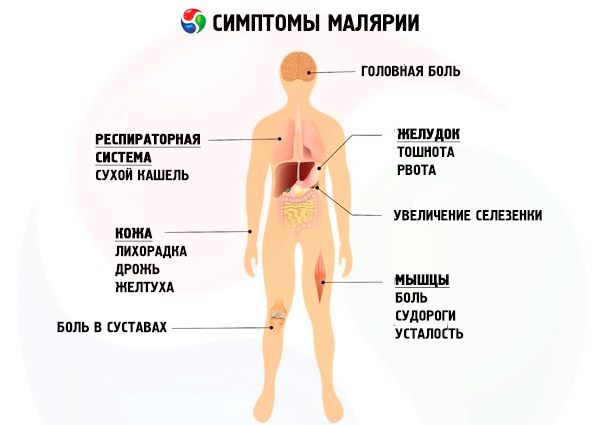
Objawy malaria
Biorąc pod uwagę cechy gatunkowe zarodźców malarii i odpowiadające im objawy malarii, wyróżnia się cztery postacie tej choroby: malaria trzydniowa (vivax-malaria, malaria tertiana), malaria czterodniowa (malaria quartana), malaria tropikalna (falciparum-malaria, malaria tropica), malaria owalna trzydniowa (ovale-malaria).
Przebieg pierwotnej malarii obejmuje początkowy okres choroby, okres szczytu choroby i rekonwalescencję. Bez leczenia lub przy niewystarczającej terapii etiotropowej malaria przechodzi w okres nawrotu. Wyróżnia się nawroty egzoerytrocytarne i erytrocytarne, w zależności od czasu rozwoju - wczesne i późne. Nawroty erytrocytarne obserwuje się przy zakażeniu wszystkimi typami malarii. Wczesne występują w ciągu 2 miesięcy od pierwotnych ataków; nawroty, które rozwijają się w późniejszym terminie, uważa się za późne. Bez leczenia lub przy niewłaściwym leczeniu malarii trzydniowej i owalnej następuje „cisza” trwająca 6-11 miesięcy wraz z zanikiem pasożytów we krwi i klinicznym dobrostanem. Następnie pojawiają się późne nawroty (spowodowane aktywacją hipnozoitów w wątrobie), ponownie zastąpione okresem utajonym bez leczenia, po którym choroba ponownie nawraca.
P. falciparum żyje w organizmie człowieka (bez leczenia) do 1,5 roku, P. vivax i P. ovale - do 3 lat, P. malariae - wiele lat, czasami całe życie.
Co Cię dręczy?
Formularze
Według zaleceń WHO malarię dzieli się na niepowikłaną, ciężką i powikłaną. Złośliwe postacie malarii i powikłania są charakterystyczne głównie dla zakażenia P. falciparum. Choroba wywołana przez P. vivax, P. ovale i P. malariae ma z reguły łagodny przebieg.
Trzydniowa malaria
Okres inkubacji trzydniowej malarii wynosi od 10-21 dni do 6-14 miesięcy. Objawy prodromalne malarii przed pierwotnym atakiem malarii są rzadko obserwowane, ale często poprzedzają nawroty i wyrażają się uczuciem ogólnego złego samopoczucia, osłabienia, zmęczenia, bólu w okolicy lędźwiowej, kończyn, niewielkim wzrostem temperatury ciała, utratą apetytu, bólem głowy. Czas trwania okresu prodromalnego wynosi średnio 1-5 dni.
Początkowo krzywa temperatury jest nieregularna (gorączka początkowa), co jest związane z asynchronicznym uwalnianiem kilku generacji P. vivax do krwi. Następnie typowe ataki malarii zaczynają się od przerywanej trzydniowej gorączki, wskazującej na powstawanie głównej generacji pasożytów we krwi. W ataku gorączkowym malarii klinicznie wyraźnie wyrażają się trzy fazy, bezpośrednio następujące po sobie: stadium dreszczy, gorąca i potu. Atak malarii zaczyna się od dreszczy, ich intensywność może być różna - od łagodnych dreszczy do oszałamiających dreszczy. W tym czasie pacjent kładzie się do łóżka, bezskutecznie próbuje się ogrzać, ale dreszcze się nasilają. Skóra staje się sucha, szorstka lub „gęsia” w dotyku, zimna, kończyny i widoczne błony śluzowe są sine. Obserwuje się następujące objawy malarii: silny ból głowy, czasami wymioty, bóle stawów i okolicy lędźwiowej. Stadium dreszczy trwa od kilku minut do 1-2 godzin i zostaje zastąpione stadium gorączki. Chory zdejmuje ubranie i bieliznę, ale to nie przynosi mu ulgi. Temperatura ciała osiąga 40-41 °C, skóra staje się sucha i gorąca, twarz robi się czerwona. Nasilają się bóle głowy, bóle w okolicy lędźwiowej i stawach, możliwe jest majaczenie i dezorientacja. Etap gorączki trwa od jednej do kilku godzin i jest zastępowany okresem pocenia. Temperatura spada krytycznie, pocenie się jest często obfite, więc chory musi wielokrotnie zmieniać bieliznę. Osłabiony atakiem, wkrótce zasypia. Czas trwania ataku wynosi 6-10 godzin. Za typowe uważa się występowanie ataków choroby w godzinach porannych i popołudniowych. Po ataku rozpoczyna się okres apireksji, trwający około 40 godzin. Po 2-3 atakach temperatury wątroba i śledziona są wyraźnie powiększone. Zmiany we krwi: niedokrwistość, rozwijająca się stopniowo od drugiego tygodnia choroby, leukopenia, neutropenia z przesunięciem komórek pasmowatych w lewo, względna limfocytoza, aneozynofilia i przyspieszone OB.
W naturalnym przebiegu choroby bez leczenia etiotropowego, po 12-14 atakach (4-6 tygodni) intensywność gorączki spada, ataki stopniowo ustępują, zmniejsza się wielkość wątroby i śledziony. Jednak po 2 tygodniach do 2 miesięcy występują wczesne nawroty, charakteryzujące się synchroniczną krzywą temperatury, wzrostem wątroby i śledziony oraz anemią. Następnie, wraz ze wzrostem odporności, pasożyty znikają z krwi i rozpoczyna się okres utajony. Jeśli w tym czasie nie zostanie przeprowadzone leczenie lekami histoschizotropowymi, to po 6-8 miesiącach (a czasami po 1-3 latach) następuje aktywacja „uśpionych” form tkankowych pasożytów i rozwijają się odległe nawroty. Charakteryzują się one ostrym początkiem, łagodniejszym przebiegiem, wczesnym wzrostem śledziony, krótką liczbą ataków (do 7-8), mniejszą intensywnością i czasem trwania pasożytemii, obecnością gametocytów we krwi.
Malaria owalna
W wielu cechach klinicznych i patogenetycznych malaria owalna jest podobna do trzydniowej malarii vivax. Okres inkubacji malarii owalnej wynosi 11-16 dni. W przypadku malarii owalnej patogen ma tendencję do pierwotnego utajenia. Okres inkubacji może trwać od 2 miesięcy do 2 lat lub dłużej. Objawy malarii obejmują okresową trzydniową gorączkę, rzadziej występuje ona codziennie. Ataki gorączkowe często występują wieczorami, a nie w pierwszej połowie dnia, co jest typowe dla innych postaci malarii. Malaria owalna charakteryzuje się głównie łagodnym przebiegiem z niewielką liczbą napadów, które występują bez wyraźnych dreszczy i z niższą temperaturą w szczycie ataków. Charakterystyczne jest to, że napady podczas ataku pierwotnego bardzo często ustępują samoistnie. Wyjaśnia się to szybkim tworzeniem stabilnej odporności. Jeżeli nie stosuje się leczenia lekami histoschizotropowymi, możliwe są 1-3 nawroty, a odstęp między nimi wynosi od 17 dni do 7 miesięcy.
Kwarta
Zwykle przebiega łagodnie. Okres inkubacji wynosi od 3 do 6 tygodni. Objawy prodromalne malarii są rzadko obserwowane. Początek choroby jest ostry. Od pierwszego ataku ustala się okresowa gorączka z okresowością ataków co 2 dni. Napad zwykle rozpoczyna się w południe, jego średni czas trwania wynosi około 13 godzin. Okres dreszczy jest długi i wyraźny. Okres gorąca trwa do 6 godzin, towarzyszą mu bóle głowy, bóle mięśni, bóle stawów, czasami nudności, wymioty. Czasami pacjenci są niespokojni i majaczą. W okresie międzynapadowym stan pacjentów jest zadowalający. Niedokrwistość, hepatosplenomegalia rozwijają się powoli - nie wcześniej niż 2 tygodnie po wystąpieniu choroby. Bez leczenia obserwuje się 8-14 ataków, ale proces schizogonii erytrocytowej na niskim poziomie trwa wiele lat. Najczęściej infekcja występuje w postaci nosicielstwa pasożytniczego bez aktywacji schizogonii erytrocytów, co czyni takie osoby potencjalnie niebezpiecznymi dawcami. W ogniskach endemicznych czterodniowa malaria powoduje zespół nerczycowy z niekorzystnym rokowaniem u dzieci.
Malaria tropikalna
Najcięższa postać zakażenia malarią. Okres inkubacji wynosi 8-16 dni. Pod koniec u niektórych osób nieodpornych występują objawy prodromalne malarii trwające od kilku godzin do 1-2 dni: złe samopoczucie, osłabienie, zmęczenie, bóle ciała, bóle mięśni i stawów, ból głowy. U większości pacjentów malaria tropikalna zaczyna się ostro, bez okresu prodromalnego, ze wzrostem temperatury ciała do 38-39 °C. Jeśli cykle schizogonii erytrocytowej w kilku pokoleniach P. falciparum w zakażonym organizmie nie kończą się jednocześnie, często klinicznie wyraża się to brakiem cyklicznej okresowości ataków gorączkowych. Ataki, występujące z naprzemienną zmianą faz, rozpoczynają się dreszczami trwającymi od 30 minut do 1 godziny. W tym okresie skóra jest blada przy badaniu, zimna w dotyku, często z szorstkością przypominającą „gęsią skórkę”. Dreszczom towarzyszy wzrost temperatury ciała do 38-39 °C. Po ustaniu dreszczy rozpoczyna się druga faza napadu - gorączka. Chorzy odczuwają lekkie uczucie ciepła, czasami odczuwają prawdziwe gorąco. Skóra staje się gorąca w dotyku, twarz jest przekrwiona. Czas trwania tej fazy wynosi około 12 godzin, zastępuje ją łagodne pocenie się. Temperatura ciała spada do wartości prawidłowych i podnormalnych, a po 1-2 godzinach ponownie wzrasta. W niektórych przypadkach wystąpieniu malarii tropikalnej towarzyszą nudności, wymioty, biegunka. Czasami odnotowuje się objawy kataralne malarii ze strony górnych dróg oddechowych: kaszel, katar, ból gardła. W późniejszym stadium obserwuje się wysypki opryszczkowe na wargach i skrzydełkach nosa. W ostrej fazie pacjenci zauważają przekrwienie spojówek, w ciężkich przypadkach choroby mogą jej towarzyszyć wybroczyny lub większe krwotoki podspojówkowe.
W szczycie tropikalnej malarii dreszcze są mniej nasilone niż w pierwszych dniach choroby, ich czas trwania wynosi 15-30 minut. Gorączka utrzymuje się przez kilka dni, rzadko odnotowuje się okresy apireksji. W łagodnym przebiegu choroby temperatura ciała w szczycie osiąga 38,5 °C, czas trwania gorączki wynosi 3-4 dni; przy umiarkowanym stopniu nasilenia - 39,5 °C i 6-7 dni, odpowiednio. Ciężki przebieg choroby charakteryzuje się wzrostem temperatury ciała do 40 °C i powyżej, a jej czas trwania wynosi osiem lub więcej dni. Czas trwania pojedynczych napadów (a właściwie nawarstwienia kilku) w tropikalnej malarii sięga 30-40 godzin. Przeważa nieregularny typ krzywej temperaturowej, rzadziej obserwowane są typy ustępujące, sporadycznie - przerywane i stałe.
Powiększenie wątroby stwierdza się zazwyczaj w 3. dniu choroby, powiększenie śledziony – również od 3. dnia, ale zwykle rejestruje się je dopiero opukiwaniem; wyraźne badanie palpacyjne staje się możliwe dopiero w 5.-6. dniu. Podczas badania USG narządów jamy brzusznej, powiększenie wątroby i śledziony stwierdza się już w 2.-3. dniu po wystąpieniu objawów klinicznych malarii tropikalnej. Zaburzenia metabolizmu barwnika obserwuje się tylko u chorych na ciężką i rzadziej umiarkowaną malarię tropikalną. Ponad trzykrotny wzrost aktywności aminotransferazy w surowicy uważa się za wskaźnik niekorzystnego rokowania. Zaburzenia metaboliczne w malarii tropikalnej obejmują zmiany w układzie hemostazy i hipoglikemię. Zaburzenia układu sercowo-naczyniowego mają charakter czynnościowy i wyrażają się tachykardią, stłumionymi tonami serca i niedociśnieniem. Czasami słyszalny jest przemijający szmer skurczowy na szczycie serca. W ciężkich postaciach choroby obserwuje się zmiany w EKG w postaci deformacji końcowej części kompleksu komorowego: spłaszczenie i odwrotna konfiguracja fali T, obniżenie odcinka ST. Jednocześnie zmniejsza się napięcie fali R w standardowych odprowadzeniach. U pacjentów z postacią mózgową zmiany fali P są typu P-pulmonale.
W przypadku malarii tropikalnej często obserwuje się zaburzenia ośrodkowego układu nerwowego, którym towarzyszy wysoka gorączka i zatrucie: ból głowy, wymioty, podrażnienie opon mózgowych, drgawki, senność, niekiedy objawy przypominające majaczenie, przy czym świadomość chorego jest zachowana.
Charakterystycznymi objawami umiarkowanego i ciężkiego zakażenia malarią są niedokrwistość hemolityczna i leukopenia, eozynofilia i neutropenia, w formule leukocytarnej odnotowuje się względną limfocytozę. W ciężkich postaciach choroby możliwa jest leukocytoza neutrofilowa; OB jest stale i znacznie podwyższone. Małopłytkowość jest objawem typowym dla wszystkich typów malarii. Podobnie jak w przypadku innych chorób zakaźnych, u pacjentów występuje przejściowa białkomocz.
Nawracająca malaria tropikalna jest spowodowana albo niewystarczającym leczeniem etiotropowym, albo opornością P. falciparum na stosowane środki chemioterapeutyczne. Naturalny przebieg malarii tropikalnej z korzystnym wynikiem nie trwa dłużej niż 2 tygodnie. W przypadku braku terapii etiotropowej nawroty występują po 7-10 dniach.
Ciąża jest powszechnie uznanym czynnikiem ryzyka malarii tropikalnej. Wynika to z wyższej częstości występowania ciąży, tendencji do ciężkich postaci klinicznych, zagrożenia dla zdrowia i życia dziecka oraz ograniczonego arsenału terapeutycznego. Malarię tropikalną u dzieci poniżej piątego roku życia należy uznać za chorobę potencjalnie śmiertelną. U dzieci w młodszych grupach wiekowych (do 3-4 lat), zwłaszcza u niemowląt, malaria ma unikalny obraz kliniczny: brakuje jej najbardziej uderzającego objawu klinicznego - napadu malarii. Jednocześnie obserwuje się takie objawy malarii, jak drgawki, wymioty, biegunka, bóle brzucha, przy szybko postępującym pogorszeniu stanu dziecka. Pojawienie się drgawek i innych objawów mózgowych niekoniecznie oznacza rozwój malarii mózgowej - jest to często jeden z objawów neurotoksykozy. Parazytemia u małych dzieci jest zwykle wysoka: P. falciparum może dotyczyć do 20% czerwonych krwinek. Choroba może szybko stać się złośliwa i zakończyć się śmiercią dziecka.
Komplikacje i konsekwencje
Zarejestrowany we wszystkich stadiach malarii tropikalnej. Prognostycznie niekorzystne objawy malarii, wskazujące na możliwość rozwoju złośliwej postaci malarii. - gorączka codzienna, brak gorączki między atakami, silny ból głowy, uogólnione drgawki nawracające więcej niż dwa razy w ciągu 24 godzin, sztywność odmózgowia, wstrząs hemodynamiczny (ciśnienie skurczowe krwi poniżej 70 mm Hg u osoby dorosłej i poniżej 50 mm Hg u dziecka). Świadczy o tym również wysoka pasożytemia (ponad 100 tys. P. falciparum w 1 μl krwi), wykrycie różnych stadiów wiekowych pasożyta we krwi obwodowej, obecność gametocytów, wzrastająca leukocytoza (ponad 12,0x10 9 /l). Niekorzystne rokowanie wykazują również hipoglikemia poniżej 2,2 mmol/l, zdekompensowana kwasica metaboliczna, ponad trzykrotny wzrost aktywności aminotransferazy w surowicy, a także spadek poziomu glukozy w płynie mózgowo-rdzeniowym i poziom mleczanu powyżej 6 μmol/l.
Ciężkie uszkodzenia ośrodkowego układu nerwowego w malarii tropikalnej są łączone pod nazwą „malaria mózgowa”, jej głównym objawem jest rozwój stanu śpiączki. Śpiączka malaryczna może być powikłaniem malarii pierwotnej, nawracającej i nawracającej, ale częściej obserwuje się ją w malarii pierwotnej, głównie u dzieci, kobiet w ciąży oraz osób młodych i w średnim wieku.
Postać mózgowa jest najczęstszym powikłaniem ciężkiej malarii falciparum. W dzisiejszych warunkach postać mózgowa rozwija się w 10% wszystkich przypadków malarii falciparum na świecie, a 60-80% wszystkich śmiertelnych skutków choroby jest związanych z tym powikłaniem. Postać mózgowa może rozwinąć się od pierwszych dni, ale częściej jest rejestrowana w 2. tygodniu choroby ze względu na brak specyficznej lub niewystarczającej terapii. Skutek śmiertelny może wystąpić w ciągu 1-2 dni. W obrazie klinicznym malarii mózgowej wyróżnia się trzy okresy: oszołomienie, stupor i prawdziwą śpiączkę.
Stadium oszołomienia charakteryzuje się psychicznym i fizycznym letargiem pacjenta, szybkim wyczerpaniem. Orientuje się w czasie i przestrzeni, ale niechętnie nawiązuje kontakt, odpowiada na pytania monosylabami, szybko się męczy. Odruchy ścięgniste są zachowane.
Stadium spoczynku wyraża się głębokim unieruchomieniem pacjenta z rzadkimi przebłyskami świadomości. Możliwe są ataksja, amnezja, drgawki, czasami o charakterze padaczkowym. Odruchy rogówkowe są zachowane, źrenice są prawidłowe. Odruchy ścięgniste są nasilone, występują odruchy patologiczne.
W śpiączce pacjent jest nieprzytomny i nie reaguje na bodźce zewnętrzne. Obserwuje się zaburzenia konwergencji, zez rozbieżny, ruchy swobodne gałek ocznych przy otwartych powiekach (jakby pacjent patrzył w sufit), oczopląs poziomy i pionowy, porażenie szóstej pary nerwów czaszkowych; brak odruchów ścięgnistych i brzusznych, ostre upośledzenie funkcji wegetatywnych. Wyrażają się objawy oponowe malarii i patologiczne odruchy Babińskiego, Rossolimo itp. Obserwuje się nietrzymanie moczu i kału. Nakłucie lędźwiowe ujawnia wzrost ciśnienia śródczaszkowego bez wyraźnych zaburzeń w składzie białkowym i komórkowym płynu mózgowo-rdzeniowego. Wysoki stopień pasożytemii z różnymi stadiami wiekowymi P. falciparum stwierdza się w grubej kropli i rozmazie krwi pacjentów z malarią śpiączkową. Jednocześnie znane są przypadki śmiertelnych skutków malarii mózgowej z bardzo niskim poziomem pasożytemii. Malaria mózgowa u dzieci często towarzyszy anemii. Anemia pogarsza stan neurologiczny i somatyczny dziecka. Przy skutecznym leczeniu świadomość zwykle powraca nagle.
W malarii mózgowej psychozy mogą rozwinąć się jako konsekwencja zmian dystroficznych w miąższu mózgu. W okresie ostrym psychozy występują w postaci majaczenia, amentii, napadów padaczkowych, stanów maniakalnych. Psychozy pomalaryczne charakteryzują się depresją, osłabieniem umysłowym, histerią, zespołami podobnymi do schizofrenii, a u dzieci przejściowe opóźnienie rozwoju umysłowego. Czasami obserwuje się odległe następstwa malarii mózgowej: porażenie połowicze, ataksję, ogniskowe objawy nerwów czaszkowych, zaburzenia pozapiramidowe, mono- i wielonerwowość.
Częstym powikłaniem wszystkich form zakażenia malarią jest niedokrwistość niedobarwliwa. Ciężką niedokrwistość diagnozuje się, gdy hematokryt spada poniżej 20%, a poziom hemoglobiny wynosi mniej niż 50 g/l. Stopień niedokrwistości zależy od rodzaju pasożyta, a także intensywności i czasu trwania zakażenia. Nasilenie malarii u rdzennych mieszkańców krajów tropikalnych jest często zaostrzane przez niedobór żelaza i kwasu foliowego w diecie. Po pierwszych atakach malarii może rozwinąć się anemia, która jest bardziej widoczna w malarii tropikalnej niż w innych formach.
Zakaźny wstrząs toksyczny (ITS) z rozwojem zespołu DIC jest powikłaniem charakterystycznym dla malarii-fаlсiраrum, występującym przy wysokiej pasożytemii. Charakterystyczny jest rozwój ostrej niewydolności nadnerczy. Przebiegowi zakaźnego wstrząsu toksycznego w gorącym klimacie towarzyszy hipowolemia.
Rozwój ostrej niewydolności nerek obserwuje się zazwyczaj w złośliwym, powikłanym przebiegu malarii falciparum. Charakterystyczny jest rozwój skąpomoczu i bezmoczu ze wzrostem kreatyniny i mocznika we krwi; analiza moczu ujawnia wyraźną białkomocz, walcowatość, ropomocz i mikrohematurię.
Zespół nerczycowy jest charakterystycznym powikłaniem malarii, charakteryzującym się powolnym, stale postępującym przebiegiem, któremu towarzyszą obrzęki, nadciśnienie tętnicze, białkomocz i rozwój niewydolności nerek.
Gorączka hemoglobinuryczna jest następstwem masywnej hemolizy wewnątrznaczyniowej zarówno przy intensywnej inwazji, jak i w wyniku stosowania niektórych leków przeciwmalarycznych (chinina, prymachina, sulfonamidy) u osób z niedoborem enzymu dehydrogenazy glukozo-6-fosforanowej. W ciężkiej postaci rozwija się intensywna żółtaczka, ciężki zespół krwotoczny, niedokrwistość i bezmocz, którym towarzyszą dreszcze, gorączka (40 °C), bóle w okolicy lędźwiowej, nawracające wymioty żółcią, bóle mięśni i stawów. Mocz nabiera ciemnobrązowego koloru, co jest spowodowane obecnością oksyhemoglobiny. Liczba erytrocytów w ciężkich przypadkach spada do 1x10 12 /l, a poziom hemoglobiny spada do 20-30 g /l. W przypadku hemoglobinurii malarycznej pasożytów we krwi jest bardzo mało lub nie są one wcale wykrywane. Przy szybkim odstawieniu leku przeciwmalarycznego, który spowodował hemolizę czerwonych krwinek, stan pacjenta poprawia się bez poważnych konsekwencji. W ciężkich przypadkach, ze względu na rozwój ostrej niewydolności nerek, rokowanie może być niekorzystne. W ostatnich latach brano pod uwagę autoimmunologiczny charakter rozwoju ostrej hemolizy związany z długotrwałym i częstym stosowaniem leków przeciwmalarycznych - chininy i prymachiny. Obserwuje się wysoką gorączkę (z niewielką pasożytemią), mocz staje się czarny, w badaniu krwi stwierdza się niedokrwistość, leukocytozę, przyspieszone OB, niewydolność nerek postępuje szybko, co prowadzi do zgonu w przypadku braku odpowiedniej terapii.
Algid malaryczny charakteryzuje się objawami klinicznymi typowymi dla zakaźnego wstrząsu toksycznego: zaburzeniami hemodynamicznymi i mikrokrążenia, zaburzeniami układu hemostazy, niewydolnością wielonarządową i hipotermią. W przeciwieństwie do malarii mózgowej, świadomość jest zachowana, chociaż śpiączka może rozwinąć się później. Algid może rozwinąć się na tle obrzęku płuc, kwasicy metabolicznej i ciężkiego odwodnienia. Odnotowuje się wysoki poziom pasożytemii. Rokowanie w dużej mierze zależy od terminowego i prawidłowego leczenia.
Ostry obrzęk płuc u pacjentów z malarią tropikalną często prowadzi do śmierci. Mechanizm tego poważnego powikłania nie został w pełni zbadany. Obrzęk płuc może być wywołany przez nadmierne nawodnienie, ale może również rozwinąć się na tle prawidłowego ciśnienia w krążeniu płucnym. Obecnie większość badaczy uważa ostrą niewydolność oddechową w malarii tropikalnej za objaw zespołu niewydolności oddechowej dorosłych.
Rzadkim, ale poważnym powikłaniem każdej klinicznej postaci malarii z hiperreaktywną splenomegalią lub bez niej jest pęknięcie śledziony. Pęknięcie może być spowodowane skrętem szypuły śledziony z ostrym zastojem krwi i rozwojem krwiaka podtorebkowego.
W malarii tropikalnej możliwe są uszkodzenia rogówki oka, zapalenie tęczówki, zapalenie tęczówki i ciała szklistego, zmętnienie ciała szklistego, zapalenie nerwu wzrokowego, zapalenie naczyniówki i siatkówki oraz krwotoki siatkówkowe; odnotowano również przypadki porażenia mięśni oka spowodowanego uszkodzeniami III, IV i VI pary nerwów czaszkowych, a także porażenie akomodacji.
Nawroty malarii
Poziom pasożytnictwa w czasie nawrotu jest zazwyczaj niższy niż w czasie pierwotnych objawów malarii. Ze względu na podwyższony próg pirogenny w trakcie zakażenia, objawy kliniczne w czasie nawrotu występują zwykle przy wyższej pasożytnictwie. Nawroty z reguły przebiegają łagodnie, z umiarkowanie wyrażonym zespołem toksycznym i regularną naprzemiennością napadów malarycznych od początku nawrotu; liczba napadów jest znacznie mniejsza niż w czasie pierwotnych objawów choroby. W zależności od czasu wystąpienia wyróżnia się nawroty wczesne (rozwój objawów klinicznych w ciągu pierwszych 2 miesięcy po pierwotnych objawach malarii) i późne (po 2 miesiącach). W zależności od pochodzenia nawroty dzielą się na erytrocytarne (wszystkie postacie malarii) i egzoerytrocytarne (tylko w malarii vivax i ovale).
Diagnostyka malaria
Rozpoznanie malarii ustala się na podstawie danych epidemiologicznych (pobyt w ognisku malarii, brak lub niewystarczająca chemioprofilaktyka), obrazu klinicznego choroby (charakterystyczne ataki) i potwierdza się badaniami laboratoryjnymi.
Rozpoznanie malarii powinno uwzględniać:
- ostry początek choroby, wyraźne objawy zatrucia, cykliczny przebieg z naprzemiennymi atakami gorączki i okresami gorączki, powiększenie wątroby i śledziony, rozwój postępującej niedokrwistości hemolitycznej;
- dane z historii epidemiologicznej (pobyt na obszarze o wysokim ryzyku zachorowań na malarię, transfuzja krwi, uzależnienie od narkotyków);
Czas trwania malarii, biorąc pod uwagę rozwój nawrotów przy pojedynczym zakażeniu i bez odpowiedniego leczenia etiotropowego
Forma malarii |
Czas trwania infekcji |
|
Normalna |
Maksymalny |
|
Malaria-falciparum |
Do 1 roku |
Do 3 lat |
Malaria-malariae |
Do 2-3 lat |
Możliwe na całe życie |
Malaria-vivax i ovale |
Do 1,5-2 lat |
Do 4-5 lat |
- wyniki badań laboratoryjnych:
- wyniki hemogramu: obniżony poziom hemoglobiny, leukopenia, limfomonocytoza, podwyższone OB;
- wyniki mikroskopii grubej kropli krwi (obejmujące co najmniej 100 pól widzenia w przypadkach niskiej pasożytemii): wykrywanie plazmodiazy i określenie poziomu pasożytemii w 1 µl krwi (100 pól widzenia - 0,2 µl krwi).
To jest konieczne:
- Aby wybrać stopień intensywności konkretnej terapii przeciwmalarycznej (przy wysokim poziomie pasożytnictwa u chorych na malarię tropikalną preferowane jest pozajelitowe podawanie leków).
- Aby monitorować skuteczność konkretnej terapii.
Stopień pasożytemii można ocenić również poprzez zliczenie odsetka zakażonych erytrocytów na 100 leukocytów w grubej kropli krwi (w tym przypadku, aby ocenić liczbę pasożytów w 1 μl, konieczna jest znajomość całkowitej liczby leukocytów i erytrocytów w 1 μl u pacjenta);
- dane mikroskopowe rozmazu krwi w celu określenia rodzaju malarii. Gruba kropla i rozmaz krwi są barwione metodą Romanovsky-Giemsa.
W wyniku gromadzenia się w naczyniach narządów wewnętrznych zaatakowanych erytrocytów zawierających dorosłe trofozoity i schizonty, przy badaniu preparatu grubej kropli w łagodnej malarii falciparum, w erytrocytach oznacza się tylko młode (młodzieńcze) trofozoity w stadium pierścieniowym. Pojawienie się we krwi obwodowej zaatakowanych erytrocytów zawierających dorosłe stadia rozwoju pasożyta (dorosłe lub ameboidalne trofozoity, schizonty) jest niekorzystnym objawem laboratoryjnym wskazującym na ciężki (powikłany) przebieg malarii falciparum.
Stopnie pasożytemii w malarii
Stopnie pasożytemii |
Oznaczenie konwencjonalne |
Liczba pasożytów w polu widzenia |
Liczba pasożytów w 1 µl krwi |
IV |
+ |
1-20 w 100 polach |
5-50 |
III |
+ + |
10-100 w 100 polach |
50-500 |
II |
+ + + |
1-10 w 1 polu |
500-5000 |
I |
+ + + + |
Ponad 10 w 1 polu |
Ponad 5000 |
U osób, które miały pierwszy kontakt (nieuodpornionych) z tą infekcją, np. u małych dzieci, pierwsze ataki mogą wystąpić przy bardzo niskiej pasożytemii, czasami niewykrywalnej mikroskopowo; wymaga to powtórzenia badania krwi (gęsta kropla) po 6-12 godzinach, ale nie później niż 24 godziny.
Diagnostyka laboratoryjna malarii polega na mikroskopowym badaniu próbek krwi (metodą grubej kropli i cienkiego rozmazu), barwionych według metody Romanowskiego-Giemsy.
Badaniu w kierunku malarii podlegają: pacjenci gorączkujący z nieokreślonym rozpoznaniem przez 3 dni w sezonie epidemicznym i 5 dni w pozostałej części roku; pacjenci z utrzymującymi się okresowymi wzrostami temperatury ciała pomimo leczenia zgodnego z ustalonym rozpoznaniem; biorcy krwi ze wzrostem temperatury ciała w ciągu ostatnich 3 miesięcy po transfuzji; osoby mieszkające w aktywnym ognisku, z jakimkolwiek wzrostem temperatury ciała. Należy wziąć pod uwagę, że podczas pierwszych ataków malarii liczba pasożytów we krwi obwodowej jest niewielka, dlatego konieczne jest jak najdokładniejsze badanie. Malaria z niską parazytemią występuje również u osób, które przyjmowały leki przeciwmalaryczne w celach profilaktycznych (terapia supresyjna) lub leki (tetracyklina, sulfonamidy) działające supresyjnie na malarię malarii przed zachorowaniem. Zaleca się pobieranie krwi do badania zarówno w czasie gorączki, jak i gorączki. W celu wykrycia pasożytów bada się grubą kroplę, ponieważ objętość krwi w niej jest 30-40 razy większa niż w cienkim rozmazie. W przypadku wysokiej parazytemii patogen malarii jest wykrywany nawet przy badaniu cienkiego rozmazu. Cechy morfologiczne i właściwości barwiące (barwienie) różnych stadiów wiekowych form bezpłciowych w erytrocytach są wyraźnie rozróżnialne w cienkim rozmazie. Konieczne jest określenie rodzaju pasożyta: jest to szczególnie ważne w przypadku P. falciparum. W niepowikłanej malarii tropikalnej P. falciparum obserwuje się we krwi obwodowej tylko w stadium młodych trofozoitów pierścieniowatych. W przypadku zakażenia pierwotnego, bardziej dojrzałe stadia pasożyta są wykrywane we krwi obwodowej, gdy choroba ma ciężki przebieg złośliwy. Parazytemia wzrasta szybciej niż przy zakażeniu innymi rodzajami patogenów. Gametocyty P. falciparum dojrzewają powoli, ale żyją długo (do 6 tygodni), podczas gdy gametocyty innych gatunków obumierają kilka godzin po osiągnięciu dojrzałości. Gametocyty wykryte w malarii tropikalnej pomagają określić okres trwania choroby: we wczesnym okresie (przy niepowikłanym przebiegu) wykrywane są tylko trofozoity w kształcie pierścieni, w okresie szczytowym - pierścienie i gametocyty (przy zakażeniu pierwotnym przy braku leczenia wskazuje to, że malaria trwa co najmniej 10-12 dni); w okresie rekonwalescencji stwierdzane są tylko gametocyty. Podczas leczenia poziom parazytemii we krwi obwodowej określa się dynamicznie. Dzień po rozpoczęciu leczenia etiotropowego powinien on zmniejszyć się o 25% lub więcej, a 3 dnia nie powinien przekraczać 25% pierwotnego. Obecność pasożytów w preparacie krwi 4 dnia po rozpoczęciu leczenia, z zastrzeżeniem wszystkich warunków skutecznego leczenia, jest oznaką oporności patogenu na zastosowany lek.
W ostatnich latach szybkie testy (metody immunochromatograficzne) oparte na wykrywaniu specyficznego białka HRP-2a i enzymu pLDH P. falciparum były stosowane w ogniskach endemicznych w celu szybkiego uzyskania wstępnej odpowiedzi. Testy jednego z dobrze znanych szybkich testów KAT-PF (KAT MEDICAL, Republika Południowej Afryki) wykazały wysoką skuteczność i swoistość w stosunku do P. falciparum. Porównanie wyników szybkiego testu, mikroskopii i PCR wykazało, że jego skuteczność diagnostyczna sięga 95-98%. Zastosowanie szybkich testów pozwala poznać wynik w ciągu zaledwie 10 minut. Personel laboratoryjny może opanować reakcję w ciągu 1-2 godzin. Szybkie metody umożliwiają osobom mieszkającym lub podróżującym w regionach endemicznych przeprowadzenie samodiagnozy; można je przeprowadzić w terenie. W Rosji szybka diagnostyka malarii jest obecnie ograniczona do indywidualnych badań klinicznych.
W nowoczesnych warunkach, zwłaszcza w badaniach masowych, metoda PCR oparta na wykrywaniu DNA pasożyta malarii ma szczególne znaczenie. Metodę tę można stosować do określania nosicielstwa przy niskiej parazytemii i mieszanym zakażeniu różnymi typami malarii, a także do różnicowania nawrotu lekoopornej malarii falciparum od ponownego zakażenia P. falciparum. Obecnie jest ona stosowana głównie w badaniach epidemiologicznych.
Jakie testy są potrzebne?
Diagnostyka różnicowa
Poszukiwanie diagnostyki różnicowej malarii przeprowadza się w zależności od nasilenia objawów klinicznych choroby i czasu jej trwania. Przede wszystkim malarię różnicuje się od chorób przebiegających z długotrwałą gorączką, powiększeniem wątroby, śledziony i możliwym rozwojem anemii: duru brzusznego i duru rzekomego, brucelozy, leptospirozy, sepsy, limfogranulomatozy. W pierwszych 5 dniach od wystąpienia choroby częstym błędnym rozpoznaniem malarii w regionach nieendemicznych jest grypa (lub inne ostre wirusowe infekcje dróg oddechowych).
W krajach tropikalnych Ameryki Południowej, Afryki, Azji Południowo-Wschodniej i Indii przeprowadza się diagnostykę różnicową malarii z krwotocznymi gorączkami wirusowymi (żółtą febrą, dengą itp.).
W postaci mózgowej malarii-falciparum diagnostykę różnicową malarii przeprowadza się z encefalopatią (śpiączką) rozwijającą się z cukrzycą niewyrównaną, niewydolnością wątroby i nerek, a także obrzękiem i opuchlizną mózgu z zapaleniem opon mózgowych lub zapaleniem opon mózgowo-rdzeniowych i mózgu o etiologii bakteryjnej lub wirusowej.
Z kim się skontaktować?
Leczenie malaria
Leczenie malarii polega na hamowaniu ostrych ataków choroby, zapobieganiu nawrotom i nosicielstwu gamet oraz przywróceniu zaburzonych funkcji organizmu.
Leki przeciwmalaryczne dzielimy na następujące grupy w zależności od ich wpływu na konkretne stadium rozwoju pasożyta: leki hematoschizotropowe, skuteczne przeciwko bezpłciowym stadiom erytrocytów zarodźca; leki histoschizotropowe, skuteczne przeciwko bezpłciowym stadiom tkankowym zarodźca; leki gamotropowe, powodujące śmierć gametocytów we krwi pacjenta lub zaburzające dojrzewanie gamemontów i powstawanie sporozoitów w ciele komara.
Leczenie etiotropowe
Leczenie etiotropowe malarii u chorych na malarię powinno być rozpoczęte niezwłocznie po ustaleniu rozpoznania klinicznego i epidemiologicznego oraz pobraniu krwi do badań parazytologicznych.
Obecnie stosowane leki należą do sześciu grup związków chemicznych: 4-aminochinoliny (chlorochina - delagyl, fosforan chlorochiny, niwakina), chinolinometanole (chinina - dichlorowodorek chininy, siarczan chininy, quinimax, meflochina), fenantrenometanole (halfan, halofantryna), pochodne artemizyniny (artesunat, artemeter, arteeter), antymetabolity (proguanil), 8-aminochinoliny (prymachina, tafenochina). Ponadto stosuje się leki przeciwmalaryczne łączone: savarin (chlorochina + proguanil), malarone (atowakwon + proguanil), coartem lub riamet (artemether + lumefantryna).
Jeśli u pacjenta wykryto P. vivax, P. ovale lub P. malariae, stosuje się leki z grupy 4-aminochinolin, najczęściej chlorochinę (delagyl). Leczenie malarii wygląda następująco: przez pierwsze dwa dni stosuje się lek w dawce dobowej 10 mg/kg zasady (cztery tabletki delagyl na raz), 3. dnia - 5 mg/kg (dwie tabletki delagyl) jednorazowo. Istnieją pojedyncze doniesienia o oporności szczepów P. vivax na chlorochinę w Birmie, Indonezji, Papui-Nowej Gwinei i Vanuatu. W takich przypadkach leczenie należy prowadzić meflochiną lub chininą zgodnie ze schematem leczenia niepowikłanej malarii. Ataki ustępują po 24-48 godzinach, a pasożyty znikają z krwi po 48-72 godzinach od rozpoczęcia przyjmowania chlorochiny.
W celu radykalnego wyleczenia (zapobiegania odległym nawrotom) malarii wywołanej przez P. vivax lub P. ovale, po zakończeniu kuracji chlorochiną, stosuje się schizontobójczy środek tkankowy, prymachinę. Przyjmuje się ją przez 14 dni w dawce 0,25 mg/kg (podstawa) na dobę. Szczepy P. vivax oporne na prymachinę (tzw. szczepy typu Chessona) występują na wyspach Pacyfiku i w krajach Azji Południowo-Wschodniej. W takich przypadkach jednym z zalecanych schematów leczenia jest przyjmowanie prymachiny w dawce 0,25 mg/kg na dobę przez 21 dni.
Jeśli P. falciparum zostanie wykryte we krwi osób nieodpornych w łagodnych przypadkach, lekami z wyboru, zgodnie z zaleceniami WHO, są meflochina i pochodne artemizyniny (artemeter, artesunat, arteeter); można również stosować halofantrynę. W przypadku braku meflochiny i halofantryny i/lub w przypadku występowania przeciwwskazań do stosowania tych leków, chininę przepisuje się w połączeniu z antybiotykami (tetracyklina, doksycyklina). Tetracyklinę przyjmuje się 0,5 g dwa razy dziennie przez 7-10 dni; można ją zastąpić doksycykliną w dawce dobowej 0,1 g, czas podawania wynosi 7-10 dni. W regionach, w których P. falciparum jest oporny na meflochinę i chininę, w leczeniu niepowikłanej malarii tropikalnej zaleca się połączenie preparatów meflochiny i artemizyniny (artemeter, artemeter). Połączenie fansidara i artesunatu jest skuteczne w leczeniu niepowikłanej malarii tropikalnej. Preparaty artemizyniny są szeroko stosowane w leczeniu wielolekoopornej malarii tropikalnej w Azji Południowo-Wschodniej, wielu krajach Ameryki Południowej i Afryki. Działają bardzo szybko zarówno na stadia krwi, jak i gametocyty. Jednak leki te są szybko eliminowane z organizmu, dlatego występują nawroty malarii. Bardziej odpowiednie jest przepisywanie ich w połączeniu z meflochiną w następujących dawkach:
- artesunat: 4 mg/kg dwa razy dziennie przez 3 dni; meflochina: 15 mg/kg raz w dniu 2 lub 25 mg/kg w dwóch dawkach w dniu 2 i 3;
- artemeter: 3,2 mg/kg raz dziennie przez 3 dni; meflochina: 15 mg/kg raz w dniu 2 lub 25 mg/kg w dwóch dawkach w dniu 2 i 3.
Schematy leczenia niepowikłanej malarii
Schematy aplikacji |
|||
Przygotowanie |
Pierwsza dawka, mg/kg |
Następne dawki, mg/kg (odstęp, h) |
Czas trwania kursu, dni |
Chlorochina |
10 (podstawy) |
10- 1-2 dzień 5- 3 dzień |
3 |
Fansidar (sulfadoksyna + pirymetamina) |
2,50-1,25 |
- |
1 |
Chinina, Kinimax, Kinoform |
10 (podstawy) |
7,5 (8) |
7-10 |
Meflochina |
15 (podstawy) |
- |
1 |
Halofantryna |
8 (sól) |
8 (6) |
1 |
Artesunat |
4 |
2 (12) |
7 |
Artemeter |
3.2 |
1,6 (24) |
7.0 |
Chinina -tetracyklina |
10,0-1,5 |
10,0 (8)+5,0 (6) |
10,0+7,0 |
Coartem (artemeter + lumefantryna) |
1,3 + 8 0 |
1,3-8,0 (8) |
3.0 |
Gdy nie ustalono rodzaju patogenu, zaleca się leczenie zgodnie ze schematami leczenia malarii tropikalnej. Jeśli pacjent wymiotuje wcześniej niż 30 minut po przyjęciu przepisanego leku przeciwmalarycznego, należy przyjąć tę samą dawkę ponownie. Jeśli wymioty wystąpią 30–60 minut po przyjęciu tabletek, przepisuje się dodatkowo połowę dawki tego leku.
Pacjenci z ciężką malarią tropikalną powinni być hospitalizowani na oddziale intensywnej terapii lub w oddziale reanimacyjnym. Chinina pozostaje lekiem pierwszego wyboru w leczeniu ciężkiej malarii tropikalnej. W leczeniu powikłanych postaci (malaria mózgowa, algid) pierwszą dawkę (7 mg/kg) zasady chininy podaje się dożylnie w ciągu 30 minut. Następnie kolejne 10 mg/kg podaje się dożylnie w kroplówce w ciągu 4 godzin. W ten sposób pacjent otrzymuje 17 mg/kg zasady chininy w ciągu pierwszych 4,5 godziny od rozpoczęcia leczenia. Zgodnie z innym schematem początkową dawkę 20 mg/kg zasady chininy podaje się w ciągu 4 godzin. Oba schematy są tolerowane przez pacjentów zadowalająco - bez zaburzeń sercowo-naczyniowych lub innych. Dawkę podtrzymującą 10 mg/kg zasady chininy podaje się w odstępach 8-godzinnych, czas podawania wynosi 1,5-2 godziny. Zaleca się łączenie chininy z tetracykliną (250 mg cztery razy dziennie przez 7 dni) lub doksycykliną (0,1 g dziennie przez 7-10 dni). W leczeniu dzieci zaleca się podawanie dawki nasycającej (15 mg/kg) zasady chininy dożylnie przez kroplówkę w 5% roztworze glukozy przez 4 godziny. Dawkę podtrzymującą (10 mg/kg) podaje się przez 2 godziny w odstępach 12-godzinnych. Tę samą dawkę stosuje się do podawania domięśniowego, ale zaleca się rozcieńczenie chininy pięć razy w wodzie destylowanej i podzielenie jej na dwa zastrzyki w różne pośladki.
Artemeter jest stosowany jako alternatywny lek w leczeniu powikłanej malarii tropikalnej w dawce dziennej 3,2 mg/kg pierwszego dnia leczenia. Przez kolejne sześć dni jest podawany w dawce 1,6 mg/kg domięśniowo w połączeniu z jedną dawką meflochiny.
Pacjentom z ciężkimi i powikłanymi postaciami malarii przepisuje się intensywną terapię patogenetyczną. Podczas rehydratacji należy uważać na obrzęk płuc i mózgu, ale hipowolemia nie jest mniej niebezpieczna. Jeśli rehydratacja okaże się nieskuteczna, u takich pacjentów może wystąpić niewydolność perfuzji tkankowej, kwasica, niedociśnienie, wstrząs i niewydolność nerek. Rozwój anemii zwykle nie zagraża życiu, ale jeśli hematokryt spadnie do 15-20%, należy przetoczyć krwinki czerwone lub pełną krew. W zespole DIC stosuje się transfuzję świeżej krwi pełnej lub koncentratów czynników krzepnięcia i płytek krwi. W przypadku hipoglikemii należy zastosować dożylne podanie 40% roztworu glukozy.
Podstawą leczenia obrzęku mózgu jest detoksykacja, odwodnienie, kontrola niedotlenienia mózgu i zaburzeń oddechowych (tlenoterapia, sztuczna wentylacja). Leki przeciwdrgawkowe są podawane zgodnie ze wskazaniami. Doświadczenie w leczeniu malarii mózgowej wykazało nieskuteczność, a nawet niebezpieczeństwo stosowania diuretyków osmotycznych: dekstranów o małej masie cząsteczkowej; adrenaliny; prostacykliny; pentoksyfiliny; cyklosporyny; surowic hiperimmunologicznych. Nie zaleca się również hiperbarycznego natleniania.
W przypadku ostrej niewydolności nerek lub ostrej niewydolności nerkowo-wątrobowej dawkę dobową chininy należy zmniejszyć do 10 mg/kg ze względu na możliwą kumulację leku, a roztwory należy podawać z szybkością 20 kropli na minutę. W początkowym okresie ostrej niewydolności nerek wykonuje się wymuszoną diurezę, a jeśli nie ma efektu i wzrasta azotemia, stosuje się hemodializę lub dializę otrzewnową, która zwykle daje dobre rezultaty. W przypadku gorączki hemoglobinurycznej odstawia się lek, który spowodował hemolizę. W razie potrzeby zastępuje się go innymi lekami przeciwmalarycznymi, a jednocześnie przepisuje się glikokortykosteroidy (prednizolon 1-2 mg/kg) i terapię detoksykacyjną.
W przypadku pęknięcia śledziony, do którego dochodzi zazwyczaj wskutek szybkiego i znacznego powiększenia narządu, wskazana jest natychmiastowa interwencja chirurgiczna.
W leczeniu nawrotów malarii tropikalnej wybiera się wcześniej nieużywany lek lub stosuje się poprzedni, ale w połączeniu z innymi lekami przeciwmalarycznymi. Nosicielstwo gamet jest eliminowane za pomocą prymachiny przez 1-3 dni w normalnych dawkach terapeutycznych.
Skuteczność leczenia malarii monitoruje się, badając grubą kroplę krwi z liczbą pasożytów w 1 μl. Badania te wykonuje się codziennie od 1. do 7. dnia po rozpoczęciu leczenia etiotropowego. Jeśli pasożyty znikną w tym czasie, dalsze badania preparatów krwi wykonuje się 14., 21. i 28. dnia po rozpoczęciu leczenia.
Ocena skuteczności
Skuteczność leczenia etiotropowego malarii u chorych na malarię ocenia się na podstawie trzech parametrów: wczesnej nieskuteczności (EF), późnej nieskuteczności (LF) i skuteczności leczenia.
Po zażyciu leku przeciwmalarycznego pacjent może wymiotować (szczególnie u dzieci). Ważne jest, aby pamiętać, że jeśli wymioty wystąpią w czasie krótszym niż 30 minut od zażycia leku, należy przyjąć tę samą dawkę ponownie, a po 30-60 minutach - połowę dawki zastosowanego leku.
Ocena skuteczności leczenia malarii (WHO, 1996)
Wczesna awaria (EF) |
Pogorszenie lub utrzymywanie się objawów klinicznych malarii przy obecności pasożytnictwa w ciągu pierwszych 3 dni od rozpoczęcia konkretnej terapii |
Późna awaria (LF) |
Ponowne pojawienie się charakterystycznych objawów klinicznych malarii (w tym rozwój ciężkiego stanu) przy obecności pasożytemii od 4 do 14 dnia od rozpoczęcia terapii swoistej |
Skuteczność leczenia |
Brak pasożytemii po 14 dniach od rozpoczęcia terapii swoistej przy braku kryteriów RN i PN |
Radykalne leczenie malarii
Radykalne leczenie malarii stosuje się równocześnie z leczeniem zatrzymującym chorobę lub bezpośrednio po nim.
- W celu zapobiegania nawrotom pozakrwinkowym malarii vivax i ovale, w celu oddziaływania na hipozoity, prymachina jest przepisywana w dawce 45 mg (27 mg zasady) na dobę (3 tabletki) - kurs 14 dni lub 6 tabletek - 1 raz w tygodniu - 6-8 tygodni (w przypadku niedoboru dehydrogenazy glukozo-6-fosforanowej). Lek tafenochina przechodzi badania kliniczne - analog prymachiny, ale o wyższej skuteczności klinicznej i niższej częstości występowania działań niepożądanych.
- Aby zapobiec przenoszeniu malarii falciparum (przez wpływ na gametocyty), prymachina jest stosowana w dawce 45 mg (27 mg zasady) na dobę (3 tabletki) - 3 dni. Leczenie jest prowadzone w regionach endemicznych dla malarii tropikalnej. Podczas stosowania Fansidaru w leczeniu pacjentów, którzy mieli malarię falciparum, prymachina nie jest przepisywana ze względu na skuteczne działanie pirymetaminy, która jest częścią Fansidaru, na gametocyty Pl. falciparum.
Leczenie ciężkiej i/lub skomplikowanej malarii falciparum przeprowadza się na oddziałach intensywnej terapii. Jeśli doustne podawanie leków nie jest możliwe, stosuje się terapię pozajelitową jednym z następujących leków:
- chlorowodorek chininy - 10-20 mg/kg (do 2,0 g na dobę) dożylnie w 500 ml 5% roztworu glukozy, powoli, 2-3 razy na dobę, aż do ustąpienia ciężkiego stanu, następnie jeden z leków doustnych według schematu leczenia niepowikłanej malarii falciparum;
- W nowoczesnych warunkach w niektórych krajach do leczenia ciężkich postaci malarii falciparum stosuje się nowe preparaty ziołowe (preparaty te nie są certyfikowane w Rosji): Artemeter (Artenam) – 160 mg domięśniowo pierwszego dnia, następnie 80 mg przez 6 dni; Artesunate – 50 mg domięśniowo (dożylnie) 2 razy dziennie przez 7 dni; Artemizynina – 1200 mg domięśniowo przez 7 dni.
Leczenie patogenetyczne malarii zależy od ciężkości choroby i rozwoju powikłań. Przepisywane są: terapia detoksykacyjna, korekcja kwasicy metabolicznej, hipoglikemia, leki moczopędne, leki przeciwhistaminowe, glikokortykosteroidy (według wskazań), witaminy, leki sercowo-naczyniowe i inne. W przypadku bezmoczu można wykonać dializę otrzewnową. W leczeniu gorączki hemoglobinurycznej w pierwszej kolejności odstawia się leki, które spowodowały hemolizę, a następnie wykonuje się transfuzję masy krwinek czerwonych.
Rekonwalescentów wypisuje się ze szpitala po zakończeniu pełnego cyklu etiotropowego leczenia pasożytniczego (zaprzestaniu terapii) w przypadku 2-3 ujemnych wyników badań krwi (gęsta kropla). Pacjenci, którzy przeszli malarię vivax i ovale, mogą przejść kolejny cykl leczenia prymachiną w trybie ambulatoryjnym. Pacjenci, którzy przeszli malarię, są monitorowani przez 1-1,5 miesiąca, powtarzając badania parazytologiczne grubej kropli krwi co 7-10 dni. Pacjenci, którzy przeszli malarię vivax, ovale i malariae, są monitorowani przez dwa lata, z obowiązkowymi badaniami parazytologicznymi grubej kropli przy każdym wzroście temperatury.
Zapobieganie
WHO walczy z malarią na całym świecie w ramach programu Roll Back Malaria, przyjętego w 1998 r. Obecnie WHO wyznaczyła nowy cel dla Regionu Europejskiego - wyeliminowanie malarii trzydniowej (P. vivax) do 2010 r., a malarii tropikalnej do 2015 r. Najważniejszym ogniwem w kompleksie działań jest terminowe wykrywanie i leczenie źródeł zakażenia.
Środki zapobiegawcze w przypadku wybuchu epidemii mają na celu terminowe wykrywanie i leczenie malarii, a także nosicieli pasożytów (źródeł zakażenia), a także zwalczanie nosicieli malarii. Obecnie nie ma skutecznych szczepionek do czynnej immunizacji przeciwko malarii.
Indywidualna profilaktyka malarii podczas pobytu w ognisku endemicznym ma na celu zapobieganie zakażeniu i zapobieganie atakowi malarii. Zapobieganie zakażeniu polega na podejmowaniu środków ochrony przed ukąszeniami komarów (stosowanie repelentów, siatek na oknach i drzwiach, zasłon w łóżkach, odzieży zakrywającej ramiona i nogi podczas przebywania na zewnątrz wieczorem i w nocy). Zgodnie z zaleceniami WHO zapobieganie atakowi malarii polega na przyjmowaniu leków przeciwmalarycznych, zaleca się je tylko osobom nieodpornym, podróżującym do ognisk o wysokim ryzyku zakażenia malarią i braku dostępnej opieki medycznej (oddalenie placówek medycznych, brak możliwości szybkiego badania krwi na malarię).
Potrzebę stosowania, czas trwania i częstotliwość przyjmowania leków ustala się wyłącznie po konsultacji ze specjalistą chorób zakaźnych. Ważne jest, aby zidentyfikować przeciwwskazania do przyjmowania leków chemioterapeutycznych, obecność ciężkich chorób współistniejących. Kobiety w ciąży, które nie są odporne, małe dzieci nie powinny odwiedzać regionów endemicznych dla malarii.
Biorąc pod uwagę wysoką oporność Pl. falciparum na chlorochinę, standardem w profilaktyce malarii falciparum, zgodnie z zaleceniami WHO, jest obecnie meflochina (250 mg raz w tygodniu, 2 tygodnie przed wyjazdem do regionu endemicznego i przez 4 tygodnie po powrocie). Stosowanie innych leków (doksycykliny, chlorochiny w połączeniu z proguanilem, atowachiny w połączeniu z proguanilem, prymachiny i innych) ustala specjalista chorób zakaźnych, biorąc pod uwagę sytuację epidemiologiczną w regionie pobytu i inne wyżej wymienione czynniki.
Prognoza
W większości przypadków śmiertelność jest spowodowana malarią tropikalną, a dokładniej jej formą mózgową, która występuje w 10% przypadków ciężkiej malarii falciparum. Śmiertelne skutki innych typów malarii są bardzo rzadkie. Ale malaria tropikalna, przy terminowej diagnozie i właściwym leczeniu malarii, kończy się całkowitym wyzdrowieniem.
W przypadku pacjentów, którzy przeszli malarię tropikalną, zaleca się ustanowienie obserwacji ambulatoryjnej przez 1-1,5 miesiąca i przeprowadzanie badań parazytologicznych krwi w odstępach 1-2 tygodni. Obserwacja ambulatoryjna pacjentów, którzy przeszli malarię wywołaną przez P. vivax. P. ovale. P. malariae, powinna być prowadzona przez dwa lata. Każdy wzrost temperatury ciała wymaga laboratoryjnych badań krwi w celu szybkiego wykrycia malarii plazmodia.

