Ekspert medyczny artykułu
Nowe publikacje
Niedomykalność zastawki mitralnej: przyczyny, diagnoza, leczenie
Ostatnia aktualizacja: 27.10.2025

Stosujemy ścisłe wytyczne dotyczące źródeł i linkujemy wyłącznie do renomowanych stron medycznych, placówek badawczych oraz, w miarę możliwości, do badań recenzowanych przez specjalistów medycznych. Należy pamiętać, że liczby w nawiasach ([1], [2] itd.) to klikalne linki do tych badań.
Jeśli uważasz, że którakolwiek z naszych treści jest niedokładna, nieaktualna lub w inny sposób wątpliwa, zaznacz ją i naciśnij Ctrl + Enter.
Niedomykalność zastawki mitralnej to cofanie się krwi z lewej komory do lewego przedsionka podczas skurczu, spowodowane nieprawidłowym zamknięciem płatków zastawki mitralnej. W łagodnych przypadkach może być niewyczuwalna, ale w miarę jej nasilenia prowadzi do przeciążenia objętościowego lewej komory, duszności, obniżonej tolerancji wysiłku, a ostatecznie do niewydolności serca i arytmii. Ważne jest, aby zrozumieć, że niedomykalność zastawki mitralnej nie jest pojedynczą diagnozą, lecz terminem zbiorczym obejmującym kilka mechanizmów, a leczenie zależy od mechanizmów leżących u jej podłoża. [1]
Rozróżnia się pierwotną (degeneracyjną) niedomykalność zastawki mitralnej – gdy same płatki/struny zastawki ulegają uszkodzeniu (wypadnięcie, pęknięcie struny, zwapnienie) – oraz wtórną (czynnościową), która występuje podczas przebudowy lewej komory lub przedsionka (np. w wyniku kardiomiopatii lub niedokrwienia), gdy płatki są formalnie „zdrowe”, ale nie zamykają się z powodu zmienionej geometrii. Są to zasadniczo różne stany wymagające stosowania różnych taktyk: w przypadku pierwotnym celem jest odbudowa/wymiana zastawki, natomiast w przypadku wtórnym celem jest optymalizacja terapii niewydolności serca i, jeśli to wskazane, interwencja w obrębie zastawki. [2]
W ostatnich latach znacząco rozwinęły się metody leczenia. Oprócz klasycznej naprawy chirurgicznej pojawiły się minimalnie inwazyjne technologie przezcewnikowe: naprawa szwu mitralnego typu „brzeg do brzegu” (TEER, MitraClip i PASCAL) oraz przezcewnikowa wymiana zastawki mitralnej (TMVR). W 2025 roku system Tendyne TMVR został po raz pierwszy zatwierdzony w Stanach Zjednoczonych dla szczególnej grupy pacjentów, a także zgromadzono długoterminowe dane dotyczące TEER (np. 5-letnie wyniki leczenia COAPT w przypadku wtórnej niedomykalności mitralnej). [3]
Aktualne wytyczne ESC/EACTS 2025 i ACC/AHA podkreślają rolę wielodyscyplinarnego zespołu ds. zastawek, zaawansowanej echokardiografii (w tym 3D) oraz precyzyjnej stratyfikacji: kto wymaga obserwacji, kto odniesie korzyści z naprawy chirurgicznej, a kto jest wskazany do TEER lub TMVR. Takie podejście poprawia objawy, jakość życia i zmniejsza liczbę hospitalizacji z powodu niewydolności serca u odpowiednio dobranych pacjentów. [4]
Kod według ICD-10 i ICD-11
W ICD-10 niedomykalność mitralna niereumatyczna jest kodowana jako I34.0, natomiast niedomykalność reumatyczna jako I05.1. W przypadku połączenia zwężenia i niedomykalności stosuje się kod I05.2 (wada reumatyczna złożona). Dla wyjaśnienia charakteru wrodzonego stosuje się kody z sekcji Q (np. Q23.3 – wrodzona niedomykalność mitralna). W codziennej dokumentacji istotne jest rozróżnienie postaci niereumatycznych od reumatycznych – są to różne grupy obserwacyjne i rozliczeniowe. [5]
W ICD-11 wady zastawki mitralnej klasyfikuje się jako blok BB6x: BB61 – niedomykalność zastawki mitralnej, BB60 – zwężenie zastawki mitralnej, BB63 – zwężenie z niedomykalnością. ICD-11 obsługuje „postkoordynację”: do głównego kodu można dodać wyjaśnienia (etiologia, ciężkość, choroby współistniejące), co poprawia dokładność statystyk. Oficjalna przeglądarka ICD-11 i źródła referencyjne potwierdzają aktualne indeksy. [6]
Tabela 1. Jak kodować niedomykalność zastawki mitralnej
| Sytuacja | ICD-10 | Komentarz | ICD-11 | Komentarz |
|---|---|---|---|---|
| Niereumatyczna niedomykalność zastawki mitralnej | I34.0 | Podstawowy kod | BB61 | Możesz dodać rozszerzenia wyjaśniające |
| Reumatyczna niedomykalność zastawki mitralnej | I05.1 | Określ etiologię reumatyczną | BB61 + "reumatyczny" | Pokoordynacja etiologii |
| Zwężenie + niewydolność (reumatyczna) | I05.2 | Połączony imadło | BB63.0 | Wariant ICD-11 dla wad złożonych |
| Nieokreślona choroba zastawki mitralnej | I34.9 | Wymaga szczegółowego opisu | BB6Z | „Wada zastawki mitralnej, nieokreślona” |
Epidemiologia
Niedomykalność zastawki mitralnej jest jedną z najczęstszych wad zastawkowych u dorosłych. Według obszernych szacunków populacyjnych i globalnych podsumowań obciążenia chorobami, częstość występowania istotnych wad zastawkowych rośnie wraz z wiekiem, a odsetek niedomykalności zastawki mitralnej jest szczególnie wysoki w grupach starszych. Przeglądy podają szacunki sięgające ~10% u osób powyżej 75. roku życia (w różnych populacjach); jednak odsetek ten jest minimalny u osób młodych. [7]
W krajach o wysokich dochodach dominuje zwyrodnieniowa (pierwotna) niedomykalność zastawki mitralnej, natomiast formy reumatyczne pozostają istotnym problemem w regionach o niskich i średnich dochodach. Analizy globalne wskazują na znaczny odsetek nierozpoznanych przypadków i zbyt małą liczbę skierowań na interwencje – wielu pacjentów pozostaje pod obserwacją przez lata, nie dochodząc do rozwiązania problemu z zastawką. [8]
U pacjentów z niewydolnością serca często występuje wtórna niedomykalność zastawki mitralnej: szacuje się, że u co piątego pacjenta z przewlekłą niewydolnością serca występuje znaczna wtórna niedomykalność zastawki mitralnej; wiąże się ona z hospitalizacjami i gorszym rokowaniem. To właśnie w tej grupie pacjentów pojawiły się przekonujące dowody przemawiające za TEER w kontekście optymalnej terapii farmakologicznej. [9]
Wraz z wprowadzeniem technologii przezcewnikowych (TEER i TMVR) wzrosła liczba interwencji u pacjentów w podeszłym wieku i pacjentów wysokiego ryzyka. Rejestry i badania randomizowane wykazują trwałą redukcję nasilenia niedomykalności i poprawę jakości życia; w przypadku wtórnej niedomykalności mitralnej TEER zmniejsza liczbę hospitalizacji, a według danych z długoterminowej obserwacji COAPT – śmiertelność. [10]
Powody
Pierwotna (zwyrodnieniowa) niedomykalność zastawki mitralnej jest spowodowana patologią płatków/strun: wypadaniem i myksomatozą, pęknięciem/rozciągnięciem struny, zwapnieniem pierścienia i płatków, a rzadziej następstwami radioterapii, zapalenia wsierdzia lub urazu. W postaci pierwotnej głównym celem jest mechaniczne przywrócenie koaptacji (najlepiej rekonstrukcja). [11]
Wtórna (czynnościowa) niedomykalność zastawki mitralnej rozwija się wraz z rozszerzeniem/przebudową lewej komory lub przedsionka: kardiomiopatia niedokrwienna i nieniedokrwienna, przedłużone rozszerzenie lewego przedsionka w migotaniu przedsionków („przedsionkowa” czynnościowa niedomykalność zastawki mitralnej). W tym przypadku płatki są początkowo „prawidłowe”, a wada zamknięcia występuje z powodu geometrii. [12]
W praktyce klinicznej często spotykane są mechanizmy mieszane: u pacjenta z wypadaniem płatka występuje również niedokrwienna dysfunkcja płatka lub zwapnienie pierścienia miażdżystego prowadzi do „restrykcyjnej” kinematyki. Zrozumienie dominującego mechanizmu determinuje wybór między naprawą, TEER, a w niektórych przypadkach TMVR. [13]
Do rzadkich przyczyn należą choroby zapalne i naciekowe, wady wrodzone oraz powikłania po operacjach kardiochirurgicznych. W takich przypadkach szczególnie ważne dla dokładnego odwzorowania anatomicznego jest echokardiografia 3D i obrazowanie metodą rezonansu magnetycznego serca. [14]
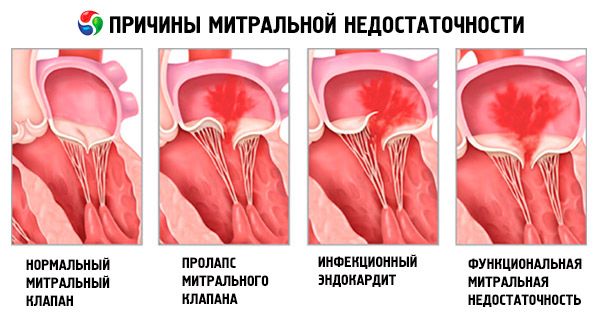
Tabela 2. Etiologia niedomykalności zastawki mitralnej – krótka „ściągawka”
| Typ | Przykłady | Klucz do rozpoznania |
|---|---|---|
| Pierwotne (zwyrodnieniowe) | Wypadnięcie, pęknięcie struny głosowej, zwapnienie | Widoczne zmiany w zaworach/akordach |
| Wtórny (komorowy) | Kardiomiopatia niedokrwienna/niedokrwienna | Rozszerzenie lewej komory, związanie płatków |
| Wtórne (przedsionkowe) | Rozszerzenie przedsionka lewego w migotaniu przedsionków | Duży LA, normalny LV |
| Zapalenie wsierdzia po radioterapii | Włóknienie/perforacje | Historia radioterapii/zakażenia |
Czynniki ryzyka
Czynniki związane z pierwotną (degeneracyjną) niedomykalnością zastawki mitralnej obejmują wiek, zmiany śluzakowe, dziedziczność (rodzinne formy wypadania zastawki), nadciśnienie tętnicze oraz zwapnienie aparatu zastawkowego/pierścienia zastawki mitralnej. Czynniki te zwiększają prawdopodobieństwo wystąpienia wady strukturalnej płatków i strun głosowych. [15]
Do czynników sprzyjających wtórnej niedomykalności zastawki mitralnej należą: poszerzenie lewej komory spowodowane chorobą wieńcową i kardiomiopatią, przewlekła niewydolność serca, przedłużony częstoskurcz i migotanie przedsionków oraz przebudowa pozawałowa. Kontrola tych stanów jest kluczowym elementem zapobiegania progresji choroby. [16]
Osobnym czynnikiem „wzmacniającym” jest płeć żeńska i starszy wiek w przypadku ciężkiego zwapnienia pierścienia mitralnego: tacy pacjenci częściej mają sztywną anatomię, w której klasyczna chirurgia plastyczna jest trudna do przeprowadzenia, a alternatywą stają się podejścia przezcewnikowe (w tym TMVR Tendyne w przypadku ciężkiego zwapnienia zastawki mitralnej). [17]
Wreszcie objawy niewydolności serca, powtarzające się hospitalizacje i niska tolerancja wysiłku w obecności umiarkowanej do ciężkiej/ciężkiej niedomykalności zastawki mitralnej są pośrednimi „markerami ryzyka”, które wymagają przeglądu taktyki i omówienia interwencji w specjalistycznym ośrodku. [18]
Patogeneza
W pierwotnej niedomykalności zastawki mitralnej defekt płatków/strun zaburza koaptację, powodując cofanie się krwi do lewego przedsionka, zwiększając jego objętość i ciśnienie. Powoduje to zwiększone obciążenie lewej komory (przeciążenie objętościowe), poszerzenie komór, przerost ekscentryczny i z czasem zmniejszenie kurczliwości. Stopień nasilenia objawów klinicznych zależy od objętości przepływu wstecznego i podatności komór. [19]
W przypadku wtórnej niedomykalności zastawki mitralnej remodeling ma charakter pierwotny: pierścień zastawkowy rozciąga się, mięśnie brodawkowate przesuwają się, a płatki zawiązują się i nie zamykają. W tym przypadku korekta geometryczna (remodeling lewej/lewej komory, zmniejszona sferyczność) jest kluczowa dla zmniejszenia niedomykalności; stąd nacisk na optymalne leczenie niewydolności serca i terapię resynchronizującą, jeśli jest wskazana. [20]
Długotrwała niedomykalność zastawki mitralnej prowadzi do powiększenia lewego przedsionka, co predysponuje do migotania przedsionków. Ta arytmia z kolei upośledza napełnianie i nasila objawy, tworząc „błędne koło”. W późniejszych stadiach wzrasta ciśnienie w żyłach i tętnicach płucnych, a prawa strona serca zostaje objęta procesem chorobowym. [21]
W kontekście interwencji należy pamiętać, że leki nie „zamykają” szczeliny między płatkami. Działanie leków polega na zmniejszeniu nacisku i spowolnieniu progresji, podczas gdy rekonstrukcja chirurgiczna, TEER lub TMVR, zapewnia eliminację wady koaptacji – wybór zależy od mechaniki i ryzyka. [22]
Objawy
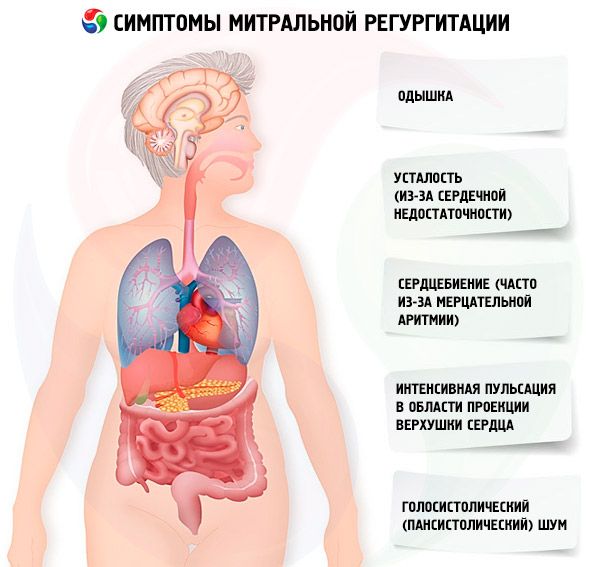
Do początkowych objawów należą zmęczenie, duszność wysiłkowa i kołatanie serca. W miarę postępu regurgitacji rozwija się ortopnoe, duszność nocna, obniżona tolerancja wysiłku oraz obrzęk obwodowy z towarzyszącą dysfunkcją lewej komory. Objawy mogą wahać się przez lata i nasilać wraz z arytmiami lub infekcjami. [23]
Obiektywnie rzecz biorąc, lekarz słyszy szmer skurczowy na szczycie serca; może występować ułamek sekundy w postaci tonu serca, oznak powiększenia lewego przedsionka (w elektrokardiogramie) i poszerzenia lewej komory (w badaniu obrazowym). Jednak głośność szmeru nie zawsze koreluje z jego ciężkością; określa to echokardiografia. [24]
U pacjentów w podeszłym wieku i z niewydolnością serca często dominują objawy ogólne (osłabienie, obrzęki, obniżona wydolność), co prowadzi do niedoszacowania udziału niedomykalności zastawki mitralnej. Każda ponowna hospitalizacja z powodu niewydolności serca jest powodem do ponownego rozważenia strategii leczenia zastawki. [25]
U osób z wypadaniem płatka zastawki mitralnej mogą występować epizody kołatania serca i nietypowego bólu w klatce piersiowej; pęknięcie struny głosowej może czasami powodować ostre pogorszenie stanu z silną dusznością – jest to nagły przypadek wymagający pilnej oceny w warunkach przedoperacyjnych/interwencyjnych.[26]
Formy i etapy
Z punktu widzenia mechaniki niedomykalność zastawki mitralnej dzieli się na pierwotną (degeneracyjną) i wtórną (czynnościową); niedomykalność wtórną dzieli się na „komorową” (kardiomiopatia, niedokrwienie) i „przedsionkową” (rozstrzeń lewego przedsionka w migotaniu przedsionków). To pierwszy krok na drodze. [27]
Według stopnia nasilenia – łagodny, umiarkowany, ciężki (zintegrowana ocena echokardiograficzna: efektywny obszar ujścia fali zwrotnej, objętość fali zwrotnej, szerokość żyły kurczliwej, przepływ wsteczny żył płucnych, wielkość/funkcja lewej komory). Rejestry i wytyczne kładą nacisk na ocenę zintegrowaną, a nie na opieranie się na pojedynczym parametrze. [28]
W zależności od przebiegu klinicznego: bezobjawowe z objawami przeciążenia objętościowego; objawowe bez ciężkiej dysfunkcji; powikłane (migotanie przedsionków, nadciśnienie płucne, niewydolność prawej komory). Im wyższy stopień zaawansowania, tym większe ryzyko i trudniejsza korekcja. [29]
Decyzja o interwencji zależy od połączenia mechanizmu → ciężkości → objawów → wielkości i funkcji lewej komory → operacji/TEER/TMVR. ESC/EACTS 2025 i ACC/AHA proponują algorytmy wyboru i „okna” interwencji przed nieodwracalną przebudową. [30]
Tabela 3. „Mapa” form niedomykalności mitralnej i prawdopodobnych taktyk
| Formularz | Mechanizm | Preferowane podejście |
|---|---|---|
| Pierwotne (zwyrodnieniowe) | Uszkodzenie zastawek/ścięgien | Naprawa chirurgiczna (akceptowalne ryzyko) lub TEER (wysokie ryzyko/brak operacji) |
| Wtórny (komorowy) | Rozszerzenie/uwięzienie lewej komory | Optymalna terapia niewydolności serca ± TEER według kryteriów (podobnych do COAPT) |
| Wtórne (przedsionkowe) | Rozszerzenie przedsionka lewego w migotaniu przedsionków | Kontrola rytmu/HR, leczenie AF ± TEER w wybranych |
| Ciężkie zwapnienie pierścieniowe (MAC) | Pierścień sztywny | Rozważ TMVR Tendyne (wskazanie FDA 2025) u pacjentów nieoperacyjnych/niekwalifikujących się do TEER |
Komplikacje i konsekwencje
Bez korekcji znaczna niedomykalność zastawki mitralnej prowadzi do postępującej przebudowy komór lewej, wzrostu ciśnienia w żyłach i tętnicach płucnych, a następnie do zajęcia komór prawej i pogorszenia niewydolności serca. Zwiększa to ryzyko hospitalizacji i zgonu. [31]
Częstym następstwem jest migotanie przedsionków, które upośledza tolerancję wysiłku i zwiększa ryzyko zatorowości. Kontrolowanie rytmu/częstości akcji serca i leczenie przeciwzakrzepowe, jak wskazano, stanowią część podstawowej strategii. [32]
U pacjentów z wtórną niedomykalnością zastawki mitralnej istnieje silny związek z ponowną hospitalizacją z powodu niewydolności serca; wykazano, że TEER w kontekście optymalnej terapii zmniejsza ryzyko hospitalizacji i poprawia przeżywalność w kilku badaniach i rejestrach (COAPT – dane 5-letnie). [33]
Po operacji lub TEER możliwe jest wystąpienie niedomykalności resztkowej/nawrotowej i konieczność ponownej interwencji; w rzeczywistych rejestrach u zdecydowanej większości pacjentów udaje się uzyskać długotrwałe utrzymanie niedomykalności mitralnej ≤2+, ale pięcioletnie przeżycie jest ograniczone przez ciężkość współistniejącej choroby podstawowej. Jest to istotny czynnik przy wyborze metody. [34]
Kiedy udać się do lekarza
Natychmiast – w przypadku nagłej, silnej duszności, obrzęku płuc, ostrego bólu/osłabienia z podejrzeniem pęknięcia struny strunowej (gwałtowny wzrost szmeru na szczycie), omdlenia lub objawów udaru. Są to sytuacje nagłe, wymagające pilnego skierowania do specjalistycznego ośrodka. [35]
Pilnie – jeśli duszność nasila się podczas normalnej aktywności, duszność nocna staje się częstsza, wytrzymałość znacznie się zmniejsza lub pojawia się nieregularne tętno (podejrzenie migotania przedsionków). Ważne jest, aby jak najszybciej wykonać echokardiografię i ocenę przez zespół ds. zastawek. [36]
W nadchodzących tygodniach – w przypadku wykrycia umiarkowanej, ciężkiej lub ciężkiej niedomykalności zastawki mitralnej podczas rutynowego badania USG serca, zwłaszcza w przypadku ciąży lub planowanej poważnej interwencji. Wczesne omówienie taktyki leczenia poprawia rokowanie. [37]
Po operacji/TEER – jeśli duszność powraca, tolerancja wysiłku pogarsza się lub występuje obrzęk, należy wykluczyć resztkową/nawracającą niedomykalność, dysfunkcję lewej komory i arytmię. [38]
Diagnostyka
Podstawową metodą jest echokardiografia: potwierdza ona obecność niedomykalności, określa mechanizm (pierwotny/wtórny), stopień zaawansowania (integralnie), wielkość i funkcję komór; echokardiografia 3D i echokardiografia przezprzełykowa mają kluczowe znaczenie w planowaniu TEER/TMVR i rekonstrukcji chirurgicznej. [39]
Ważne jest, aby ocenić nie tylko „ile przecieka”, ale także „dlaczego przecieka”: długość koaptacji, uwięzienie, zwapnienie, rozmiar pierścienia zastawki i stan strun strunowych – te szczegóły decydują o tym, czy koaptację można przywrócić za pomocą klipsa (TEER), czy konieczna jest wymiana zastawki (chirurgiczna lub TMVR). W wątpliwych przypadkach stosuje się obrazowanie metodą rezonansu magnetycznego serca (ilościowa ocena niedomykalności) i tomografię komputerową (anatomia pierścienia zastawki/zwapnienie). [40]
W przypadku wtórnej niedomykalności zastawki mitralnej konieczna jest optymalizacja terapii niewydolności serca i ocena możliwości terapii resynchronizującej. Terapia ta może zmniejszyć niedomykalność poprzez zmianę mechaniki lewej komory. Decyzje podejmuje się po ustabilizowaniu farmakoterapii. [41]
Markery laboratoryjne (peptydy natriuretyczne) pomagają ocenić przeciążenie serca i rokowanie, ale diagnozę i leczenie ustala się na podstawie badań obrazowych i objawów klinicznych. Długotrwałe monitorowanie rytmu serca jest pomocne w przypadku arytmii. [42]
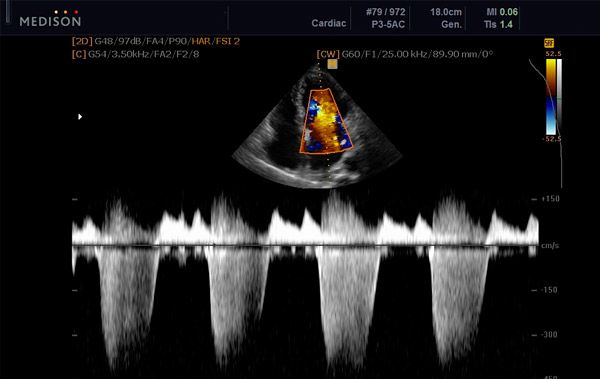
Tabela 4. Narzędzia diagnostyczne i kto co „mówi”
| Metoda | Rola | Kiedy jest to obowiązkowe? |
|---|---|---|
| TT-Echo/ChP-Echo (2D/3D) | Mechanizm, grawitacja, anatomia | Zawsze; przed jakąkolwiek interwencją |
| MRI serca | Ilościowa regurgitacja, objętości | Wątpliwe przypadki, skomplikowana anatomia |
| Tomografia komputerowa serca | Pierścień/wapnienie, planowanie TMVR | Silne zwapnienie, podejrzenie MAC |
| Testy obciążeniowe | Rezerwa funkcjonalna | Przypadki graniczne, ocena objawów |
Diagnostyka różnicowa
Ważne jest rozróżnienie pierwotnej i wtórnej niedomykalności mitralnej: w pierwotnej niedomykalności mitralnej obserwujemy defekt strukturalny płatków/strun, natomiast we wtórnej niedomykalności mitralnej obserwujemy geometryczny defekt koaptacji bez elementów organicznych. To determinuje, u których pacjentów priorytet powinna mieć naprawa chirurgiczna/TEER, a u innych optymalizacja terapii niewydolności serca z TEER w wybranych przypadkach. [43]
Niedomykalność zastawki mitralnej różni się od niedomykalności aorty umiejscowieniem strumienia i jego profilem skroniowym: w przypadku niedomykalności zastawki mitralnej strumień jest skurczowy i cofa się do lewego przedsionka, a w przypadku niedomykalności aorty następuje cofanie się krwi do lewej komory w fazie rozkurczowej. Kolorowe echo Dopplera ustawia wszystko na swoim miejscu. [44]
W przypadku arytmii (zwłaszcza migotania przedsionków) objawy mogą być nieproporcjonalne do stopnia niedomykalności. Normalizacja częstości akcji serca/rytmu często prowadzi do częściowej poprawy, jednak ciężka niedomykalność zastawki mitralnej nadal wymaga leczenia. [45]
Wreszcie, niedomykalność zastawki mitralnej odróżnia się od zwężenia zastawki mitralnej z komponentą niedomykalności i od skutków zwapnienia zastawki mitralnej: w przypadku ciężkiego MAC koaptacja może nie być możliwa – TMVR Tendyne omówiono w niniejszym dokumencie w ramach zatwierdzonych wskazań. [46]
Tabela 5. „Podobne, ale nie takie same”: jak szybko się zorientować
| Państwo | Co to jest | Co jest przeciw? |
|---|---|---|
| MR wtórny a pierwotny | Uwięź, rozszerzenie lewej/lewej komory | Czysta organiczna struktura zaworów/akordów |
| Niedomykalność aorty | Strumień rozkurczowy w lewej komorze | Skurczowy strumień powietrza w Los Angeles |
| Pan w MAC | Zwapnienie pierścienia zastawkowego/zastawki | Elastyczna anatomia bez MAC |
| MS+MR (połączone) | Na zastawce mitralnej występuje gradient | Czysta regurgitacja bez zwężenia |
Leczenie
Leki poprawiają samopoczucie i zmniejszają ryzyko wtórnej niedomykalności zastawki mitralnej, ale nie „zamykają” płatków zastawki. Podstawą jest optymalna terapia niewydolności serca (inhibitory kotransportera sodowo-glukozowego-2, inhibitory konwertazy angiotensyny/sakubitryl-walsartan, beta-blokery, antagoniści receptora mineralokortykoidowego), kontrola ciśnienia tętniczego, leczenie niedokrwienia oraz resynchronizacja serca w razie wskazań. Interwencja jest rozważana dopiero po stabilizacji. [47]
Złotym standardem w leczeniu pierwotnej niedomykalności zastawki mitralnej u pacjentów z akceptowalnym ryzykiem chirurgicznym jest naprawa chirurgiczna: annuloplastyka, naprawa/wymiana struny ścięgnistej i naprawa płatka. Wytyczne z 2025 roku nadal priorytetowo traktują naprawę nad wymianą, jeśli jest to możliwe z anatomicznego punktu widzenia, ze względu na poprawę przeżywalności i zachowanie funkcji lewej komory. [48]
Badanie końcowe przezcewnikowe (TEER) - MitraClip i PASCAL.
- Wtórna MR: W połączeniu z optymalną terapią TEER zmniejsza liczbę hospitalizacji z powodu niewydolności serca i śmiertelność u odpowiednio dobranych pacjentów (dane COAPT z 5 lat). Potwierdzają to wytyczne. [49]
- Pierwotna MR u pacjentów wysokiego ryzyka: TEER stanowi alternatywę dla operacji u pacjentów z ciężką degeneracyjną MR i wysokim/niemożliwym do przeprowadzenia zabiegiem. System PASCAL jest dostępny od 2022 roku. W randomizowanym badaniu CLASP IID wykazał on niegorszą skuteczność i bezpieczeństwo w porównaniu z MitraClip (dane z okresu do 2 lat). Wybór systemu zależy od anatomii i doświadczenia ośrodka. [50]
Przezcewnikowa wymiana zastawki mitralnej (TMVR).
- W maju 2025 roku amerykańska Agencja ds. Żywności i Leków (FDA) zatwierdziła system Tendyne dla pacjentów z ciężkim zwapnieniem zastawki mitralnej (MAC) i objawową ciężką dysfunkcją zastawki mitralnej, niekwalifikującą się do leczenia operacyjnego ani TEER (potwierdzone zatwierdzeniem przez FDA i publikacjami). Jest to pierwszy system TMVR zatwierdzony w USA; w innych scenariuszach TMVR pozostaje w fazie badań (Intrepid/APOLLO, Sapien M3/ENCIRCLE itp.). Rozwiązanie wymaga szczegółowego planowania tomografii komputerowej i zespołu z doświadczeniem w TMVR. [51]
Kto i co powinien wybrać?
- Choroba zwyrodnieniowa MR, ryzyko niskie/umiarkowane: priorytetem jest leczenie chirurgiczne.
- Zwyrodnieniowa MR, ryzyko wysokie/niedopuszczalne: TEER (MitraClip lub PASCAL).
- Wtórna MR po optymalizacji terapii HF: TEER u pacjentów „podobnych do COAPT”; rola rozszerza się wraz z wynikami badania RESHAPE-HF2.
- Ciężki MAC, niekwalifikujący się do operacji/TEER: Rozważ TMVR Tendyne w przypadku zatwierdzonych wskazań. Wszystkie decyzje podejmuje zespół kardiologiczny po wykonaniu 3D-Echo/TK. [52]
Tabela 6. TEER: Najważniejsze fakty z bazy dowodowej
| Sytuacja | Co jest pokazane | Źródła |
|---|---|---|
| Wtórny MR w tle ATSN | ↓ hospitalizacji, ↓ śmiertelności w ciągu 5 lat | COAPT 5-latkowie [53] |
| Wysokiego ryzyka zwyrodnieniowa MR | Skuteczność/bezpieczeństwo potwierdzone | ACC/AHA, ESC/EACTS [54] |
| PASCAL kontra MitraClip (DMR) | Niegorszość według MAC i MR≤2+; wyniki są stabilne do 2 lat | ZAPIĘCIE IID (FDA 2022) [55] |
Tabela 7. TMVR w 2025 r. (w skrócie)
| System | Status | Dla kogo jest przeznaczony? | Notatki |
|---|---|---|---|
| Tendyne | Zatwierdzone przez FDA (maj 2025) | Objawowa ciężka dysfunkcja zastawki MV ze znacznym MAC, nieoperacyjna/nieodpowiednia do TEER | Wymaga planowania TK, doświadczenia w ośrodku [56] |
| Nieustraszony (APOLLO) | Badanie | Pacjenci niekwalifikujący się do TEER/operacji (zgodnie z protokołem) | Trwa rekrutacja/ocena wyników [57] |
| Sapien M3 (OKRĄŻ) | Badanie | Podobnie | Wczesne dane, niezarejestrowane [58] |
Tabela 8. Praktyczne progi dyskusji o interwencji (uproszczone)
| Scenariusz | Co jest alarmujące |
|---|---|
| Objawowa ciężka MR (dowolna mechanika) | Rozważ korektę (naprawę/TEER/TMVR) |
| Bezobjawowa pierwotna MR | Zwiększona objętość/wielkość skurczowa lewej komory (LV), zmniejszona frakcja wyrzutowa, hormon luteinizujący (LH) – powód, dla którego nie należy opóźniać |
| Wtórny MR | Po optymalizacji OTSN-TEER w „COAPT-like” |
| Ciężki MAC | TEER → Ocena TMVR (Tendyne) |
Zapobieganie
Zapobieganie pierwotnej niedomykalności zastawki mitralnej polega na kontrolowaniu czynników przyspieszających degenerację i przebudowę zastawki: nadciśnienia tętniczego, choroby wieńcowej, palenia tytoniu, masy ciała i czynników metabolicznych. Regularne badania i ultrasonografia serca u pacjentów z grupy ryzyka (wypadanie, zwapnienie) pozwalają na wczesne wykrycie progresji choroby. [59]
W przypadku wtórnej niedomykalności zastawki mitralnej kluczem jest profilaktyka i wysokiej jakości leczenie niewydolności serca: przestrzeganie schematów leczenia, kontrola częstości i rytmu serca w migotaniu przedsionków, leczenie niedokrwienia i resynchronizacja w razie potrzeby. Spowalnia to przebudowę i zmniejsza nasilenie niedomykalności. [60]
Zapobieganie powikłaniom obejmuje szczepienie przeciwko grypie/pneumokokom, higienę jamy ustnej (profilaktyka zapalenia wsierdzia w grupach ryzyka) oraz monitorowanie masy ciała i objawów. Ważna jest edukacja pacjenta: rozpoznawanie „sygnałów ostrzegawczych” (postępująca duszność, obrzęk, nowe arytmie). [61]
Wreszcie zapobieganie „systemowym stratom czasu” – kierowanie do ośrodków mających doświadczenie w rekonstrukcji, TEER i TMVR: to właśnie tam dokonają one oceny anatomii echokardiografii 3D, wybiorą metodę i „wyłapią” optymalny moment interwencji przed nieodwracalną przebudową. [62]
Prognoza
Bez korekcji ciężka niedomykalność zastawki mitralnej wiąże się ze zwiększoną śmiertelnością i częstymi hospitalizacjami, zwłaszcza u pacjentów z niewydolnością serca. Wczesna korekcja mechaniczna – chirurgiczna lub przezcewnikowa – poprawia objawy, jakość życia i rokowanie.[63]
W przypadku wtórnej niedomykalności zastawki mitralnej, TEER, stosowany w połączeniu z optymalną terapią, zmniejsza liczbę hospitalizacji i zapewnia 5-letni wzrost przeżywalności u odpowiednio dobranych pacjentów (COAPT). Rejestry w warunkach rzeczywistych wykazały trwałe utrzymanie MR ≤2+ i poprawę czynnościową, chociaż całkowite przeżycie jest ograniczone przez ciężkość chorób współistniejących. [64]
W przypadku ciężkiego zwapnienia zastawki mitralnej (MAC) wprowadzenie Tendyne TMVR rozszerzyło możliwości leczenia w kategorii, która wcześniej była „beznadziejna”, z klinicznie istotną poprawą jakości życia i wyników w klasie funkcjonalnej u starannie wyselekcjonowanych pacjentów. Dalsze rejestry pozwolą na uzyskanie bardziej szczegółowych wyników długoterminowych. [65]
Podsumowując: najlepiej nie zwlekać. Wczesna diagnoza mechaniki wady, optymalna terapia niewydolności serca i terminowy wybór rekonstrukcji/TEER/TMVR w specjalistycznym ośrodku zapewniają korzystną trajektorię dla większości pacjentów. [66]
Często zadawane pytania
Czym pierwotna niedomykalność mitralna różni się od wtórnej niedomykalności mitralnej i dlaczego jest to ważne?
W pierwotnej niedomykalności mitralnej płatki/struny zastawkowe są uszkodzone – priorytetem jest rekonstrukcja/wymiana (lub TEER u pacjentów wysokiego ryzyka). W przypadku wtórnej niedomykalności mitralnej płatki są „zdrowe”, a problem tkwi w geometrii lewej komory/lewego przedsionka – w pierwszej kolejności należy rozważyć optymalne leczenie niewydolności serca, a następnie TEER u wybranych pacjentów. Taktyka leczenia jest zasadniczo różna. [67]
Czy TEER rzeczywiście pomaga w leczeniu wtórnej niedomykalności zastawki mitralnej?
Tak. W badaniu COAPT zmniejszenie liczby hospitalizacji z powodu niewydolności serca i korzyści w zakresie przeżycia utrzymywały się przez okres do 5 lat obserwacji. Znalazło to odzwierciedlenie w wytycznych. [68]
Jakie są różnice między MitraClip a PASCAL? Który wybrać?
Oba systemy są wariantami TEER. W randomizowanym badaniu CLASP IID stwierdzono, że PASCAL nie ustępuje MitraClip pod względem bezpieczeństwa i skuteczności, a rezultaty utrzymują się do 2 lat; wybór zależy od anatomii i doświadczenia ośrodka. [69]
Czym jest TMVR i dla kogo jest obecnie wskazany?
TMVR to przezcewnikowa wymiana zastawki mitralnej. System Tendyne ma zostać zatwierdzony w Stanach Zjednoczonych w 2025 roku dla pacjentów z zaawansowanym zwapnieniem zastawki mitralnej (MAC), którzy nie kwalifikują się do operacji ani TEER. Inne systemy TMVR są nadal w fazie rozwoju. [70]
Jakie kody należy stosować w dokumentach?
ICD-10: I34.0 (niewydolność niereumatyczna), I05.1 (niewydolność reumatyczna), I05.2 (stenoza + niedomykalność). ICD-11: BB61 (niedomykalność zastawki mitralnej), BB63 (wada łączona), z późniejszą koordynacją etiologii/ciężkości. [71]
Gdzie boli?
Co trzeba zbadać?

