Ekspert medyczny artykułu
Nowe publikacje
Zespół Klinefeltera
Ostatnia recenzja: 05.07.2025

Cała zawartość iLive jest sprawdzana medycznie lub sprawdzana pod względem faktycznym, aby zapewnić jak największą dokładność faktyczną.
Mamy ścisłe wytyczne dotyczące pozyskiwania i tylko linki do renomowanych serwisów medialnych, akademickich instytucji badawczych i, o ile to możliwe, recenzowanych badań medycznych. Zauważ, że liczby w nawiasach ([1], [2] itd.) Są linkami do tych badań, które można kliknąć.
Jeśli uważasz, że któraś z naszych treści jest niedokładna, nieaktualna lub w inny sposób wątpliwa, wybierz ją i naciśnij Ctrl + Enter.
Zespół Klinefeltera, 47,XXY jest klinicznym przykładem zaburzenia chromosomów płciowych.
Choroba Klinefeltera charakteryzuje się obecnością co najmniej jednego dodatkowego chromosomu X u chłopców, co prowadzi do zaburzeń dojrzewania u nich. Po raz pierwszy została opisana klinicznie przez Klinefeltera w 1942 r. Częstość występowania w populacji wynosi 1:1000 mężczyzn. Zespół Klinefeltera występuje u około 1/800 żywo urodzonych chłopców. Dziecko otrzymuje dodatkowy chromosom X od matki w 60% przypadków.
 [ 1 ]
[ 1 ]
Co jest przyczyną choroby Klinefeltera?
W większości przypadków nieprawidłowa dywergencja chromosomów płciowych występuje w gametach rodziców. Występują również warianty mozaikowe, na przykład 47, XXY/46, XY.
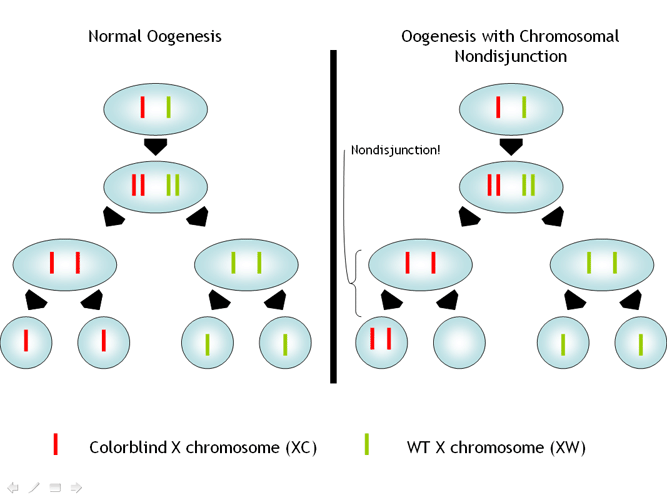
Zespół Klinefeltera jest spowodowany nieprawidłowością chromosomową, najczęściej reprezentowaną przez 47XXY. Formy mozaikowe, 46XY/47XXY, są znacznie rzadsze. Następujące formy są opisywane jako warianty kariotypu kazuistycznego: 48XXXY, 47XXY/46XX, 47XXY/45XO. Istnieje również obserwacja pacjenta z kariotypem 47XXYY46XX/45XO. Przyczyną tych nieprawidłowości chromosomowych, dodatkowego chromosomu X w męskim kariotypie, może być nierozdzielenie chromosomu X podczas pierwszego lub drugiego podziału mejotycznego lub zaburzona mitotyczna dywergencja chromosomów podczas rozwoju zygoty (warianty mozaikowe). Analiza DNA wykazała, że 53% pacjentów z zespołem Klinefeltera miało dodatkowy chromosom pochodzenia ojcowskiego, co było konsekwencją nierozdzielenia podczas pierwszego podziału mejotycznego. U 43% pacjentów w wyniku patologii pierwszego i drugiego podziału mejotycznego wystąpił dodatkowy chromosom pochodzenia matczynego. Najwyraźniej nie ma różnic w fenotypie u pacjentów z dodatkowym chromosomem X pochodzenia matczynego lub ojcowskiego. Częstotliwość urodzeń chłopców z zespołem Klinefeltera wzrasta wraz z wiekiem matki. Nie stwierdzono takiej zależności od wieku ojca. Obecność dodatkowego chromosomu X w kariotypie męskim nie wpływa na różnicowanie jąder i powstawanie narządów płciowych typu męskiego. Jednak aktywność życiowa komórek rozrodczych jest upośledzona, spermatogeneza jest nieobecna. Powodem tego jest aktywność dodatkowego chromosomu X w komórkach rozrodczych, które normalnie mają haploidalny zestaw chromosomów. Wykazano, że w komórkach rozrodczych jajnika płodu u dziewcząt reaktywacja drugiego chromosomu X następuje przed wejściem do mejozy (normalnie aktywowany jest tylko jeden). U chłopców z kariotypem XXY zachowany jest również premejotyczny proces reaktywacji drugiego chromosomu X, ale proces dywergencji jest zaburzony, a komórka rozrodcza może zawierać dwa aktywne chromosomy X, co prowadzi do jej obumarcia już w pierwszych dniach po reaktywacji chromosomu X. U dorosłych mężczyzn z zespołem Klinefeltera, analizując plemniki, pojedyncze zachowane komórki rozrodcze miały tylko normalny haploidalny zestaw chromosomów.
Objawy zespołu Klinefeltera
W chwili narodzin zespół Klinefeltera nie objawia się klinicznie. Opisano wiele wariantów klinicznych, dotyczących zarówno anomalii statusu seksualnego, jak i zaburzeń somatycznych w zespole Klinefeltera. Nie zidentyfikowano ogólnego wzorca wpływu kariotypu na fenotyp, ale pacjenci z kariotypem mozaikowym z prawidłowym męskim klonem 47XXY/46XY mają mniej poważne zaburzenia.
Pierwsze wyraźne objawy fenotypowe choroby pojawiają się w okresie ontogenezy przedpokwitaniowej i dojrzewania. Przed dojrzewaniem chłopcy mogą mieć wnętrostwo (zwykle obustronne) i małego penisa. 50% chłopców ma umiarkowane upośledzenie umysłowe, któremu towarzyszą zaburzenia zachowania i trudności w kontaktach z rówieśnikami. Chłopcy mają zazwyczaj długość ciała powyżej średniej dla swojego wieku. Charakterystyczne są stosunkowo długie kończyny i nadmierne odkładanie się tłuszczu typu żeńskiego (typ budowy ciała eunuchoidalnego).

Drugorzędne cechy płciowe pojawiają się późno. Najbardziej charakterystycznym objawem zespołu Klinefeltera jest hipoplazja jąder i prącia (hipogonadyzm i hipogenitalizm). Ginekomastię wykrywa się u 50% pacjentów w okresie dojrzewania. Występuje nieznaczny spadek inteligencji, co wpływa na wyniki w szkole. Dorośli pacjenci są podatni na alkoholizm, narkomanię, homoseksualizm i zachowania antyspołeczne, szczególnie pod wpływem stresu.
Dojrzewanie zwykle zaczyna się w normalnym wieku, ale zarost jest często niski. Dzieci te są predysponowane do niepełnosprawności w uczeniu się, a wiele z nich ma obniżoną inteligencję werbalną, upośledzoną percepcję słuchową i przetwarzanie informacji oraz upośledzone umiejętności czytania. Zmienność kliniczna jest znaczna, wielu chłopców i mężczyzn z kariotypem 47,XXY ma normalny wygląd i normalną inteligencję.
W okresie dojrzewania wtórny wzrost włosów pojawia się w zwykłym czasie, zauważa się również powiększenie penisa. Jednak objętość jąder zwiększa się tylko nieznacznie, zwykle nie przekraczając 8 ml; jądra mają gęstą konsystencję. Ginekomastia pokwitaniowa, często dość wczesna, jest wykrywana u 40-50% chłopców. U tych pacjentów występuje następnie zwiększone ryzyko rozwoju raka piersi. Dojrzewanie kości zwykle odpowiada wiekowi w momencie rozpoczęcia dojrzewania, ale późniejsze różnicowanie kości szkieletowych jest opóźnione z powodu niewystarczającego wydzielania testosteronu. Liniowy wzrost kończyn trwa do 18-20 roku życia, co prowadzi do ukształtowania eunuchoidalnych proporcji ciała; ostateczny wzrost pacjentów jest zwykle wyższy niż wzrost ich rodziców. Inwolucja jąder po okresie dojrzewania prowadzi do hipogonadyzmu i utraty płodności. Badanie histologiczne ujawnia hialinozę kanalików nasiennych i brak spermatogenezy. Liczba komórek Leydiga może być prawidłowa, jednak wraz z wiekiem ulegają one zanikowi.
Oprócz objawów zaburzeń rozwoju płciowego u pacjentów z zespołem Klinefeltera może występować szereg wrodzonych anomalii tkanki kostnej: klinodaktylia, deformacja mostka, koślawość łokcia, koślawość biodra, hiperteloryzm, mikrognacja, podniebienie „gotyckie” itp. Chorobie często towarzyszą wrodzone wady układu sercowo-naczyniowego. U pacjentów często wykrywa się nowotwory złośliwe, w szczególności istnieją informacje o wysokiej częstości występowania guzów zarodkowych.
Mozaicyzm występuje w 15% przypadków. Tacy mężczyźni mogą mieć dzieci. Niektórzy mężczyźni mogą mieć 3, 4, a nawet 5 chromosomów X wraz z jednym chromosomem Y. Wraz ze wzrostem liczby chromosomów X, nasilenie upośledzenia umysłowego i wad rozwojowych wzrasta.
Rozpoznanie zespołu Klinefeltera
Zespół Klinefeltera często jest wykrywany podczas oceny niepłodności (prawdopodobnie wszyscy mężczyźni 47,XXY są bezpłodni). Rozwój jąder różni się od zhialinizowanych, niefunkcjonujących struktur kanalikowych do pewnej produkcji plemników; często obserwuje się zwiększone wydalanie hormonu folikulotropowego z moczem.
Jeśli występują objawy fenotypowe zespołu Klinefeltera, określa się chromatynę płciową. Jeśli test jest pozytywny, wskazane jest kariotypowanie. W większości przypadków wykrywa się kariotyp 47, XXY lub jego wariant mozaikowy. Jednak spotyka się również inne warianty cytogenetyczne zespołu, na przykład 48, XXXY; 48, XXYY.
 [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ]
[ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ]
Cechy funkcji gonadotropowych i gonadowych
W wieku przedpokwitaniowym poziomy LH, FSH i T u chłopców z zespołem Klinefeltera są zazwyczaj prawidłowe. Na początku okresu dojrzewania poziom FSH wzrasta i w wieku 14-15 lat znacznie przekracza normę. Poziom testosteronu w okresie dojrzewania zwykle wzrasta, ale jego stężenie nie osiąga normy. Poziom LH w okresie dojrzewania jest prawidłowy, ale później, w miarę obniżania się poziomu testosteronu, wzrasta stężenie LH. Reakcja LH i FSH na wprowadzenie GnRH ma zazwyczaj charakter hiperergiczny już we wczesnych stadiach dojrzewania
Proces powstawania niedoboru androgenów, który jest wtórny do pierwotnego uszkodzenia nabłonka zarodkowego jąder, nie jest obecnie w pełni poznany. Wczesna śmierć nabłonka spermatogennego prowadzi do niedoboru komórek Sertoliego, które wydzielają inhibinę, naturalny regulator wydzielania FSH u mężczyzn. W rezultacie poziom FSH u pacjentów jest podwyższony od wczesnego okresu dojrzewania. Jednak produkcja testosteronu i wydzielanie LH nie są upośledzone w pierwszych latach dojrzewania i po okresie dojrzewania, dopiero później następuje spadek wydzielania testosteronu i wzrost wydzielania LH - rozwój hipogonadyzmu hipergonadotropowego. Oczywiste jest, że nabłonek zarodkowy i komórki Sertoliego mają pewien wpływ troficzny na śródmiąższowe komórki Leydiga, a brak ich wpływu troficznego uniemożliwia prawidłowe wydzielanie testosteronu.
 [ 15 ], [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ], [ 21 ], [ 22 ]
[ 15 ], [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ], [ 21 ], [ 22 ]
Diagnostyka różnicowa zespołu Klinefeltera
W przypadku stwierdzenia objawów zespołu Klinefeltera przy prawidłowym kariotypie (46, XY) należy wykluczyć inne formy hipogonadyzmu.
Jak leczy się chorobę Klinefeltera?
W okresie dojrzewania podaje się androgeny, co stymuluje rozwój drugorzędnych cech płciowych, jednak nie powoduje to wyleczenia niepłodności.
U nastolatków z zespołem Klinefeltera, pomimo częściowego niedoboru androgenów, terapia estrami testosteronu według schematu standardowego powinna być przepisywana od 13-14 roku życia. Preparaty androgenowe znacząco poprawiają adaptację i inteligencję nastolatka, zapobiegają rozwojowi eunuchoidyzmu. Długotrwała obserwacja nastolatków z zespołem Klinefeltera wykazała, że wczesna terapia preparatami testosteronu znacząco zwiększa inteligencję dorosłych pacjentów, ich zdolność do pracy i adaptację społeczną.
 [ 25 ]
[ 25 ]
Ocena skuteczności leczenia
Kryterium skuteczności leczenia jest wykształcenie się drugorzędnych cech płciowych.
Powikłania i skutki uboczne leczenia
Wprowadzenie estrów testosteronu może powodować zatrzymanie płynów i pobudzenie w pierwszych dniach po wstrzyknięciu.
Monitorowanie ambulatoryjne prowadzi endokrynolog.
Jakie są rokowania w zespole Klinefeltera?
Zespół Klinefeltera ma inną prognozę i zależy od postaci choroby, połączonych zaburzeń hormonalnych i somatycznych. Terapia zastępcza hormonami płciowymi jest dożywotnia.
Использованная литература